
Угловое уравнение.
Движение электрона
в водородоподобном атоме, по координатам
![]() и
и
![]() ,
описываемое функцией
,
описываемое функцией
![]() ,
можно рассматривать, как ротатор.
,
можно рассматривать, как ротатор.
Угловое уравнение вида
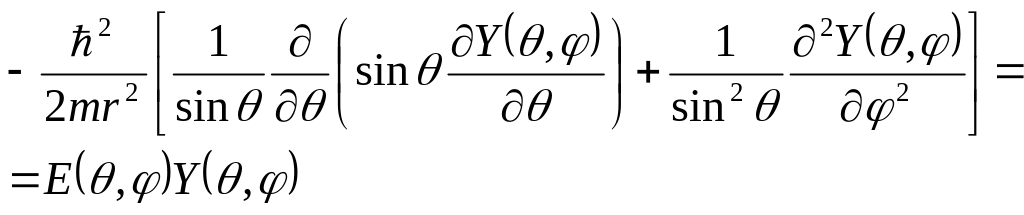
или
![]() ,
,
где собственные значения энергии
![]() ,
,
а собственные значения квадрата момента импульса
![]() .
.
Собственными
функциями оператора
![]() являются шаровые функции вида:
являются шаровые функции вида:
![]() ,
,
где
![]() - присоединенные полиномы Лежандра
- присоединенные полиномы Лежандра
![]() .
.
Орбитальное
(азимутальное) квантовое число
![]() определяет момент импульса электрона
в атоме, т.е. конфигурацию электронного
облака и принимает
определяет момент импульса электрона
в атоме, т.е. конфигурацию электронного
облака и принимает
![]() значений:
значений:
![]() .
.
Квантовое
число
![]() - магнитным
квантовым числом.
Оно определяет проекцию момента импульса
на произвольно выбранную ось:
- магнитным
квантовым числом.
Оно определяет проекцию момента импульса
на произвольно выбранную ось:
![]() ,
,
![]() ,
но
,
но
![]() ,
,
![]() и
и
![]() принимает
принимает
![]() значений:
значений:
![]() .
.
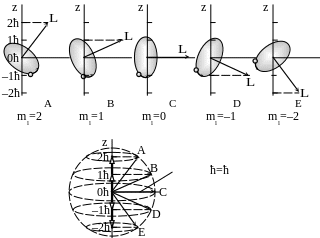 определяет
дискретные значения проекции момента
импульса на выбранное направление,
т.е., определяет ориентацию оси симметрии
и конфигурацию распределения электронного
облака в пространстве.
определяет
дискретные значения проекции момента
импульса на выбранное направление,
т.е., определяет ориентацию оси симметрии
и конфигурацию распределения электронного
облака в пространстве.
Электрон
создает магнитный момент
![]() :
:
![]() ,
,
где
![]() - гиромагнитное отношение,
- гиромагнитное отношение,
![]() -
магнетон Бора ,
-
магнетон Бора ,
![]() .
.
Числовое
значение
![]() совпадает со значением, полученным из
теории Бора.
совпадает со значением, полученным из
теории Бора.
Проекция
магнитного момента на ось
![]()
![]() ,
следовательно,
,
следовательно,
![]() ,
,
где - магнитное квантовое число.
П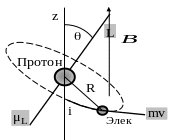 ри
наложении внешнего магнитного поля
происходит взаимодействие магнитного
момента
атома с
ри
наложении внешнего магнитного поля
происходит взаимодействие магнитного
момента
атома с
![]() .
В результате атом получает дополнительную
энергию
.
В результате атом получает дополнительную
энергию
![]()
Используя
![]() ,
получаем
,
получаем
![]() .
.
Проекции
момента импульса принимают дискретные
значения (пространственное квантование
![]() ):
):
![]() .
.
Тогда
![]() ,
,
Полная энергия атома в магнитном поле
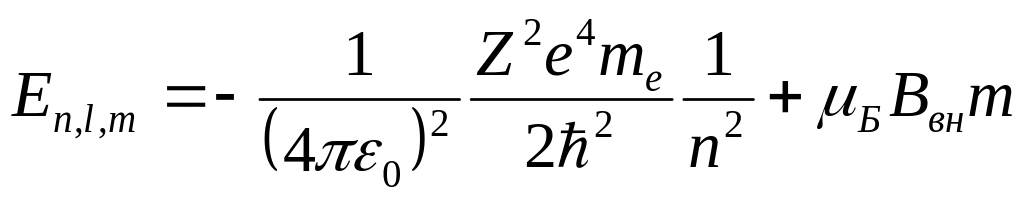 .
.
Для атома водорода
при
![]() ;
;
![]() ;
;
![]() .
.
Если
![]() ,
то
,
то
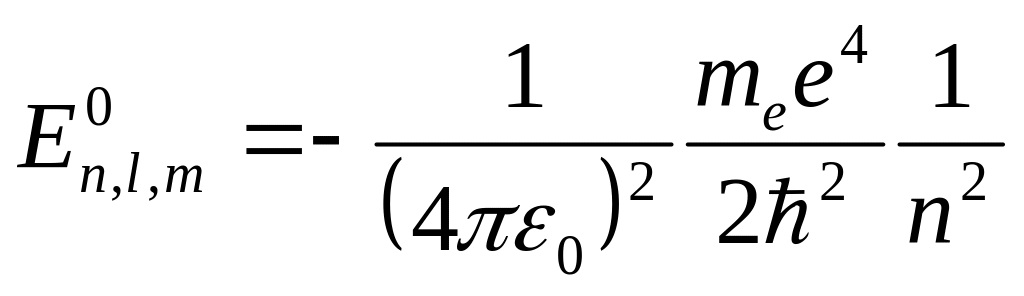 .
.
Если
![]() ,
то
,
то
![]() .
.
Уровень
энергии
![]() расщепляется на 3 подуровня
расщепляется на 3 подуровня
![]() ;
;
![]() ;
;
![]() ;
;
![]() .
.
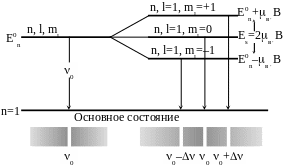
Полное число состояний в атоме водорода. Квантовые числа.
Рассмотрим полное число состояний в атоме водорода в общем случае.
![]() .
.
Подставив
![]() в уравнение Шредингера, мы получили два
взаимосвязанных уравнения для функций
в уравнение Шредингера, мы получили два
взаимосвязанных уравнения для функций
![]() и
и
![]() .
.
Эти функции имеют вид
![]() ,
,
![]() ,
,
![]() ;
;
Где
![]() -
полином Лагерра,
-
полином Лагерра,
- полиномы Лежандра.
Тогда решение
![]() =
=
![]()
![]()
![]()
содержит
три целочисленных параметра – три
квантовых числа:
![]() ,
,
![]() и
.
и
.
Главное
квантовое число
определяет энергию электрона в атоме
и может принимать значения
![]() - это по существу номер уровня энергии.
- это по существу номер уровня энергии.
Орбитальное
(азимутальное) квантовое число
определяет модуль момента импульса
электрона
![]() и может принимать значения
и может принимать значения
![]() (всего
значений). Значения
определяет азимутальное распределение
плотности вероятности локализации
электрона в атоме (форму электронного
облака).
(всего
значений). Значения
определяет азимутальное распределение
плотности вероятности локализации
электрона в атоме (форму электронного
облака).
Магнитное
квантовое число
определяет проекцию
![]() на произвольно выбранное направление
(или ориентацию электронного облака в
пространстве) и может принимать значения
(всего
значений).
на произвольно выбранное направление
(или ориентацию электронного облака в
пространстве) и может принимать значения
(всего
значений).
Полное число состояний для данного
![]() ,
,
т.е.,
данной энергии
![]() соответствует
соответствует
![]() состояний (или
функций). Состояния с одинаковой энергией
называются вырожденными,
а число этих состояний называется
кратностью
вырождения.
состояний (или
функций). Состояния с одинаковой энергией
называются вырожденными,
а число этих состояний называется
кратностью
вырождения.
В
атомной физике состояния принято
обозначать символами
![]() ,
,
![]() ,
,
![]() и т.д. (по числу
):
и т.д. (по числу
):
![]() -
-состояние,
-
-состояние,
![]() -
-состояние,
-
-состояние,
![]() -
-состояние,
-
-состояние,
![]() -
-
![]() -состояние
и т.д.
-состояние
и т.д.
Значение главного квантового числа указывается перед обозначением квантового числа :
![]() -состояние
-состояние
![]() ,
;
,
;
![]()
![]() -состояние
-состояние
![]() ,
,
,
,
![]()
![]() -состояния
,
-состояния
,
![]() ,
,
![]()
![]() -состояние
-состояние
![]() ,
,
,
,
![]() -состояния
,
,
-состояния
,
,
![]() -состояния
-состояния
![]() ,
,
![]() ,
,
![]() .
.
Волновую
функцию
![]() часто называют атомной
орбиталью (АО)
и, в зависимости от того, какое значение
принимает орбитальное число
,
говорят, что электрон находится на
-,
-,
-,
… орбитали.
часто называют атомной
орбиталью (АО)
и, в зависимости от того, какое значение
принимает орбитальное число
,
говорят, что электрон находится на
-,
-,
-,
… орбитали.
Полная энергия электрона в атоме водорода
![]() ,
,
где .
Этот результат совпадает с выводами теории Бора. Однако в квантовой механике эти значения получаются как следствия основных положений квантовой механики, тогда как в теории Бора такой результат получался при специальных предположениях.
