
- •Дослідження автомобільних акумуляторів
- •1. Мета роботи
- •2.2. Будова акумуляторних батарей
- •2.3. Основні характеристикистартерних акумуляторних батарей
- •2.4. Технічне обслуговування акумуляторних батарей
- •3. Програма роботи
- •4. Вимірювальні прилади та електрична схема лабораторної установки
- •5. Порядок виконання роботи
- •6. Обсяг та зміст звіту
Міністерство освіти і науки, молоді та спорту України
Національний державний університет водного
господарства та природокористування
Кафедра електротехніки та автоматики
Лабораторна робота №1
з курсу „Електричне та електронне обладнання автомобілів.”
Дослідження автомобільних акумуляторів
Підготував:
Студент МЕФ, ААГ-31
Козачок А.В.
Перевірив:
Стець С.Є.
Рівне 2012
Методичні вказівки: до виконання лабораторної роботи „Електричне та електронне обладнання автомобілів” Дослідження автомобільних акумуляторів / В.М.Арсенюк, Рівне: НУВГП, 2005
Упорядник В.М.Арсенюк ст.., викладач
Відповідальний за випуск Б.О.Баховець, професор, завідувач кафедри електротехніки і автоматики, академік УЕАН / В.М.Арсенюк, Рівне: НУВГП, 2005
©Арсенюк В.М., 2005
©НУВГП, 2005
Дослідження автомобільних акумуляторних батарей
1. Мета роботи
Вивчити методи і прилади визначення технічного стану акумуляторних батарей та дослідити їх електричні параметри і характеристики.
Теоретичні відомості
Стартерні акумуляторні батареї (САБ) являються одним з двох джерел електричної енергії в системі електропостачання автомобілів (другим джерелом є автомобільний генератор).
Основне призначення САБ – забезпечення стартерного пуску автомобільних двигунів внутрішнього згоряння (Д.В.З.)
Пуск
ДВЗ здійснюється за рахунок його розгону
прикладеним до нього крутним моментом
від стартерного електричного двигуна
(С.Е.Д.), який живиться в свою чергу від
С.А.Б. Поскільки бартова електрична
мережа автомобіля має низьку напругу
![]() або
або
![]() ,
то для забезпечення розгону Д.В.З. СЕД
повинен споживати хоча і короткочасно
від САБ дуже великий струм
,
то для забезпечення розгону Д.В.З. СЕД
повинен споживати хоча і короткочасно
від САБ дуже великий струм
![]() .
Необхідність живлення СЕД великими
струмами визначили тип акумуляторних
батарей, а саме – свинцево-кислотні
акумуляторні батареї, які мають найменший
власний (внутрішній) опір серед інших
типів акумуляторів (наприклад, лужних
акумуляторів).
.
Необхідність живлення СЕД великими
струмами визначили тип акумуляторних
батарей, а саме – свинцево-кислотні
акумуляторні батареї, які мають найменший
власний (внутрішній) опір серед інших
типів акумуляторів (наприклад, лужних
акумуляторів).
У будь-якому джерелі енергії відбувається перетворення енергії з одного виду на інший. Свинцевий акумулятор належить до хімічних джерел струму, які перетворюють енергію, що виділяється під час хімічних реакцій, на електричну.
У свинцевому акумуляторі процеси протікають зворотно. Активні речовини, витрачені в процесі реакції, можуть відновлюватися під час пропускання через акумулятор постійного струму від іншого джерела електричної енергії. Процес, під час якого хімічна енергія перетворюється на електричну, називається розряджанням, зворотний процес — заряджанням.
Активні речовини зарядженого акумулятора: діоксид свинцю РЬО2 темно-коричневого кольору на позитивному електроді, губчастий свинець РЬ темно-сірого кольору на негативному електроді і водний розчин сірчаної кислоти H2SO4+Н2О — електроліт, в якому розміщено електроди. Якщо позитивний та негативний електроди з'єднати між собою споживачем електричної енергії, наприклад, лампочкою(рис.1.1,а), то через неї (зовнішня ділянка кола) і акумулятор (внутрішня ділянка кола) протікатиме розрядний струм.
Під час розряджання акумулятора активна маса негативного й позитивного електродів перетворюється на сульфат свинцю PbSO4. Темно-сірий колір негативного електрода змінюється на світло-сірий, а темно-коричневий позитивного — на світло-коричневий. Оскільки в процесі розряджання на проходження реакції витрачається сірчана кислота й утворюється вода, то густина електроліту поступово зменшується.
б
а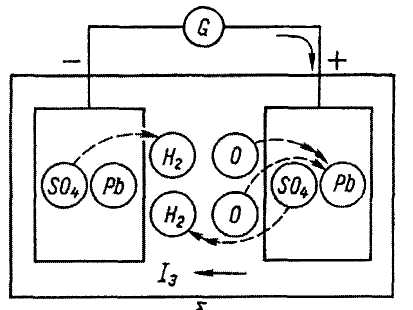
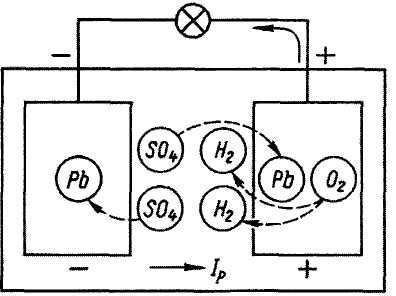
Рис. 1.1. Схеми процесів, які відбуваються у свинцевому акумуляторі: а – розрядження; б – зарядження
кислоти в електроліті, завдяки чому густина його збільшується.
Після повного відновлення активних речовин позитивного негативного елетродів густина електроліту далі не збільшується. Це є ознакою закінчення заряджання акумулятора.
Наприкінці заряджання розпочинається процес розкладання води на кисень та водень, і на поверхні електроліту виникають бульбашки газу. Цей процес називається «кипінням» електроліту.
Хімічні зміни, які відбуваються під час розряджання-заряджання свинцевого акумулятора, можна описати рівнянням:
РЬО2 + РЬ + 2H2SO4 = 2PbSO4 + 2Н2О,
де зліва праворуч маємо процес розряджання, а справа ліворуч — заряджання.
