
- •Повторення основних питань курсу хімія
- •Валентність атомів деяких елементів у сполуках
- •Класифікація неорганічних сполук Оксиди
- •Класифікація
- •Добування
- •Хімічні властивості
- •Хімічні властивості
- •Кислоти
- •За числом атомів водню, які можуть заміщуватися на метал:
- •Добування
- •Хімічні властивості
- •Класифікація
- •Середні солі Добування
- •Хімічні властивості
- •Окисно-відновні реакції
- •Неметали та їх сполуки
- •Взаємодія неметалів з металами:
- •2. Взаємодія неметалів із неметалами.
- •Добування кисню:
- •Властивості кисню й озону
- •Сульфур
- •Алотропні видозміни Карбону
- •Вуглець
- •Нітроген
- •Сполуки неметалічних елементів ізГідрогеном
- •Хлороводень і хлороводнева кислота
- •Амоніак
- •Солі амонію
- •Виділення амоніаку – характерна ознак для розпізнавання солей амонію.
- •Розв’язування розрахункових задач на надлишок та вихід продукту.
- •1.Розвязування задач на визначення масової частки, об’єму та кількості речовини.
- •Самостійна робота:
- •Розв’язування задач на надлишок
- •Розв’язування задач на вихід продукту реакції
- •Оксиди неметалічних елементів. Оксиди Сульфуру
- •Оксиди Нітрогену
- •Хімічні властивості.
- •Оксиди Фосфору
- •Оксиди Карбону
- •Оксиди силіцію
- •Сульфатна кислота
- •Розбавлена сульфатна кислота
- •Концентрована сульфатна кислота
- •Добування і застосування сульфатної кислоти
- •Сульфати
- •Нітратна та ортофосфатна кислота
- •Мінеральні добрива
- •Карбонатна і силікатна кислота
- •Кристалічні гратки металів
- •Загальні фізичні властивості металів
- •Хімічні властивості металів.
- •Фізичні властивості лужних металів
- •Хімічні властивості лужних металів
- •Добування лужних металів
- •Оксиди лужних металів
- •Застосування оксидів лужних металів.
- •Гідроксиди лужних металів
- •Лужно-земельні метали
- •Кальцій
- •Кальцій оксид
- •Кальцій гідроксид
- •Алюміній
- •Алюміній оксид
- •Алюміній гідроксид
- •Солі Алюмінію
- •Оксиди і гідроксиди Феруму
- •Сполуки Феруму(ііі).
- •Органічна хімія
- •Отримання алкенів
- •Отримання алкінів
- •Отримання і хімічні властивості ароматичних вуглеводнів
- •Розв'язування задач на виведення молекулярної формули речовини.
- •Оксигеновмісні органічні сполуки
- •Альдегіди і карбонові кислоти
- •Естери і жири
- •Отримання і хімічні властивості жирів
- •Вуглеводи
- •Глюкоза
- •Сахароза
- •Крохмаль і целюлоза
- •Характеристики амінів
- •Амінокислоти
- •Реакції амінокислот
- •Загальні правила роботи і техніка безпеки в хімічній лабораторії
Застосування оксидів лужних металів.
|
Гідроксиди лужних металів
Гідроксиди лужних металів – NaOH, KOH – кристалічні речовини йонної будови, білого кольору, легко поглинають вологу, особливо натрій гідроксид NaOH, добре розчиняються у воді з виділенням великої кількості теплоти.
Хімічні властивості гідроксидів лужних металів.
Гідроксиди натрію та калію роз’їдають тканини, шкіру, органічні речовини, тому їх називають їдкими лугами.
дисоціація на йони:
1.Дисоціація
У водних розчинах гідроксиди лужних металів повністю дисоціюють на йони:
![]()
2.дія на індикатори:
*пригадайте,як діють луги на індикатори
|
|
3.взаємодія з кислотами:
Гідроксиди лужних металів вступають у реакцію нейтралізації з кислотами, утворюючи середні або кислі солі та воду:
2NaOH + H2SO4 = Na2SO4 + 2H2O
NaOH + H2SO4 = NaHSO4 + H2O
*напишіть як будуть взаємодіяти луги з фосфатною ,карбонатною ,хлоридною та нітратною кислотою.Які солі будуть утворюватись при надлишку одного з реагентів?
4.взаємодія з кислотними оксидами:
2KOH + SO3 = K2SO4 + H2O
2NaOH + SiO2 = Na2SiO3 + H2O - сплавляння
*напишіть рівняння реакцій взаємодії лугів з вуглекислим газом,сульфур (4)оксидом,оксидом фосфору(5).
5.взаємодія з амфотерним оксидами:
2NaOH + ZnO = Na2ZnO2 + H2O – сплавляння
2KOH + Al2O3 = 2KAlO2 + H2O - сплавляння
6.взаємодія з амфотерним гідроксидами:
2NaOH + Zn(OH)2 = Na2ZnO2 + 2H2O – сплавляння
2NaOH + Zn(OH)2 = Na2[Zn(OH)4] - у розчині
7.взаємодія з металами, яким відповідають амфотерні гідроксиди:
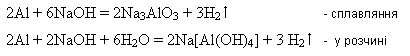
8.взаємодія з солями
Реакція між гідроксидами і солями відбувається за типом реакції обміну, яка проходить тільки в розчині, при цьому утворюються або основні солі, або нерозчинні у воді основи:
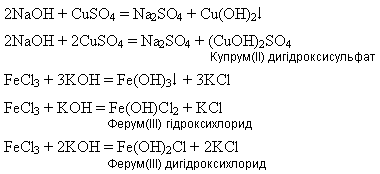
*допишіть рівняння реакцій,складіть повне та скорочене іонне рівняння
FeCl3 + 3 NaOH =
Cr(NO3)2 + 2 KOH =
9.взаємодія з натрій ацетатом:
![]()
10.взаємодія з галогенами:

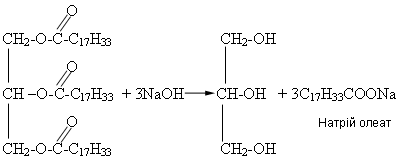
11.взаємодія з жирами:
Під дією лугів на рослинні олії або тваринніжири утворюються розчинні солі вищих карбонових кислот, які є основною складовою частиною мила:
Добування лугів.
*на основі знань про основні класи неорганічних сполук запропонуйте кілька способів добування лугів
1)
2)
3)
Застосування лугів.
Луги застосовують у виробництві фарб, мила, штучного волокна, паперу, текстилю, очищення нафтопродуктів та ін.
* Na→Na2O→NaOH→Na2SO4→Na→Na2S
*K→KOH→KCI→K2SO4→ KOH→K3AIO3
*Добудьте,використовуючи калій, кисень ,воду,сульфатну кислоту ,як найбільше сполук
