
- •Векторные модели атомов.
- •Полный магнитный момент атома.
- •Атом во внешнем магнитном поле. Эффект Зеемана.
- •Принцип тождественности микрочастиц. Принцип Паули.
- •Принцип тождественности (неразличимости) микрочастиц является фундаментальным принципом и состоит в том, что экспериментально различить тождественные частицы невозможно.
- •Распределение электронных состояний в атоме. Периодическая система химических элементов д.И.Менделеева.
Принцип тождественности микрочастиц. Принцип Паули.
В классической механике одинаковые частицы (электроны, протоны, элементарные частицы, атомы и т.д.) не теряют своей индивидуальности. Можно проследить за изменением состояния каждой частицы, ее траекторией и импульсом.
В квантовой механике выполняется соотношение неопределенностей, и понятие траектории не имеет смысла.
В квантовой механике одинаковые частицы теряют свою индивидуальность и тождественно неразличимы.
Принцип тождественности (неразличимости) микрочастиц является фундаментальным принципом и состоит в том, что экспериментально различить тождественные частицы невозможно.
Принцип тождественности микрочастиц можно также определить следующим образом: в системе одинаковых частиц реализуются только такие состояния, которые не меняются при перестановке местами двух любых частиц.
Например,
система из 2-х частиц описывается функцией
![]() ,
где
,
где
![]() и
и
![]() -
совокупность независимых переменных,
определяемых местоположением и спином
частицы. Если частицы поменять местами,
то функция
-
совокупность независимых переменных,
определяемых местоположением и спином
частицы. Если частицы поменять местами,
то функция
![]() может измениться только на фазовый
множитель
может измениться только на фазовый
множитель
![]() (так, чтобы
(так, чтобы
![]() осталось неизменным). В результате
получаем:
осталось неизменным). В результате
получаем:
![]()
![]() и
и
![]() ,
,
где
![]() - некоторая вещественная постоянная.
- некоторая вещественная постоянная.
Тогда
![]() .
.
Из этого
выражения следует, что
![]() ,
тогда
,
тогда
![]() .
Это означает, что
.
Это означает, что
![]() =
=![]() .
Знаки
.
Знаки
![]() ”+”
и “-“ означают симметричные и
антисимметричные состояния, определяемые
спином.
”+”
и “-“ означают симметричные и
антисимметричные состояния, определяемые
спином.
Частицы, состояния которых описываются антисимметричными функциями, называются фермионами. Это частицы с полуцелым спином (например, электроны, протоны, нейтроны, нейтрино). Системы, образованные этими частицами, подчиняются статистике Ферми-Дирака.
Симметричные
функции описывают состояния частиц
называемых бозонами.
Это частицы с целым спином, к ним
относятся, например, фотоны,
![]() -
и
-
и
![]() -
мезоны. Системы частиц, состоящих из
бозонов, подчиняются статистике
Бозе-Эйнштейна.
-
мезоны. Системы частиц, состоящих из
бозонов, подчиняются статистике
Бозе-Эйнштейна.
Рассмотрим
систему, состоящую из
![]() электронов. Каждая частица может
находиться в одном из состояний
электронов. Каждая частица может
находиться в одном из состояний
![]() .
Амплитуда вероятности
.
Амплитуда вероятности
![]() -
го состояния системы будет
-
го состояния системы будет
![]() ,
,
где
![]() -
номер частицы.
-
номер частицы.
![]() -
функция – это суперпозиция всех возможных
состояний системы
-
функция – это суперпозиция всех возможных
состояний системы
![]() .
.
Для системы из 2-х электронов реализуется антисимметричная комбинация:
![]()
или
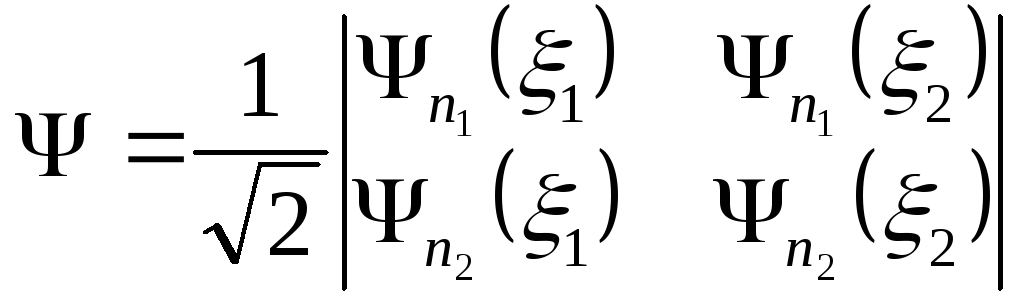 .
.
Для
системы из
![]() электронов:
электронов:
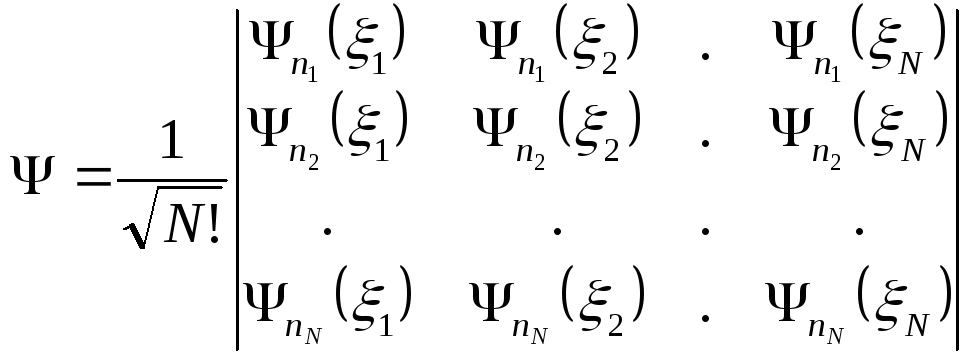 .
.
Если из
![]() - состояний окажется два одинаковых
состояния, например,
- состояний окажется два одинаковых
состояния, например,
![]() ,
то две строки определителя будут
одинаковыми, и определитель станет
равным нулю (из свойств определителя).
Получается, что вероятность такой
ситуации тождественно равна нулю.
Следовательно, для того, чтобы
,
то две строки определителя будут
одинаковыми, и определитель станет
равным нулю (из свойств определителя).
Получается, что вероятность такой
ситуации тождественно равна нулю.
Следовательно, для того, чтобы
![]() ,
необходимо, чтобы состояния
,
необходимо, чтобы состояния
![]() были различными.
были различными.
Отсюда следует важный вывод: в системе частиц с полуцелым спином (например, электронов) в одном и том же квантовом состоянии не может находиться более одной частицы. Это – так называемый принцип Паули, установленный в 1925 г.
Следовательно,
в атоме каждый электрон может находиться
в состоянии, характеризуемом квантовыми
числами
![]() ,
,
![]() ,
,
![]() ,
,
![]() .
.
Распределение электронных состояний в атоме. Периодическая система химических элементов д.И.Менделеева.
Рассмотрим
атом в невозбужденном состоянии.
Состояние каждого электрона этой системы
описывается квантовыми числами
![]() ,
,
![]() ,
,
![]() и
и
![]() .
.
Электроны в атомах распределяются по состояниям в определенном порядке в соответствии с принципом Паули, т.е. в каждом состоянии может находиться не более одной частицы с полуцелым спином.
Энергия
электрона определяется главным образом
числами
![]() и
и
![]() (от взаимной ориентации моментов
(от взаимной ориентации моментов
![]() и
и
![]() ,
т.е. от квантовых чисел
,
т.е. от квантовых чисел
![]() и
и
![]() ,
энергия электрона зависит значительно
слабее). Совокупность электронов с
одинаковым
,
энергия электрона зависит значительно
слабее). Совокупность электронов с
одинаковым
![]() образует оболочку (оболочки принято
обозначать буквами
образует оболочку (оболочки принято
обозначать буквами
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() и т.д.). Число электронных состояний
(уровней) в оболочке с учетом спина равно
кратности вырождения, т.е. равно
и т.д.). Число электронных состояний
(уровней) в оболочке с учетом спина равно
кратности вырождения, т.е. равно
![]() .
Оболочки подразделяются на подоболочки,
отличающиеся значением числа
.
Оболочки подразделяются на подоболочки,
отличающиеся значением числа
![]() .
.
Как же заполняются электронные оболочки атомов?
![]() (
(![]() -оболочка);
-оболочка);![]() (
(![]() -состояние);
-состояние);
![]() ;
;
![]() 2 электрона; форма облака – сфера.
2 электрона; форма облака – сфера.
![]() (
(![]() -оболочка);
-оболочка);
![]() (
(![]() -состояние);
-состояние);
![]() ;
;
![]()
![]() (
(![]() -состояние);
-состояние);
![]() ;
;
![]() 8 электронов
8 электронов
![]() ;
;
![]()
![]() ;
;
![]()
форма облака – 3 гантели, ориентированные в 3-х взаимноперпендикулярных направлениях.
![]() (
(![]() -оболочка);
-оболочка);
![]() (
(![]() -состояние);
-состояние); ![]() ;
;
![]()
![]() (
(![]() -состояние);
-состояние); ![]() ;
;
![]() 8 электронов
8 электронов
![]() ;
;
![]()
![]() ;
;
![]()
![]() (
(![]() -состояние);
-состояние); ![]() ;
;
![]()
![]() ;
;
![]()
![]() ;
;
![]() 18 электронов
18 электронов
![]() ;
;
![]()
![]() ;
;
![]()
Символы
![]() наглядно обозначают
наглядно обозначают
![]() .
.
Полностью
заполненные оболочки и подоболочки
имеют
![]() ,
,
![]() и
и
![]() .
.
Например,
![]() -подоболочка:
-подоболочка:
![]() и это единственное значение, поэтому
и это единственное значение, поэтому
![]() ,
также
,
также
![]() (т.к.
(т.к.![]() ),
следовательно,
),
следовательно,
![]() .
.
Это
важный результат: при определенных
квантовых числах
![]() и
и
![]() атома заполненные оболочки можно не
принимать во внимание. Оболочки (или
подоболочки), полностью заполненные
электронами, называют замкнутыми.
Основным термом замкнутых оболочек
(подоболочек) является
атома заполненные оболочки можно не
принимать во внимание. Оболочки (или
подоболочки), полностью заполненные
электронами, называют замкнутыми.
Основным термом замкнутых оболочек
(подоболочек) является
![]() .
.
Закономерность заполнения электронных оболочек в атомах соответствует периодической системе элементов Менделеева.
Если
происходит заполнение только
![]() -оболочки
– это I
период (H,
He),
заполнение
-оболочки
– это I
период (H,
He),
заполнение
![]() -
и
-
и
![]() -оболочкек
– II
период (от Li до Ne), заполнение
-оболочкек
– II
период (от Li до Ne), заполнение
![]() -,
-,![]() -
и
-
и
![]() -оболочки
– III период (от Na до Ar,
-оболочки
– III период (от Na до Ar,
![]() -
и
-
и
![]() -
состояния).
-
состояния).
Каждый следующий атом получается из предыдущего добавлением одного электрона, который помещают в разрешенное принципом Паули состояние.
Распределение
электронов в атоме называется электронной
конфигурацией. Например, электронная
конфигурация Na
-
![]() .
Здесь полностью заполнены
.
Здесь полностью заполнены
![]() -
и
-
и
![]() -оболочки.
Электрон в
-оболочки.
Электрон в
![]() -
состоянии является валентным. Терм
атома натрия в основном состоянии
-
состоянии является валентным. Терм
атома натрия в основном состоянии
![]() .
Следует отметить, что наблюдаемая
периодичность химических и ряда
физических свойств объясняется поведением
именно внешних, валентных электронов.
.
Следует отметить, что наблюдаемая
периодичность химических и ряда
физических свойств объясняется поведением
именно внешних, валентных электронов.
До
IV
периода заполнение оболочек и подоболочек
имеет «идеальный» характер. В четвертом
периоде дальнейшее заполнение электронных
оболочек происходит не за счет заполнения
![]() - состояния
- состояния
![]() -
оболочки, а за счет заполнения
-
оболочки, а за счет заполнения
![]() -
состояния
-
состояния
![]() -оболочки.
Это происходит из-за того, что уровень
-оболочки.
Это происходит из-за того, что уровень
![]() оказывается выше, чем уровень
оказывается выше, чем уровень
![]() .
Такая конфигурация является энергетически
более выгодной. Причина - экранировка
ядра атома внутренними электронами.
Влияние экранировки тем больше, чем
больше число электронов в атоме.
.
Такая конфигурация является энергетически
более выгодной. Причина - экранировка
ядра атома внутренними электронами.
Влияние экранировки тем больше, чем
больше число электронов в атоме.
Термы основных состояний атомов определяются состояниями валентных электронов.
Термы первых четырех элементов можно легко определить – для этого достаточно принципа Паули:
для
водорода -
![]() ,
,
для
гелия -![]() ,
,
для
лития -
![]() ,
,
для
берилия -
![]() .
.
У
бора
![]() пятый электрон занимает одно из
пятый электрон занимает одно из
![]() -состояний
(
-состояний
(![]() ,
,
![]() ,
,
![]() или
или
![]() )
– термы соответствующих состояний
)
– термы соответствующих состояний
![]() и
и
![]() .
Какой из этих термов соответствует
основному состоянию атома? Ответить на
этот вопрос
.
Какой из этих термов соответствует
основному состоянию атома? Ответить на
этот вопрос
позволяют полуэмпирические правила Хунда:
-
из термов, принадлежащих данной электронной конфигурации наименьшей энергией обладает терм с наибольшим квантовым числом
 и наибольшим возможным при данном
и наибольшим возможным при данном
 числом
числом
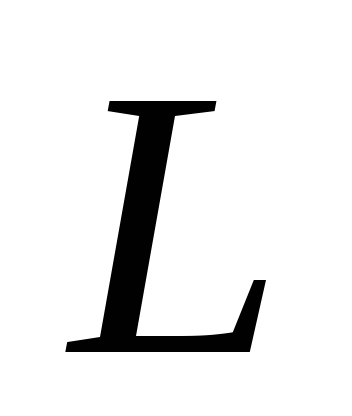 ;
; -
при этом полное квантовое число атома принимает значение
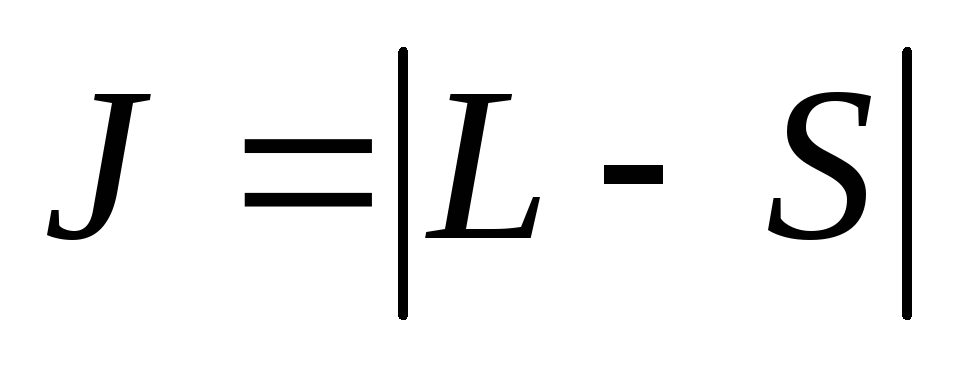 ,
если подоболочка заполнена меньше, чем
наполовину, в остальных случаях
,
если подоболочка заполнена меньше, чем
наполовину, в остальных случаях
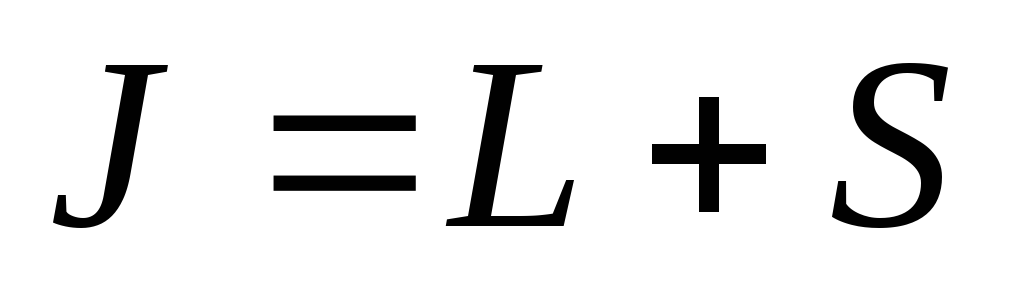 .
.
Минимальной энергии соответствуют состояния с наибольшим значением суммарного спина, а среди них наименьшим будет уровень с наибольшим орбитальным моментом.
