
2014022710224821
.pdf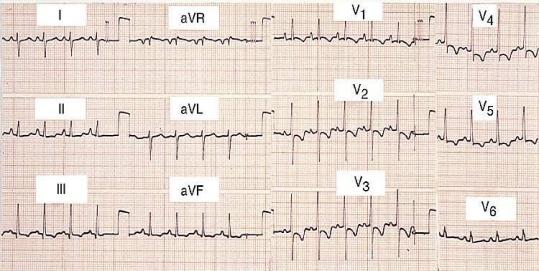
гностические возможности по сравнению с выявлением в крови повышенных уровней кардиоспецифичных ферментов, в первую очередь МВ-КФК.
Определение титров сывороточных антител при вирусных миокардитах. Титры повышаются в 4 и более раза, наибольшее значение имеют специфические IgM антитела к вирусным антигенам.
Инструментальные методы исследования. Электрокардиогра-
фия. Изменения на ЭКГ являются неспецифическими и могут совпадать с таковыми при других заболеваниях сердца (рис. 1). Самыми ранними и наиболее частыми помимо синусовой тахикардии являются изменения зубца Т в виде его уплощения, двухфазности или инверсии, часто наблюдается смещение интервала ST, реже — остроконечный гигантский зубец Т. Считают, что появление атриовентрикулярной блокады, желудочковой аритмии, а также изменений ST-T, схожих с таковыми при миокардиальной ишемии или перикардите (псевдоинфарктная картина), говорит о плохом прогнозе. Изменения на электрокардиограмме чаще появляются в отведениях V1–V6, реже во II, III, aVF, I и aVL отведениях.
Рис. 1. Электрокардиограмма пациента с диффузным острым вирусным миокардитом с неспецифическими изменениями сегмента ST и зубца T
ЭхоКГ проводится для исключения других причин сердечной декомпенсации (клапанных врожденных и приобретенных, амилоидоза и др.), а также для определения степени миокардиальной дисфункции. Нередко выявляется снижение систолической функции миокарда, а при тяжелых формах миокардита — локализация и распространение воспаления (нарушение движения и истончение стенок, перикардиальный выпот) (рис. 2). Эхокардиографическая картина при миокардите может быть схожей с таковой при дилатационной кардиомиопатии, а также при ишемической болезни сердца, поэтому результаты ЭхоКГ с целью подтверждения диагноза миокардита могут быть использованы при выборе пациентов для проведения эндомиокардиальной биопсии.
11
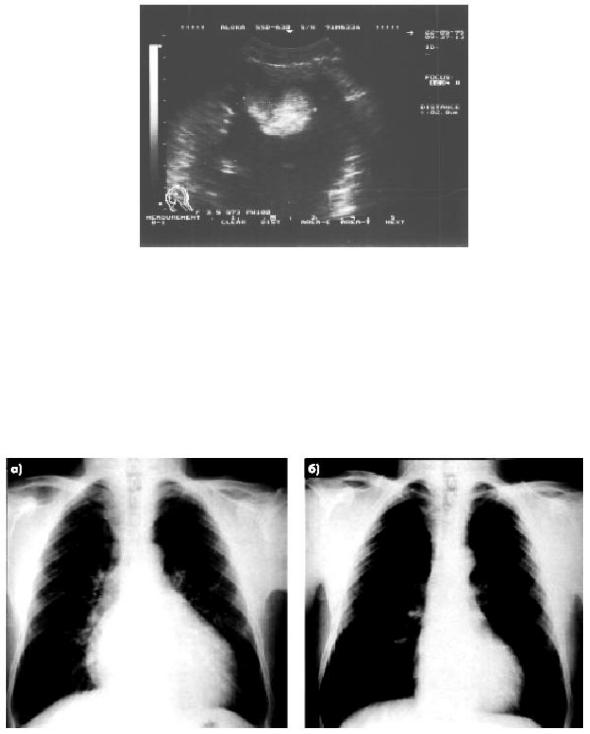
Рентгенологически примерно у половины больных миокардитом обнаруживается увеличение левых размеров сердца, в первую очередь левого желудочка, гораздо реже правых отделов или правых и левых отделов сердца (рис. 3). В легких можно выявить умеренно выраженный венозный застой, широкие корни, усиление венозного рисунка.
Рис. 2. Двухмерная эхокардиограмма, зарегистрированная из апикальной позиции у пациента с острым миокардитом, дилатацией полости левого желудочка и пристеночным тромбом в области верхушки
Выявление изменений в тканях, обусловленных миокардитом, воз-
можно с помощью томографии и сцинциграфии миокарда. Изотопное ис-
следование сердца с галлием-67, технецием-99 и моноклональными антителами к актомиозину, меченными индием-111, МРТ, позитронно-эмиссионная томография позволяют визуализировать зоны повреждения и некроза миокарда и, согласно современным представлениям, являются перспективными.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
а |
|
|
|
б |
|
|
|
|
|
|
|
Рис. 3. Рентгенограмма сердца в прямой проекции пациента с вирусным миокардитом: а) острая фаза болезни; б) после эффективного лечения
12
МРТ миокарда с контрастированием парамагнитными контра-
стирующими препаратами также используется для визуальной диагностики воспалительных процессов. Парамагнитные контрасты (соединения гадолиния) накапливаются во внеклеточной жидкости, вызывают изменение интенсивности МР-сигнала, показывая воспалительный отек. Таким образом можно судить не только о наличии, но и о локализации и протяженности воспаления в миокарде.
Биопсия миокарда. Согласно современным представлениям, одним из наиболее информативных лабораторных методов в диагностике миокардита является эндомиокардиальная биопсия с последующей световой микроскопией в сочетании с иммуногистологическим исследованием биоптата и применением молекулярно-биологических технологий: ПЦР или гибридизации in-situ. Результаты ПЦР позволяют идентифицировать вирусный геном в эндомиокардиальных биоптатах, что важно для дифференциального диагноза вирусного и аутоиммунного миокардита. При оценке результатов биопсии, как правило, используются Далласские (1987) критерии. При первичной биопсии можно диагностировать острый миокардит, который рассматривается как активный, хронический — как пограничный или заживающий, а также отсутствие миокардита.
Для гистологического подтверждения диагноза «миокардит» (определенный миокардит) необходимым и достаточным считается обнаружение в биоптате двух морфологических признаков: воспалительного клеточного инфильтрата и некроза или повреждения кардиомиоцитов. Если в биоптате выявляется воспалительная инфильтрация, но отсутствуют признаки повреждения кардиомиоцитов, диагноз сомнителен (хотя и вполне вероятен). Наконец, отсутствие воспалительных инфильтратов в гистологическом препарате является основанием для отрицательного диагностического заключения.
Таким образом, главным морфологическим признаком миокардита является обнаружение в биоптате воспалительного клеточного инфильтрата (рис. 4, 5). Считается, что при вирусных миокардитах в инфильтрате преобладают лимфоциты, а при бактериальном — нейтрофилы. Аллергические миокардиты сопровождаются инфильтрацией эозинофилами. Гигантоклеточная инфильтрация характерна для миокардита, отличающегося крайне тяжелым течением, быстрым прогрессированием и неизбежным возникновением летального исхода.
13
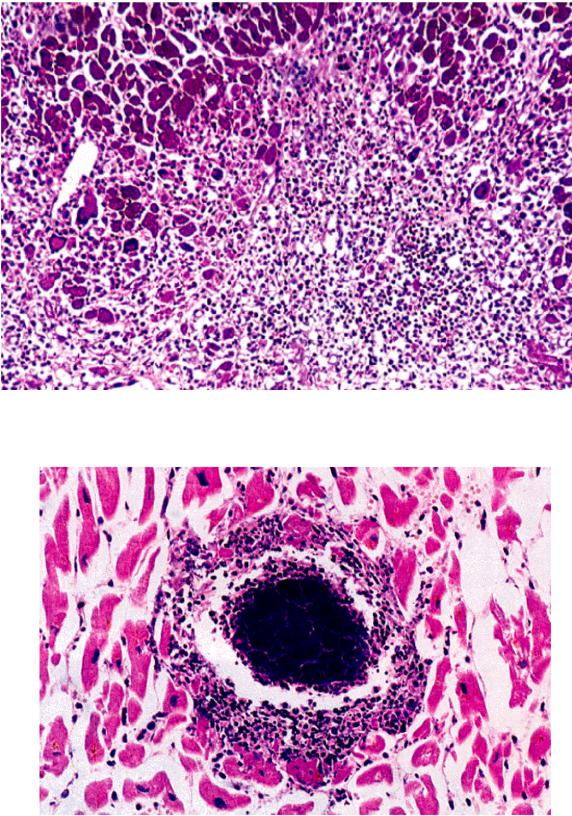
Рис. 4. Микроскопия эндомиокардиального биоптата, полученного у больного острым вирусным миокардитом (по R. H. Anderson, A. E. Becker, 1998) (обильная очаговая инфильтрация некротизированного участка миокарда моноцитами и лимфоцитами)
Рис. 5. Микроскопия эндомиокардиального биоптата, полученного у больного бактериальным миокардитом, развившимся у пациента с инфекционным эндокардитом (по R. H. Anderson, A. E. Becker, 1998) (формирование микроабсцесса, обильная очаговая инфильтрация миокарда нейтрофилами и стафилококками)
14
Эндомиокардиальная биопсия также не дает полной гарантии постановки диагноза. С одной стороны, при очаговом процессе высока вероятность забора неизмененного участка миокарда и получения ложноотрицательного результата. С другой стороны, немало сложностей существует в интерпретации данных, и полученный ложноположительный результат может быть обусловлен, например, трудностями при дифференцировке лимфоцитов (в норме в небольшом количестве присутствующих в миокарде) с другими клетками. Кроме того, миокардиальный некроз, характерный для активного миокардита, можно определить только в первые 7–10 дней от начала заболевания.
На основании информации, полученной с помощью эндомиокардиальной биопсии в зависимости от патогенетического механизма можно выделить следующие типы миокардита, а также воспалительной кардиомиопатии:
 вирусный миокардит (наличие вируса и воспаления при отсутствии аутоантител к миокарду);
вирусный миокардит (наличие вируса и воспаления при отсутствии аутоантител к миокарду);
 вирусный и аутоиммунный миокардит (наличие вируса и воспаления, а также аутоантител к миокарду);
вирусный и аутоиммунный миокардит (наличие вируса и воспаления, а также аутоантител к миокарду);
 аутоиммунный миокардит (наличие воспаления и аутоантител к миокарду при отсутствии вируса);
аутоиммунный миокардит (наличие воспаления и аутоантител к миокарду при отсутствии вируса);
 воспалительная кардиомиопатия (наличие воспаления при отсутствии вируса и аутоантител к миокарду);
воспалительная кардиомиопатия (наличие воспаления при отсутствии вируса и аутоантител к миокарду);
 идиопатическая кардиомиопатия (отсутствие вируса, воспаления и аутоантител к миокарду);
идиопатическая кардиомиопатия (отсутствие вируса, воспаления и аутоантител к миокарду);
 персистенция вируса в миокарде (наличие вируса при отсутствии воспаления и аутоантител к миокарду).
персистенция вируса в миокарде (наличие вируса при отсутствии воспаления и аутоантител к миокарду).
В соответствии с рекомендациями Европейского общества кардиологов, Американской ассоциации сердца и Американского колледжа кардиологов эндомиокардиальная биопсия в настоящее время показана пациентам с сердечной недостаточностью в следующих ситуациях:
 необъяснимая вновь возникшая сердечная недостаточность в течение более 2 недель при нормальном или дилатированном левом желудочке с нарушениями гемодинамики;
необъяснимая вновь возникшая сердечная недостаточность в течение более 2 недель при нормальном или дилатированном левом желудочке с нарушениями гемодинамики;
 необъяснимая вновь возникшая сердечная недостаточность в течение от 2 недель до 3 месяцев при дилатированном левом желудочке и с вновь возникшими желудочковыми аритмиями, атривентрикулярной блокадой типа Мобитц II 2–3 степени или недостаточной эффективностью обычной терапии в течение 1–2 недель;
необъяснимая вновь возникшая сердечная недостаточность в течение от 2 недель до 3 месяцев при дилатированном левом желудочке и с вновь возникшими желудочковыми аритмиями, атривентрикулярной блокадой типа Мобитц II 2–3 степени или недостаточной эффективностью обычной терапии в течение 1–2 недель;
 необъяснимая сердечная недостаточность, связанная с дилатационной кардиомиопатией любой продолжительности, которая ассоциируется с подозрением на аллергическую реакцию с эозинофилией;
необъяснимая сердечная недостаточность, связанная с дилатационной кардиомиопатией любой продолжительности, которая ассоциируется с подозрением на аллергическую реакцию с эозинофилией;
15

 исключительные случаи при необъяснимой желудочковой аритмии.
исключительные случаи при необъяснимой желудочковой аритмии.
Клинические диагностические критерии острого диффузного миокардита (рекомендации NYHA). Диагноз может основываться на рекомендациях NYHA. Для диагностики острого диффузного миокардита используют 2 группы диагностических критериев «больших» и «малых» симптомов.
«Большие» критерии:
1. Имеется хронологическая связь перенесенной инфекции (или аллергической реакции, или токсического воздействия) с появлением следующих кардиальных симптомов:
кардиомегалия; сердечная недостаточность; кардиогенный шок;
синдром Морганьи–Адамса–Стокса (МАС).
2.Патологические изменения ЭКГ, в том числе сердечные аритмии
инарушения проводимости. Повышение активности кардиоспецефиче-
ских ферментов (КФК, МВ-КФК, ЛДГ, ЛДГ1) и содержание тропонинов. «Малые» критерии:
1.Лабораторное подтверждение перенесенной инфекции (например, высокие титры противовирусных антител).
2.Ослабление I тона.
3.Протодиастолический ритм галопа.
Диагноз «миокардита» ставится на основании наличия хронологической связи признаков перенесенной инфекции (аллергия, токсическое воздействие) с двумя «большими» критериями миокардита или с одним «большим» и двумя «малыми».
Примеры формулировки диагноза. Вирусный (Коксаки) миокар-
дит, острое течение, среднетяжелая форма, частая суправентрикулярная экстрасистолия с эпизодами парной. ХСН, II функциональный класс. Дифтерийный миокардит, острое течение, тяжелая форма, полная атриовентрикулярная блокада с синдромом МАС, имплантирован электрокардиостимулятор (2008), ХСН, III функциональный класс.
ЛЕЧЕНИЕ
Всех больных с подозрением на поражение миокарда следует помещать в стационар и следить, насколько эффективно проводимое лечение.
Терапия миокардита направлена на поддержание насосной функции сердца и снижение риска прогрессирования сердечной недостаточности, борьбу с аритмией, а также на выявление и ликвидацию источников токсичности. В острой стадии миокардита необходимо максимальное ограничение физической нагрузки. Эксперименты на животных показали,
16
что физическая нагрузка во время острого миокардита вредна. Есть данные о том, что физические нагрузки провоцируют увеличение вирусной репликации в миокарде. В период выздоровления больным рекомендуют ограничить занятия спортом. Это важно, учитывая, что многие пациенты, страдающие данным заболеванием, молодые люди.
Пища должна быть полноценной, содержать, прежде всего, белки, витамины, микроэлементы, необходимые для анаболических процессов в миокарде.
Стратегия и длительность этиотропной терапии зависит от конкретного возбудителя и индивидуального течения заболевания у пациента. При бактериальных инфекциях назначают антибиотики после определения чувствительности микробного агента на различные препараты. При необходимости курс антибактериальной терапии следует повторить с использованием препаратов второго ряда. Для лечения вирусных инфекций, осложнившихся миокардитом, показаны противовирусные препараты. Обязательным считается поиск и санация очагов хронической инфекции (тонзиллит, отит, гайморит, аднексит, простатит и др.). После проведения терапевтической или хирургической санации, антибактериальной и противовирусной терапии необходимо провести микробиологический контроль. Без проведения этиологической терапии и санации гнойных очагов трудно рассчитывать на выздоровление, т. к. инфекционные агенты являются пусковым механизмом и поддерживающим фактором миокардита. В настоящее время изучается возможность использования новых противовирусных и иммуномодулирующих препаратов: рекомбинантного интерферона, поликлонального иммуноглобулина, рибаверина, виферона, гепона, полиоксидония.
Энтеровирусы (вирусы Коксаки A и B, ECHO-вирусы, вирус полиомиелита). Специфическое лечение не разработано. Показана симптоматическая терапия. ГКС не рекомендованы. Выздоровление обычно наступает в течение нескольких недель, однако, нарушения по данным ЭКГ и ЭхоКГ могут сохраняться в течение нескольких месяцев.
Вирус эпидемического паротита, кори, краснухи. Рекомендована патогенетическая и симптоматическая терапия.
Вирусы гриппа. Наибольшая эффективность противовирусных препаратов отмечается в первые 48–72 часа после начала заболевания, однако, при тяжелом и осложненном течении гриппа их назначение целесообразно в любой срок от момента заболевания. Рекомендовано 75 мг озельтамивира внутрь 2 раза в сутки в течение 7 дней с момента появления симптомов. Лечение следует начинать не позднее 48 часов от начала заболевания.
Вирус varicella zoster (ветряная оспа, опоясывающий лишай), ви-
рус простого герпеса, вирус Эпштейна–Барр, цитомегаловирус. Реко-
17
мендованы 500 мг валацикловира 2 раза в день внутрь; внутривенная инфузия 5 мг/кг ганцикловира каждые 12 часов. При миокардите, вызванном вирусом varicella zoster и вирусом простого герпеса, назначают валацикловир, при цитомегаловирусной инфекции — ганцикловир.
ВИЧ-инфекция. Рекомендована комплексная антиретровирусная терапия (назначается инфекционистом) и лечение оппортунистических инфекций (в соответствии с протоколом).
Mycoplasma pneumoniae. Проявления многообразны и включают лихорадку, пневмонию, сыпь. Часто миокардиту сопутствует перикардит. Рекомендовано назначение антибактериальных препаратов, в частности макролидов.
Borrelia burgdorferi (болезнь Лайма). Переносчики инфекции — иксодовые клещи. Заболевание начинается с сыпи. Через несколько недель или месяцев появляются неврологические симптомы (менингоэнцефалит, двустороннее поражение лицевого нерва, радикулит), артриты, поражение сердца (миокардит с тяжелыми нарушениями проводимости, вплоть до полной атриовентрикулярной блокады). Рекомендовано назначение антибактериальных препаратов, в частности по 1 г цефтриаксона внутривенно 2 раза в сутки.
Corynebacterium diphtheriae. Поражение сердца отмечается в 50 %
случаев. Оно обычно возникает в конце первой недели и является самой частой причиной смерти от дифтерии. Рекомендована антибиотикотерапия с экстренным введением противодифтерийной сыворотки.
Cryptococcus neoformans. Рекомендовано: внутривенная инфузия 0,3 мг/кг/сут амфотерицина B + 100–150 мг/кг/сут фторцитозина внутрь в 4 приема.
Trypanosoma cruzi (болезнь Чагаса). Основная причина дилатационной кардиомиопатии в Центральной и Южной Африке. Это острая инфекция, вызываемая укусами летающих клопов. Обычно проявляется лихорадкой, миалгией, гепатомегалией и спленомегалией, миокардитом. В зависимости от места укуса возможен односторонний периорбитальный отек (симптом Романьи) или поражение кожи (чагома). Спустя несколько лет после заражения может развиться дилатационная кардиомиопатия, которая, в частности, проявляется двухпучковой блокадой, предсердными и желудочковыми нарушениями ритма и тромбоэмболиями. Эффективного специфического лечения нет. Наиболее перспективными считаются производные нитрофурана (нифуртимокс) внутрь по 8–12 мг/кг/сут в 3 приема и имидазола (бензонидазол) по 5–8 мг/кг/сут.
Trichinella spiralis (трихинеллез). Признаки миокардита (одышка, сердцебиение, боль в груди) появляются через 3–4 недели после миопатии и эозинофилии. В тяжелых случаях рекомендованы ГКС. Эффектив-
18

ность мебендазола и тиабендазола не доказана. В последние годы препаратом выбора считают 400 мг албендазола 2 раза в сутки.
Toxoplasma gondii. Чаще наблюдается при иммунодефицитных состояниях, особенно у ВИЧ-инфицированных. Рекомендовано: пириметамин в начальной дозе 100 мг/сут внутрь, затем 25–50 мг/сут + 1–2 г сульфадиазина внутрь 3 раза в сутки 4–6 недель + 10 мг/сут кислоты фолината кальция внутрь для профилактики угнетения кроветворения. У беременных (не ранее 12 недели гестации) рекомендуется назначение спиромицина в разовой дозе 1,5–3 млн МЕ каждые 8 часов на протяжении 7 дней.
При лечении миокардита применяют различные группы лекарственных препаратов, обладающих противовоспалительными, десенсибилизирующими свойствами. Считают, что их назначение способствует уменьшению проницаемости сосудистой стенки, стабилизации лизосомальных мембран, снижению титров противокардиальных антител, подавлению возможных аллергических реакций замедленного типа. С этой целью чаще используют:
 препараты аминохинолинового ряда (делагил, резохин, хлорохин). Их назначают в суточной дозе 0,25–0,5 г. Возможно применение 0,4 г/сут плаквинила. Эти препараты используют для лечения миокардита в течение 6–9 мес., а при рецидивирующем течении — до 1 года;
препараты аминохинолинового ряда (делагил, резохин, хлорохин). Их назначают в суточной дозе 0,25–0,5 г. Возможно применение 0,4 г/сут плаквинила. Эти препараты используют для лечения миокардита в течение 6–9 мес., а при рецидивирующем течении — до 1 года;
 ацетилсалициловую кислоту, которую назначают в дозе до 3 г/ сут в течение 4–5 недель;
ацетилсалициловую кислоту, которую назначают в дозе до 3 г/ сут в течение 4–5 недель;
 индометацин, который применяют в дозе 75–100 мг/сут в течение 4–6 недель, иногда в сочетании с хинолиновыми производными;
индометацин, который применяют в дозе 75–100 мг/сут в течение 4–6 недель, иногда в сочетании с хинолиновыми производными;
мовалис, диклофенак; пиразолоновые производные (бутадион, бруфен, ибупрофен). Их
применяют для лечения миокардитов, но они все же обладают малой эффективностью.
Хотя перечисленные нестероидные противовоспалительные препараты оказывают определенное влияние на клинические проявления заболевания (болевой синдром, лихорадка, динамика клинико-лабораторных показателей), убедительных доказательств их благоприятного действия на исходы миокардита до сих пор не получено.
В течение последних 10–15 лет для лечения миокардитов достаточно широко используются иммуносупрессоры. Применение ГКС в терапии основывается на следующих свойствах препаратов:
1)они тормозят клеточный и гуморальный иммунитет, синтез антител и образование иммунных комплексов;
2)обладают прямым противовоспалительным действием, стабилизируя клеточные мембраны, уменьшая проницаемость стенок капилляров
итормозя активность протеолитических ферментов;
19

3) замедляют пролиферацию клеток соединительной ткани и развитие фиброза.
Хотя применение этих препаратов при иммунном воспалении сердечной мышцы теоретически вполне обосновано, многие исследователи весьма негативно оценивают перспективу их использования при острых миокардитах. Так, в клиническое исследование «The Myocarditis Treatment Trial» включали пациентов только с подтвержденным по данным биопсии диагнозом «миокардит» и «хроническая сердечная недостаточность II–IV функционального класса». Все пациенты получали стандартную терапию дигоксином, диуретиками, эналаприлом. Пациенты основной группы в течение 24 недель дополнительно получали преднизолон в сочетании с азатиоприном или циклоспорином. Исследование показало, что стандартная терапия иммуносупрессантами положительно влияет на сократительную функцию левого желудочка, однако, не улучшает прогноз заболевания.
Эти и другие данные современных экспериментальных и клинических исследований свидетельствуют о том, что назначение ГКС, так же как и других иммуносупрессантов, пациентам с миокардитом должно быть избирательным и строго дифференцированным. При вирусном миокардите иммуносупрессия, наоборот, увеличивает репликацию вирусов в миокарде, усугубляя повреждение в сердечной мышце. Глюкокортикостероидные гормоны целесообразно использовать при хронических и рецидивирующих формах миокардита, в патогенезе которых большее значение приобретают аутоиммунные механизмы:
 при тяжелых миокардитах, протекающих с выраженным аллергическим компонентом или иммунными нарушениями;
при тяжелых миокардитах, протекающих с выраженным аллергическим компонентом или иммунными нарушениями;
миокардитах затяжного и рецидивирующего течения; миокардитах, сопровождающихся перикардитом (миоперикар-
диты);
 миокардитах, протекающих с выраженным болевым синдромом. Целесообразно назначение ГКС при тяжелом гигантоклеточном миокардите, а также у больных СПИДом. В этих случаях преднизолон назначают обычно в дозе 0,4–0,75 мг/кг массы тела в сутки. Длительность приема составляет 1,5–2 месяца с постепенным снижением дозы и отме-
миокардитах, протекающих с выраженным болевым синдромом. Целесообразно назначение ГКС при тяжелом гигантоклеточном миокардите, а также у больных СПИДом. В этих случаях преднизолон назначают обычно в дозе 0,4–0,75 мг/кг массы тела в сутки. Длительность приема составляет 1,5–2 месяца с постепенным снижением дозы и отме-
ной препарата.
Симптоматическая терапия направлена на устранение нарушений сердечного ритма, признаков сердечной недостаточности, гипертензии, предупреждение тромбоэмболических осложнений. Медикаментозное лечение сердечной недостаточности проводится согласно общим принципам лечения этого патологического синдрома. В комплекс терапии ХСН обычно включают: ингибиторы АПФ, β-адреноблокаторы, диуретики и сердечные гликозиды. Сердечные гликозиды при миокардите с при-
20
