
- •Розрахунковий варіант
- •Робоче завдання
- •Робоче тіло – ідеальний газ.
- •Маса ідеального газу.
- •Визначення параметрів стану в початковій точці циклу
- •Визначимо основні параметри станів по графікам процесів
- •Визначимо параметри стану в точці 2
- •Визначимо параметри стану в точці 3
- •Визначимо параметри стану в точці 4
- •Визначимо параметри стану в точці 5
- •Зображення циклу ідеального газу pv- I Ts- діаграмах
- •Розрахунок процесів, що входять до циклу
- •Процес 1-2
- •Процес 2-3
- •Процес 3-4
- •Процес 4-5
- •Процес 5-1
- •Розрахунок циклу за іі законом термодинаміки
- •Маса водяної пари
- •Параметри стану водяної пари у початковій точці 1
- •Параметри водяної пари в точці 2
- •Параметри водяної пари в точці 3
- •Параметри водяної пари в точці 4
- •Параметри водяної пари в точці 5
- •Розрахунок процесів водяної пари
- •Процес 1-2
- •Процес 2-3
- •Процес 3-4
- •Процес 4-5
- •Процес 5-1
- •Аналіз циклу водяної пари за іі законом термодинаміки
- •Ексергетична оцінка
-
Процес 2-3
Розглянемо процес ізотермічного розширення 2-3. Для ідеального газу внутрішня енергія і ентальпія залежать тільки від температури, тобто зміна цих функцій в ізотермічному процесі дорівнює нулю (∆U2-3=∆H2-3=0). Зміну ентропії та ексергії ідеального газу знайдемо за формулами:
∆S2-3 = m·(S3-S2) = 11,5·(0,8159 + 0,027) = 9,687 кДж/K
∆E2-3 = m·(e3-e2) = 11,5·(132,71 – 384,227) = -2909,26кДж
Розрахуємо кількість теплоти у ізотермічному процесі розширення 2-3:
Q2-3= кДж
кДж
Знак «+», що стоїть перед числовим значенням кількості теплоти, вказує на те, що у процесі теплота підводиться.
Обчислимо роботу процесу L.
Для визначення роботи використовуємо
загальну формулу L=
 та рівняння ізотермічного процесу, яке
зв’язує абсолютний тиск і питомий об’єм
p1v1=p2v2=pv=const.
Розв’язавши цей інтеграл з урахуванням
залежності p=φ(v),
отримаємо
та рівняння ізотермічного процесу, яке
зв’язує абсолютний тиск і питомий об’єм
p1v1=p2v2=pv=const.
Розв’язавши цей інтеграл з урахуванням
залежності p=φ(v),
отримаємо
L2-3=p2V2·ln кДж
кДж
Розрахована робота так само як і теплота – величина додатня і вказує на те, що ідеальний газ у процесі 2-3 розширюється.
Після того, як знайдена теплота і робота, обчислимо наявну роботу. Аналізуючи вираз Q = ∆H + Lн та маючи на увазі, що у ізотермічному процесі ідеального газу зміна ентальпію, дорівнює нулю, приходимо до висновку:
при Т=const ⇒ Q=L=Lн;
Lн2-3 = L2-3 = 6934,78 кДж
Теж саме отримаємо, якщо
будемо розв’язувати інтеграл Lн= ,
враховуючи залежність v=f(p)
ізотермічного процесу. Таким чином ми
знайшли всі характеристики
,
враховуючи залежність v=f(p)
ізотермічного процесу. Таким чином ми
знайшли всі характеристики
процесу: теплоту, роботу і наявну роботу. Зобразимо процес ізотермічного розміщення у pv- i Ts- діаграмах і виділимо площини які еквівалентні питомим теплоті(q), роботі(l) та наявній роботі (lн).


Зведемо енергетичний баланс процесу згідно І закону термодинаміки, та виявимо похибку балансу. Оскільки ∆U2-3=0, то Q2-3=L2-3. За розрахунками маємо:
Q2-3=6931,52 кДж, L2-3=6934,78 кД ж
Отже розбіжність балансу у відсотках становить:
δ%
Складемо схему енергобалансу процесу 2-3 та розкриємо його суть.

Отримані результати запишемо в таблицю 2.
-
Процес 3-4
Процес 3-4 - ізохорний процес зниження тиску. Обчислимо змінення параметрів стану цього процесу:
∆U3-4 = m·(u4 – u3) = 11,5·(549,43 – 473,89) = 870,23 кДж
∆H3-4 = m·(h4 – h3) = 11,5·(706,06- 608,98) = 1116,9 кДж
∆S3-4 = m·(S4-S3) = 11,5·(0,914 – 0,8159) = 1,1286 кДж/K
∆E3-4 = m·(e4-e3) = 11,5·(200,36 – 132,71) = 778,313кДж
Оскільки у ізохорному процесі об’єм сталий, то робота зміни об’єму рівна нулю.
L=
 =
0, v3 = v4
, dv = 0.
=
0, v3 = v4
, dv = 0.
 Наявну
роботу процесу 3-4 знайдемо
за формулою:
Наявну
роботу процесу 3-4 знайдемо
за формулою:
Lн
=
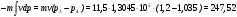 кДж
кДж
Теплоту процесу розрахуємо як добуток маси ідеального газу на ізохорну теплоємність та різницю температур у кінці та початку процесу:
Q3-4= кДж
кДж
Зобразимо процес 3-4 у pv- i Ts- діаграмах.

Всі розрахункові дані для процесу 3-4 зведемо у табл.2.
Запишемо І закон термодинаміки Q = ∆H + Lн та визначимо його відносну похибку.
δ%=
Побудуємо схему енергобалансу та з’ясуємо його суть:

