
- •Аудиторные занятия
- •Классификация и номенклатура органических соединений
- •Структура и реакционная способность углеводородов
- •Лабораторная работа №1 «Реакционная способность углеводородов, обнаружение и идентификация» Форма отчета по лабораторной работе:
- •Техника лабораторных работ.
- •Правила по технике безопасности при работе в химической лаборатории.
- •Меры первой помощи.
- •Лабораторно-практическая работа №2 «Гетероциклические соединения, алкалоиды, флавоноиды»
- •Лабораторная №2 «Реакционная способность гетероциклических соединений. Реакции обнаружения алкалоидов и флавоноидов»
Лабораторная №2 «Реакционная способность гетероциклических соединений. Реакции обнаружения алкалоидов и флавоноидов»
ОПЫТ №1. Качественный анализ витамина РР (никотинамид)
Витамин РР широко распространен в растительных продуктах (рисовые и пшеничные отруби), много витамина в печени и почках животных.
Методика эксперимента. В две пробирки прилить по 2 мл 1% раствора никотиновой кислоты, затем добавить в одну - 1 мл 10% раствора сульфата меди, в другую - 0,5 мл 10% раствора сульфата меди и 2 мл 1% раствора роданида аммония. В первом случае образуется осадок синего цвета, в другом - раствор зеленого цвета.
Наблюдения:
Выводы:
ОПЫТ №2. Качественный анализ барбитуратов
Реакции обнаружения основаны на образовании различно окрашенных солей, в первом случае раствор окрашивается в розовый цвет, в другом - выпадает осадок голубого цвета.
а) В пробирку прилить 0,5 мл 1 % спиртового раствора барбитала, затем прибавить по 2 к. 10 % водных растворов хлорида кальция и нитрата кобальта. Наблюдать изменения .
б) В пробирку прилить 0,5 мл 1 % спиртового раствора этаминала натрия, затем прибавить по 0,2 мл 10% растворов гидрокарбоната и карбоната калия, 0,1 мл 10% раствора сульфата меди. Наблюдать изменения.
Наблюдения: Выводы:
ОПЫТ №3. Качественный анализ производных пурина (мурексидная проба)
Производные пурина - ксантин, теобромин, теофиллин, кофеин, мочевая кислота при окислении азотной кислотой дают окрашенную смесь продуктов окисления и гидратации, одним из которых является пурпуровая кислота.
Методика эксперимента. В фарфоровую чашку поместить 1-2 кристаллика кофеина и прилить 0,5 мл конц. азотной кислоты. Выпарить раствор досуха, сухой остаток приобретает при этом желто- коричневый цвет. Дают чашке остыть и смачивают при помощи стеклянной палочки сухой остаток с одного края каплей конц. раствора аммиака, а с другого - каплей разбавленного раствора гидроксида калия. Наблюдают изменения окраски.
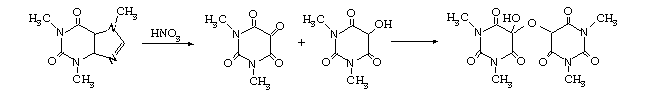
Кофеин Диметилаллоксан Диметилдиа- Тетраметилаллоксантин
луровая кислота
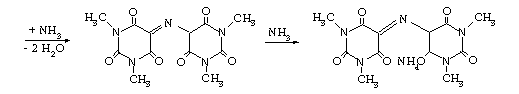
Пурпуровая кислота Аммонийная соль
пурпуровой кислоты
При добавлении к сухому остатку раствора аммиака образуется ярко - красное (пурпурное) окрашивание, обусловленное образованием мурексида - аммонийной соли пурпуровой кислоты, а если прибавить раствор гидроксида калия - образуется калиевая соль пурпуровой кислоты сине - фиолетового цвета.
Наблюдения: Выводы:
ОПЫТ №4. Обнаружение флавонолов, флавононов, флавонов (проба Шинода)
Флавонолы, флавононы и флавоны при восстановлении магнием в присутствии соляной кислоты дают красное или оранжево-красное окрашивание, обусловленное образованием антоцианидинов.
Методика эксперимента. В пробирку приливают 2 мл раствора флавоноидов добавляют 5-7 к. соляной кислоты и небольшое количество магния (~0,3см по высоте пробирки) в виде опилок, затем нагреть, через 3-5 минут наблюдают окрашивание.
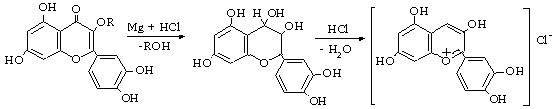
Наблюдения: Выводы:
ОПЫТ №5. Реакция обнаружения окисленных групп флавоноидов
а) Взаимодействие с ацетатом свинца
Флавоноиды различаются по степени окисленности или насыщенности гетероциклического фрагмента, числа и взаимным положением гидроксильных групп. Флавоноиды при взаимодействии с ацетатом свинца образуют осадки, окрашенные в желто-оранжевый, красный или синий цвет.
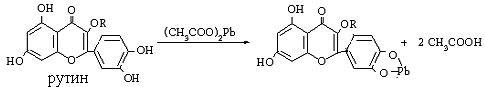
Методика эксперимента. В пробирку приливают 1 мл раствора флавоноидов (настой зеленого чая или лука, рутин, кверцетин и др.), добавляют 3-5 капель 2% раствора ацетата свинца. Наблюдают выпадение осадка.
Наблюдения: Выводы:
б) Взаимодействие с аммиаком
С раствором аммиака идет реакция конденсации по оксогруппе кольца гетероцикла, с образованием окрашенных продуктов. Флавоны, флавононы и флавонолы дают желтое окрашивание, при нагревании переходящее в оранжевое или красное, антоцианы - дают синее или фиолетовое окрашивание. Чистые катехины окрашивания не дают.
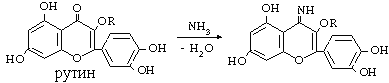
Методика эксперимента. В пробирку приливают 1 мл раствора флавоноидов (настой зеленого чая или лука, рутин, кверцетин и др.), добавляют 3-5 капель концентрированного раствора аммиака. Наблюдают изменение окраски раствора.
Наблюдения: Выводы:
ОПЫТ №6. Обнаружение катехинов
Катехины содержатся в листьях зеленого чая, какао-бобах, яблоках, черном винограде, зернах ячменя. В технологическом процессе получения черного чая происходит ферментативное окисление катехинов, сопровождающееся процессами межмолекулярной конденсации (образование теафлавинов, определяющих желто-оранжевую окраску раствора).
Характерной реакцией на катехины является черно - зеленое окрашивание по реакции с раствором хлорида железа, красно - малиновое - с раствором ванилина в соляной кислоте.

Методика эксперимента. В две пробирки приливают по 1 мл водного раствора катехинов (настой зеленого чая), затем в одну пробирку добавляют 3-5 капель 1% раствора хлорида железа, в другую - 3-5 капель свежеприготовленного 1% раствора ванилина в концентрированной соляной кислоте.
Наблюдения: Выводы:
ОПЫТ №7. Обнаружение алкалоидов
Общие алкалоидные реакции осаждения основаны на свойстве алкалоидов, как оснований образовывать даже в разбавленных растворах простые или комплексные соли с кислотами, солями тяжелых металлов. При этом образуются осадки различного цвета: белого, желтого, оранжевого, бурого.
Методика эксперимента. В несколько пробирок прилить по 1 мл раствора алкалоида (хинина, кофеина и др.) и добавить по 1-2 капли реактивов:
а) реактив Бушарда (йод в растворе иодида калия) - осадки бурого цвета;
б) реактив Зонненштейна (1% раствор фосфорно-молибденовой кислоты) - осадки желтого цвета, переходящие в осадки синего или зеленого цвета;
в) 1 % водный раствор пикриновой кислоты - осадки желтого цвета;
г) 5 % водный раствор танина (или настой черного чая) - осадки желтого цвета.
Наблюдения: Выводы:
Контрольные вопросы
Какие структурные компоненты определяют кислотные и основные свойства никотиновой кислоты?
Каких реакционные центры в молекулах алкалоидов обуславливают протекание общих реакций осаждения?
Напишите структуру флавоноидов (на примере кверцетина) в кислой и щелочной среде, укажите аналитический эффект реакций.
