
- •Аудиторные занятия
- •Классификация и номенклатура органических соединений
- •Структура и реакционная способность углеводородов
- •Лабораторная работа №1 «Реакционная способность углеводородов, обнаружение и идентификация» Форма отчета по лабораторной работе:
- •Техника лабораторных работ.
- •Правила по технике безопасности при работе в химической лаборатории.
- •Меры первой помощи.
- •Лабораторно-практическая работа №2 «Гетероциклические соединения, алкалоиды, флавоноиды»
- •Лабораторная №2 «Реакционная способность гетероциклических соединений. Реакции обнаружения алкалоидов и флавоноидов»
Правила по технике безопасности при работе в химической лаборатории.
При всех работах соблюдать осторожность, помня, что неаккуратность и невнимательность, недостаточное знакомство со свойствами веществ, с которыми ведется работа, могут повлечь за собой несчастный случай.
При работе с металлическим натрием не бросать обрезки в раковины, склянки для сливов, а убирать в специальные склянки, в которых он хранится под слоем обезвоженного керосина.
Помещать кусочки натрия в совершенно сухие пробирки, избегать проводить реакции с металлическим натрием на кипящей водяной бане.
Нагревать жидкость в пробирке следует постепенно, направляя отверстие пробирки в сторону от себя и работающих товарищей.
Не наклоняться над пробиркой, в которой кипит жидкость.
Нюхать какие бы то ни было вещества, направляя к себе пары или газ движением руки.
Никаких веществ в лаборатории не пробовать на вкус.
Все опыты проводить в вытяжном шкафу.
Различные кислоты и щелочи засыпать песком, нейтрализовать и после этого убирать.
При работе с газоотводной трубкой убирать спиртовку из-под пробирки с реакционной смесью можно лишь тогда, когда конец газоотводной трубки, опущенный в жидкость, удален из нее. Если убрать спиртовку преждевременно, то жидкость засосет в реакционную пробирку и может произойти разбрызгивание реакционной смеси на лицо и руки.
Меры первой помощи.
При термических ожогах пораненное место нужно смочить раствором танина в спирте или 2%-м раствором марганцевокислого калия.
При химических ожогах необходимо, прежде всего, удалить с кожи вещества вызвавшие ожоги, а затем обработать соответствующим образом:
При ожогах кислотами или щелочами промывают обожженное место сильной струей воды, а затем нейтрализуют кислоту 1%-м раствором бикарбоната натрия, а щелочь - 1%-м раствором уксусной кислоты.
При ожоге бромом, пораженное место обрабатывают 10-20%-м раствором тиосульфата натрия, смывают его большим количеством воды.
При ожоге жидким фенолом побелевший участок кожи растирают глицерином, пока не восстановится нормальный цвет, обмывают водой с мылом.
ОПЫТ №1. Получение этилена и изучение его свойств
Этилен получают по реакции дегидратации этилового спирта при нагревании с концентрированной серной кислотой (1). Этилен относится к ненасыщенным соединениям (алкенам), содержащим в молекуле двойную углерод-углеродную связь. Алкены вступает в реакции присоединения, при которых происходит разрыв менее прочной π-связи и образование двух новых σ-связей (2). В отличие от алканов, алкены легко окисляются многими окислителями (3).
![]()
![]()
этилен 1,2 - дибромэтан
![]()
этандиол - 1,2
![]()
Методика эксперимента. В пробирку поместить 1мл этилового спирта, 2мл концентрированной серной кислоты и несколько крупинок песка. Закрыть пробирку пробкой с газоотводной трубкой, закрепить в лапке штатива Бунзена и осторожно нагреть смесь в пламени спиртовки. Конец газоотводной трубки опустить в предварительно приготовленные пробирки с бромной водой (~2мл), затем смеси 2% раствора перманганата калия (~2мл). Отметив наблюдения, поджечь газ у конца газоотводной трубки.
Наблюдения:
Выводы:
ОПЫТ №2. Нитрование бензола и его гомологов
Продукты нитрования бензола и его гомологов являются тяжелыми маслянистыми жидкостями с запахом горького миндаля.
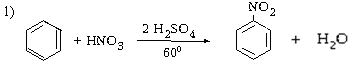
бензол нитробензол
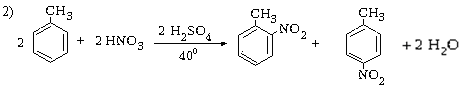
толуол о-нитротолуол п-нитротолуол
Методика эксперимента. В две сухие пробирки поместить по 2 капели концентрированной азотной кислоты и по 4 капли концентрированной серной кислоты, смесь перемешать и охладить в стакане с водой до комнатной температуры. Затем, при постоянном перемешивании, добавить в одну пробирку 3 капли бензола, в другую - 3 капли толуола. Через 5 минут содержимое пробирок вылить в стаканы с водой. Отметить изменения в реакционной смеси по ходу реакции и запах содержимого стаканов.
Наблюдения: Выводы:
ОПЫТ №3. Окисление бензола и его гомологов
Бензол устойчив к действию таких окислителей как перманганат калия, хромовая смесь. Его окисление происходит под действием кислорода в присутствии катализатора (V2O5), а также при действии озона. Гомологи бензола окисляются значительно легче, за счет активности боковой цепи.
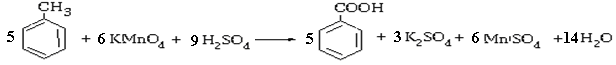
толуол бензойная кислота
Методика эксперимента. В две пробирки поместить по 3 капли воды, 1 капли 10% раствора перманганата калия и 1 капли 10% раствора серной кислоты. Затем в одну из пробирок добавить 2 капли бензола, в другую – 2 капли толуола, содержимое перемешать в течение 1-2 минут. Наблюдать изменение окраски смесей.
Наблюдения: Выводы:
УИРС: Обнаружение ненасыщенных систем в
биологически активных соединениях
ОПЫТ №4. Определение наличия двойных связей в маслах, жирах
Реакция окисления алкенов раствором перманганата калия с образованием гликолей используется для обнаружения двойной связи в сложных биологически активных соединениях, при этом происходит обесцвечивание раствора.
Методика эксперимента. В отдельные пробирки прилить по 5 капель жидких масел (подсолнечное, оливковое, льняное и др.), внести сливочное масло и вазелиновое масло (размером с рисовое зерно), затем в каждую пробирку добавить по 5 капель этилового спирта, энергично встряхивать в течение 1-2 мин, до образования однородной эмульсии. Прилить по 2-3 капли 2% водного раствора перманганата калия. Энергично встряхнуть. Отметить изменения.
Наблюдения: Выводы:
ОПЫТ №5. Обнаружение двойных связей в терпенах и эфирных маслах
Терпены и эфирные масла содержат в молекуле одну или несколько двойных связей, которые легко окисляются раствором перманганата калия.
-
лимонен
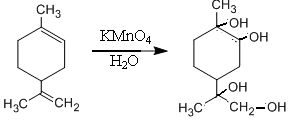
Методика эксперимента. В пробирку поместить 1 каплю 2% раствора перманганата калия и 5 капель воды, к полученному раствору добавить 5 капель исследуемого вещества (скипидар, лимонное масло, укропное масло и др.). Энергично встряхнуть, наблюдать изменение окраски.
Наблюдения: Выводы:
ОПЫТ №6. Обнаружение гидропероксидов в маслах
Растительные и эфирные масла при хранение на воздухе легко окисляются с образованием -гидропероксидов, которые можно обнаружить по реакции с иодидом калия.
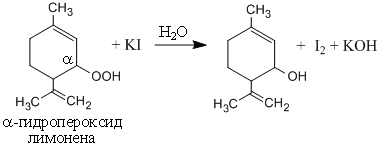
Методика эксперимента. В пробирку поместить 1 каплю 10% раствора йодида калия и 5 капель исследуемого вещества (скипидар, укропное масло, олеиновая кислота, подсолнечное масло и др.). Смесь энергично встряхните. Выделяющийся йод окрашивает раствор от соломенно-желтого до коричневого цвета. Если окраска раствора слабо соломенно-желтая (т.е. плохо различима), то прибавьте к смеси 1-2 капли 1% раствора крахмала. В присутствии йода окраска раствора приобретает синий цвет.
Наблюдения: Выводы:
ОПЫТ №7. Реакция подлинности терпингидрата
В фарфоровую чашку (на 20-30мл) помещают 1-2 кристалла терпингидрата, добавляют 5к раствора хлорида железа (III) в этаноле. Выпаривают жидкость досуха и наблюдают переход карминово-красной окраски в фиолетовую и зеленую на стенках чашки. После охлаждения добавляют 1мл бензола, наблюдают синее окрашивание.
Наблюдения: Выводы:
ОПЫТ №8. Обнаружение ароматических систем в соединениях
Реакция нитрования используется для обнаружения бензола в составе аминокислот, белков и других веществ, т.к. сопровождается образованием кристаллических или жидких продуктов желтого цвета.
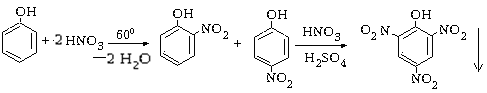
фенол о-нитрофенол п-нитрофенол пикриновая кислота
Методика эксперимента. В пробирку вносят несколько кристаллов или 0,5 мл исследуемого соединения (фенол, фенилаланин, раствор яичного белка и др.), затем приливают 1 мл концентрированной азотной кислоты, энергично встряхивают и нагревают до кипения. Наблюдают изменение окраски раствора, при добавлении 10% раствора гидроксида натрия окраска усиливается.
Наблюдения: Выводы:
Вопросы по лабораторной работе:
1. Напишите схемы химических превращений α-пинена, лежащих в основе проведенных реакций .
2. Используйте пробы для обнаружения кратных связей в молекулах других представителей терпенов и терпеноидов. Будут ли эти пробы положительными для ментола?
3. Исходя из условий, проведенного эксперимента, сделайте вывод об отношении терпенов к окислению.
4. Напишите схему реакции получения нитробензола из бензола. По какому механизму протекает эта реакция?
5. Объясните ориентирующее влияние нитрогруппы и напишите реакцию последующего нитрования нитробензола.
