
senchuk_v_v_biohimiya_kurs_lekcii
.pdfÓÄÊ 577.1(042) ÁÁÊ 28.072ÿ73 Ñ31
Печатается по решению Редакционно-издательского совета Белорусского государственного университета
Ð å ö å í ç å í ò û:
доктор химических наук В. А. Костюк; доктор биологических наук В. М. Шкуматов
Сенчук, В. В.
С31 Биохимия : курс лекций. В 2 ч. Ч. 1. Биомолекулы /
Â.В. Сенчук. — Мн. : БГУ, 2005. — 179 с. : ил. ISBN 985-485-453-1.
Первая часть курса лекций посвящена изложению основ биохимии в отношении важнейших биомолекул — природных органиче- ских соединений, организация и функционирование которых лежит в основе процессов жизнедеятельности.
Адресуется студентам и аспирантам, специализирующимся в области биологии, химии, экологии, биотехнологии, биофизики и других наук.
ÓÄÊ 577.1(042) ÁÁÊ 28.072ÿ73
ISBN 985-485-453-1 (÷. 1) |
© Сенчук В. В., 2005 |
ISBN 985-485-454-Õ |
© ÁÃÓ, 2005 |

ВВЕДЕНИЕ
Биохимия (биологическая химия) является важнейшей фундаментальной дисциплиной в системе университетского образования при подготовке специалистов — биологов, химиков, медиков. Биохимия — это наука о химических основах жизнедеятельности на всех уровнях организации живых систем, включая химическое строение и свойства природных соединений и их комплексов, основные пути и механизмы регуляции метаболизма, биохимиче- ские механизмы реализации генетической информации, хими- ческие основы биоинженерии и биоинформатики и др.
Становление биохимии как самостоятельной науки пришлось на конец XIX — начало XX в. в результате объединения физиологической химии, соответствующих разделов органиче- ской химии и ряда других направлений. В 1903 г. Карл Нейбер ввел в обращение термин «биохимия». Многие важнейшие вехи формирования биохимических знаний непосредственно обязаны проникновением в науку передовых инструментальных физиче- ских и химических методов анализа, тесным контактам с химиками, физиками, математиками и специалистами других специальностей.
Биохимия в настоящее время сохраняет тенденцию устойчи- во бурного развития и справедливо относится к числу приоритетных научных направлений в странах с развитой экономикой, привлекая около 20 % кадров и всех инвестиций в научные исследования. Эти обстоятельства находят отражение и в том, что около половины всех Нобелевских премий, присужденных в области химии и по физиологии и медицине, относятся к достижениям в области биохимии.
Общепризнано, что биохимия представляет собой в значи- тельной степени теоретическую и методическую основу всех биологических наук, медицины, сельскохозяйственных наук. Основополагающая роль по праву принадлежит биохимии в становлении и современном облике молекулярной генетики, биоинженерии и ее разделов — белковой, генетической и клеточной инженерии, фармацевтике и др. Биотехнология, создающая про-
3
изводственные процессы на основе биохимических принципов, также во всех отношениях базируется на достижениях биохимии. Молекулярная биология, отделившаяся от биохимии около 50 лет назад, уже не является альтернативным явлением, а напротив, формирует вместе с биохимией единый практически неразделимый комплекс знаний. Это нашло закономерное отражение и в создании Международного союза биохимии и молекулярной биологии (IUBMB), который формирует вершину мировой системы организации науки и образования.
Современная биохимия охватывает необъятную область знаний. Качественный и количественный состав живых организмов изучает статическая биохимия. Динамическая биохимия вклю- чает сведения о биохимических превращениях, т. е. метаболизм и биоэнергетику. Функциональная биохимия концентрируется на решении проблем взаимосвязи химической структуры биомолекул и функции живого. Биоорганическая химия создает физи- ко-химические основы биологических систем. Бионеорганиче- ская химия изучает роль неорганических соединений в жизни. В зависимости от объекта выделяют биохимию человека (медицинская, клиническая биохимия), биохимию животных, биохимию растений, ветеринарную биохимию, биохимию микроорганизмов. Техническая биохимия создает основы биотехнологических процессов, а биохимическая фармакология — основа создания лекарственных средств. Активно развивается сравнительная и эволюционная биохимия, экологическая биохимия, радиационная биохимия, космическая биохимия è äð. Нейрохимия изучает биохимические основы нейробиологии, т. е. организации и функционирования нервных систем. Выделяют также биохимию белков, биохимию липидов, биохимию нуклеиновых кислот и т. п. При известной самостоятельности все эти разделы и направления биохимии неизбежно очень тесно переплетаются, взаимодополняются и обогащаются, создавая новые перспективные со- четания.
Настоящая книга представляет собой часть курса лекций по биохимии, который в течение ряда лет читается для студентов 2 курса биологического факультета Белорусского государственного университета. Курс лекций не претендует на роль всеобъемлющего учебника по всем разделам биохимии. Это очевидно, так как даже мировые бестселлеры по основам биохимии уже давно перешагнули порог 3-томных изданий. Более того, опыт последних 5—10 лет показывает, что удачные попытки написать учеб-
4
ные пособия по биохимии относятся почти исключительно к изложению принципов биохимии. Поэтому настоящая книга посвящена изложению основ биохимии в отношении важнейших универсальных биомолекул — природных органических соединений, организация и функционирование которых лежит в основе процессов жизнедеятельности. Особое внимание уделяется рассмотрению тех биомолекул, функционирование которых принципиально для проявлений жизни. В книгу включен анализ следующих вопросов:
Классификация, структуры и свойства природных аминокислот, пептидов и белков. Структурная организация белков. Фолдинг белков. Продукты биохимических модификаций белков.
Классификация и номенклатура, особенности строения и свойства нуклеозидов и нуклеотидов. Структурная организация
èсвойства нуклеиновых кислот: одно- и двуцепочечные, кольцевые и линейные молекулы ДНК; матричные, рибосомальные и транспортные РНК.
Классификация и номенклатура, особенности строения, изомерии и конформации природных моносахаридов, олигосахаридов, полисахаридов, протеогликанов.
Классификация и номенклатура, строение и свойства жирных кислот, важнейших природных стероидов (холестерол, эргостерол, желчные кислоты, стероидные гормоны, витамины D), терпенов. Биохимия ацилглицеринов, восков, фосфолипидов, гликолипидов, эйкозаноидов (простагландинов, лейкотриенов, тромбоксанов, простациклинов).
Макроэргические соединения: АТФ и другие нуклеозидтрифосфаты, креатинфосфат, аргининфосфат, аминоацил-тРНК
èäð.
Классификация, номенклатура, структура и свойства отдельных представителей водорастворимых и жирорастворимых витаминов. Анализ коферментных форм витаминов.
Безусловно, этим не ограничивается перечень органических соединений, входящих в состав биологических объектов.
Алкалоиды составляют очень разнообразную по структуре большую группу биологически активных соединений, синтезируемых в основном растениями. Многие алкалоиды очень важны для человека, так как составляют фармакологически активную основу десятков тысяч лекарственных препаратов. Не менее важны и интересны антибиотики — биологически активные вещества микроорганизмов, многие из которых широко применя-
5
ются для борьбы с инфекционными заболеваниями человека. Вместе с тем алкалоиды и антибиотики не относятся к числу универсальных биомолекул и их тщательное рассмотрение более уместно в других курсах лекций («Биологически активные соединения», «Фармакология», «Физиология растений», «Микробиология»). Некоторые углеводороды также принимают участие в биохимических процессах, однако их функции и биологиче- ская активность в большинстве случаев не относятся к универсальным и критическим для проявлений жизни. Среди животных распространены телергоны — вещества, синтезируемые железами внешней секреции и оказывающие специфическое действие на другие организмы. Следовательно, телергоны принимают самое непосредственное участие в межвидовых и внутривидовых химических коммуникациях. У животных развита нейрогуморальная регуляция процессов жизнедеятельности, которая реализуется при регуляторном участии гормонов, тканевых гормонов, факторов роста, нейромедиаторов. Некоторые вопросы находят отражение в настоящей книге, но детальный анализ классификации, строения и роли белково-пептидных гормонов, тиреоидных гормонов, катехоламинов, факторов роста, нейромедиаторов войдет в следующую книгу, посвященную рассмотрению метаболизма биомолекул. Неорганические компоненты живых объектов также составляют предмет для отдельного анализа. Таким образом, рассмотрение этих соединений несколько выходит за рамки издаваемого курса лекций «Биомолекулы».
Настоящая книга является частью создаваемого учебно-ме- тодического комплекса по биохимии в соответствии с реформой высшего образования в направлении многоступенчатой системы подготовки кадров. В рамках этой реформы приоритетное развитие самостоятельной работы студентов обеспечивается большим перечнем рекомендуемой литературы, приведенной в конце книги. Курс лекций может быть рекомендован для студентов университетов, специализирующихся в области биологии, экологии, биотехнологии, биофизики, химических и сельскохозяйственных наук.
АМИНОКИСЛОТЫ
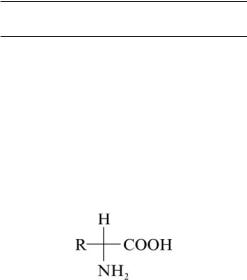
Аминокислоты — это универсальные природные соединения, аминопроизводные соответствующих карбоновых кислот. Следует отметить, что размеры скелета родоначальных карбоновых кислот ограничены и обычно составляют 2—6 С-атомов. Подавляющее большинство природных аминокислот представлены-аминокислотами с общей структурной формулой
Разнообразие природных аминокислот (> 300 индивидуальных соединений) обусловлено различиями в строении бокового радикала R. У всех живых объектов только 20 аминокислот являются генетически кодируемыми и составляют основу химиче- ской структуры биополимеров — пептидов и белков, а некоторые из них входят в состав ряда сложных соединений (фосфолипидов, желчных кислот, коферментов и др.). Разнообразные посттрансляционные биохимические модификации аминокислот, которые осуществляются путем специфического изменения строения боковых радикалов аминокислот в составе уже синтезированных белков и пептидов, приводят к появлению нескольких десятков модифицированных форм кодируемых аминокислот. Кроме этого, как генетически кодируемые, так и некодируемые аминокислоты содержатся внутри клеток и во внеклеточной среде в свободном состоянии. Свободные аминокислоты — это активные участники метаболических процессов, включая биосинтез белков, пептидов и меланинов, реакции детоксикации аммиака, биосинтеза гормонов, нейромедиаторов, монооксида азота, углеводов и многих других биомолекул.
7

Строение, классификация и номенклатура аминокислот
Классификация аминокислот может быть основана на полярности боковых радикалов, вследствие чего аминокислоты делят:
1)на неполярные (гидрофобные);
2)полярные;
3)кислые, отрицательно заряженные (при физиологическом
значении рН 7,4);
4) оснoвные, положительно заряженные (при рН 7,4). Особенности химического строения аминокислот позволяют
их классифицировать и по-другому:
моноаминомонокарбоновые;
моноаминодикарбоновые (кислые) и их амиды;
диаминомонокарбоновые (оснoвные);
гидроксиаминокислоты;
тиоаминокислоты;
гетероциклические;
другие.
Âнастоящее время общепринятым является использование тривиальных названий природных аминокислот, а также одно- и трехбуквенных сокращенных обозначений аминокислот. Хими- ческое строение важнейших природных аминокислот представлено в табл. 1.
|
|
|
|
|
|
|
Таблица 1 |
Важнейшие природные аминокислоты |
|
||||||
|
|
|
|
|
|
|
|
Название |
Обозначение |
|
|
Структурная |
|||
аминокислоты |
аминокислоты |
|
|
формула |
|||
|
|
|
|
|
|
|
|
Моноаминомонокарбоновые |
|
|
|||||
|
|
|
|
|
|
|
|
Глицин |
Ãëè |
Gly |
|
G |
|
H2C |
COOH |
Аминоуксусная кислота, |
|
|
|
|
|
|
|
гликокол |
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
L-Аланин |
Àëà |
Ala |
|
A |
|
H3C |
COOH |
2-аминопропионовая |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-Аланин |
-Àëà |
-Ala |
|
|
|
|
COOH |
3-аминопропионовая |
|
|
|
|
|
H2N |
|
|
|
|
|
|
|
||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8

Продолжение табл. 1
Название |
Обозначение |
|
Структурная |
|||||
аминокислоты |
аминокислоты |
|
формула |
|||||
|
|
|
|
|
|
|
|
|
-Аминомасляная |
ÃÀÌÊ |
GABA |
|
|
H2N |
|
COOH |
|
4-аминомасляная |
|
|
|
|
|
|||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Валин |
Âàë |
Val |
|
V |
|
CH3 |
||
2-амино-3-метилбутановая |
|
|
|
|
H3C |
COOH |
||
кислота |
|
|
|
|
||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
NH2 |
||
L-Норвалин |
|
Nva |
|
|
H3C |
|
COOH |
|
2-аминопентановая |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
L-Лейцин |
Ëåé |
Leu |
|
L |
H3C |
|
COOH |
|
2-амино-4-метилпентановая |
|
|
|
|
CH3 |
NH2 |
||
кислота |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
L-Норлейцин |
|
Nle |
|
|
|
|
|
COOH |
2-аминогексановая |
|
|
|
|
H3C |
|
||
|
|
|
|
|
|
|||
кислота |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
L-Изолейцин |
Èëå |
Ile |
|
I |
|
|
|
|
2-амино-3-метилпентановая |
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Фенилаланин |
Ôåí |
Phe |
|
F |
|
|
COOH |
|
2-амино-3-фенилпро- |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
пионовая кислота |
|
|
|
|
|
NH2 |
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Моноаминодикарбоновые (кислые) и их амиды |
|
|
||||||
|
|
|
|
|
|
|
|
|
L-Аспарагиновая кислота |
Àñï |
Asp |
|
D |
|
|
|
COOH |
2-аминоянтарная |
|
|
|
|
HOOC |
|
||
|
|
|
|
|
|
|||
кислота |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
L-Аспарагин |
Àñí |
Asn |
|
N |
O |
|
COOH |
|
|
|
|
|
|||||
-моноамид аспарагиновой |
|
|
|
|
NH2 |
NH2 |
||
кислоты |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
L-Глутаминовая кислота |
Ãëó |
Glu |
|
E |
HOOC |
|
COOH |
|
2-аминоглутаровая |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
L-Глутамин |
Ãëí |
Gln |
|
Q |
O |
|
COOH |
|
-моноамид глутаминовой |
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
|||
кислоты |
|
|
|
|
NH2 |
|||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
9

|
|
|
|
|
|
Продолжение табл. 1 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||
Название |
|
Обозначение |
|
Структурная |
|||||||||
аминокислоты |
|
аминокислоты |
|
|
формула |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
Диаминомонокарбоновые (оснoвные) |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Орнитин |
|
|
Orn |
|
|
|
|
|
|
|
|
|
COOH |
2,5-диаминопентановая |
|
|
|
|
|
H2N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Лизин |
|
Ëèç |
Lys |
|
K |
H2N |
|
|
|
|
|
|
COOH |
2,6-диаминогексановая |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Аргинин |
|
Àðã |
Arg |
|
G |
|
|
|
|
|
|
|
|
2-амино-5-гуанидинова- |
|
|
|
|
|
|
|
|
|
|
|
|
|
лериановая кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Гидроксиаминокислоты |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Серин |
|
Ñåð |
Ser |
|
S |
|
|
|
|
|
|
COOH |
|
2-амино-3-гидроксипропио- |
|
|
|
|
|
HO |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
новая кислота |
|
|
|
|
|
|
|
NH2 |
|
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Треонин |
|
Òðå |
Thr |
|
T |
|
|
OH |
|
||||
2-амино-3-гидроксибута- |
|
|
|
|
|
H3C |
|
COOH |
|||||
новая кислота |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
NH2 |
|
||||
L-Тирозин |
|
Òèð |
Tyr |
|
Y |
|
|
|
|
|
|
|
COOH |
4-гидроксифенилаланин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Тиоаминокислоты |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Цистеин |
|
Öèñ |
Cys |
|
C |
|
|
|
|
|
|
COOH |
|
2-амино-3-меркаптопро- |
|
|
|
|
|
HS |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
пионовая кислота |
|
|
|
|
|
|
|
NH2 |
|
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Цистин |
|
(Öèñ)2 |
(Cys)2 |
|
|
HOOC |
|
|
|
|
|
|
COOH |
3,3’-дитиобис (2-аминопро- |
|
|
|
|
|
|
|
S |
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|||||
пионовая кислота); |
|
|
|
|
|
NH2 |
|
|
NH2 |
||||
дицистеин |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Метионин |
|
Ìåò |
Met |
|
M |
|
S |
|
|
COOH |
|||
2-амино-4-(метилтио)бута- |
|
|
|
|
|
H3C |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
новая кислота |
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
Гетероциклические |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Пролин |
|
Ïðî |
Pro |
|
P |
|
|
|
|
|
COOH |
||
пирролидин-2-карбоновая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
H |
|
|||||
|
|
|
|
|
|
|
|
|
|||||
10

|
|
|
|
|
Окончание табл. 1 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Название |
Обозначение |
|
|
|
Структурная |
||||||||||||||||
аминокислоты |
аминокислоты |
|
формула |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-4-Гидроксипролин |
|
Hyp |
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
||
4-гидроксипирролидин- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
N |
|
|||||||||||
2-карбоновая кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Гистидин |
Ãèñ |
His |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
COOH |
|||||||
-амино-1Н-имидазо- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лил-4-пропионовая кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|||||
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Триптофан |
Òðï |
Trp |
|
W |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
-амино-3-индолилпропио- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
новая кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L-Пироглутаминовая |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
||||||||
|
|
|
|
|
N |
|
|
|
|
||||||||||||
2-пирролидон-5-карбоновая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота; 5-оксопролин |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Другие |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таурин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||
аминоэтан- -сульфоновая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SO3H |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
L- -карбоксиглутаминовая |
|
Gla |
|
|
HOOC |
|
|
|
|
|
|
|
COOH |
||||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4-карбоксиглутаминовая |
|
|
|
|
|
HOOC NH2 |
|||||||||||||||
кислота |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Моноаминомонокарбоновые аминокислоты
Глицин — самая простая по структуре аминокислота. С тех пор как в 1820 г. А. Браконно получил глицин из гидролизата желатина, глицин открывает список природных аминокислот. Глицин входит в состав практически всех белков. Максимальное содержание глицина в белках достигает в желатине около 25 %. Глицин создает в белках изгибы полипептидной цепи. В свободном состоянии глицин проявляет свойства тормозного медиатора в стволе головного мозга и в спинном мозге.
L-Аланин содержится почти во всех белках, участвует в реакциях переаминирования, в биосинтезе терпенов, жиров и углеводов.
11
