
- •6.Биноминальное распределение. Распределения Пуассона и Гаусса. Флуктуации.
- •8.Распределение Максвелла по абсолютному значению скорости. Характерные скорости.
- •12.Процессы переноса в газах. Теплопередача, диффузия и трение. Взаимодиффузия в газе из различных молекул. Основные особенности явлений переноса в твердых телах и жидкостях.
- •13.Физические явления в разреженных газах. Явления в сосудах, сообщающихся через пористую перегородку.
- •16.Броуновское движение.Вращательное броуновское движение
- •17 Степени свободы молекул. Теорема о равнораспределении энергии по степеням свободы. Внутренняя энергия идеального газа.
- •18.Теплоемкость идеального газа.Расхождение теории теплоемкостей.
- •19.Внутренняя энергия тел.Теплоемкость изотропных и однородных тел.Количество теплоты.
- •21.Работа.Первое начало термодинамики.Равновесные и неравновесные процессы.
- •23. Скорость звука в газах. Уравнение Бернулли.
- •24.Тепловая машина.Кпд цикла.Холодильная Машина.Цикл Карно.Кпд Карно.
- •25.Формулировка Клаузиуса и Томсона(Кельвина) второго начала темодинамики.Первая теорема Карно.Равенство Клаузиуса.
- •26.Энтропия,Энтропия идеального.Вторая теорема Карно.Неравенство Клаузиуса.Изменени энтропии при необратимых процессах.
- •27.Формулировка второго начала темодинамики с помощью энтропии.Роль энтропии в производстве.Статистический характер.
- •28.Термодтнамическое равновесие. Эмпирические шкалы температур Международная практическая шкала Термодинамическая шкала Отрицательные абсолютные температуры
- •29.Понятие о термодинамич потенциалах.Принцип Ле-Шателье-Брауна.
- •30.Силы межмолекулярного взаимодействия.Ионная связь.Ковалентная связь.Силы Ван-дер-Ваальса.Потенциал Ленарда-Джонса.
- •31.Ураынение Ван-дер-Вальса. Изотермы газа Ван-дер-Вальса. Правило Максвела. Метостобильное состояние
- •32. Приведенное уравнения Ван-дер-Вальса. Внутрения энергия газа ванн-дер-Вальса.
- •33. Эффект Джоуля-Томсана
- •34.Переход из газообразного в жидкое. Экспериментальные изотермы.
- •35. Поведение 2-х фазной сис-мы. Ур Клапейрона-Клаузиуса
- •36.Зависимость свойств реальных газов от идеальных..
- •37.Вириальное ур состояния.
- •38.Сжижение газов. Свойство веществ при температуре близктй к 0.
- •39.Свойства и структура жидкостей жидкие кристаллы. Теплоёмкость жидкостей.
- •40.Поверхностное натяжение. Условия равновесия на границе двух жидкостей и на границе жидкость – твердое тело.
- •41.Давление под искривленной поверхностью жидкости. Капиллярные явления.
- •43.Кипение. Перегретая жидкость. Пузырьковая камера. Переохлажденный пар. Камера Вильсона.
- •44.Жидкие растворы. Растворимость. Теплота растворения.
- •45.Идеальные растворы. Закон Рауля. Закон Генри. Зависимость растворимости от температуры.
- •46. Диаграмма состояния раствора. Кипение жидких растворов.
- •48. Фазовые переходы первого и второго рода. Кристаллизация и плавление. Сублимация. Фазовые диаграммы. Полиморфизм.
- •49.Симметрия твердых тел. Кристаллические решетки. Примитивная решетка. Элементы симметрии решетки. Обозначения атомных плоскостей и направлений.
- •50.Теплоёмкость твёрдых тел. Физические процессы в кристаллах при деформациях. Дислокации.
32. Приведенное уравнения Ван-дер-Вальса. Внутрения энергия газа ванн-дер-Вальса.
Приведенное уравнение ВдВ Делая замену в уравнении Ван-дер-Ваальса:
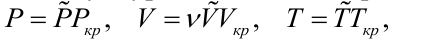
Получим приведенное уравнение Ван-дер-Ваальса
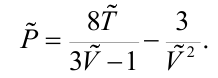
Видно, что при выборе в качестве единиц критических параметров вещества уравнение ВдВ принимает вид, одинаковый для всех веществ. Отсюда можно заключить, что и поведение различных веществ (в приведенных величинах) одинаково. Это утверждение называется законом соответственных состояний. Формулируется он так: если два приведенных параметра вещества одинаковы, то и третий параметр одинаков. Однако надо заметить, что закон соответственных состояний все же не соблюдается для реальных газов и жидкостей.
Отличие результатов
К сожалению, простая теория, связанная с использованием уравнения ВдВ не всегда адекватно описывает реальную ситуацию. Основные отличия следующие. 1. Для данного вещества постоянные а и b в уравнении Ван-дер-Ваальса должны быть независимыми от температуры. В действительности же они зависят от температуры. 2. Из соотношения критических параметров следует, что величина
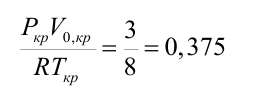
должна быть универсальной постоянной для всех веществ. В действительности же она изменяется.Например, для воды она равна 0,23, а для гелия 0,31. 3. Соотношение V0,кр=3b не соблюдается. Более точным соотношением является V0,кр≈2b. 4. В области двухфазных состояний уравнение Ван-дер-Ваальса не обосновано теоретически и дает расхождения с экспериментом.
Внутренняя энергия газа ВдВ
Взаимодействие между молекулами газа ВдВ обусловливает их взаимную потенциальную энергию. Поэтому, наряду с величиной νCVdT, в элементарное изменение внутренней энергии газа dU должна входить работа против внутренних сил притяжения dA’= Pвнутр dV. Следовательно, для газа Ван-дер-Ваальса
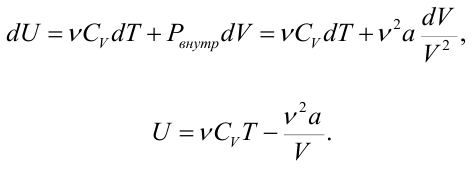
33. Эффект Джоуля-Томсана
Пропуская реальный газ по теплоизолированной трубке с пористой перегородкой, Джоуль и Томсон обнаружили, что при расширении, которым сопровождается прохождение газа через перегородку, температура его несколько изменяется. В зависимости от начальных давления и температуры изменениеприращения температуры ΔT имеет различные знаки («плюс» или «минус»). Это явление получило название эффекта Джоуля-Томсона. Если температура газа понижается (ΔT <0), эффект называется положительным; если газ нагревается (ΔT >0), эффект называется отрицательным. Пусть индексом «1» выделены, параметры, описывающие начальное состояния газа, а индексом «2» обозначим параметры, соответствующие его конечному состоянию (после расширения) Можно доказать, что в эксперименте Джоуля и Томсона сохраняется энтальпия, т.е. выполняется условие
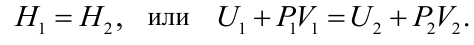

Таким образом, знак эффекта Джоуля-Томсона
определяется знаком выражения, стоящего в квадратных
скобках.
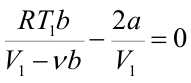
- эффект получается нулевым. Следует заметить, что эффект Джоуля-Томсона всецело обусловлен отклонениями газа от идеальности. Для идеального газа энтальпия H1 имеет вид
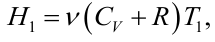
а условие равенства энтальпий принимает вид
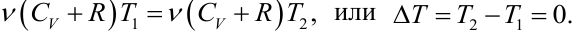
Т.е. эффект является нулевым.
