
- •«Амінокислотний склад і структура білків»
- •Теоретичне обґрунтування теми:
- •Амінокислоти
- •Таблиця 1. Класифікація амінокислот за полярністю радикалу Неполярний радикал
- •5.2. Пептидний зв'язок. Пептиди
- •Деякі гормони пептидної природи
- •Структура білків
- •Первинна структура
- •Фактори, які викликають специфічний гідроліз пептидних зв’язків
- •Вторинна структура
- •Третинна структура
- •Четвертинна структура
- •Фізико-хімічні властивості білків
- •Класи білків. Структурно-функціональна характеристика окремих представників
- •Структура та властивості фібрилярних білків
- •Лабораторна робота «Кольорові реакції на білки і амінокислоти»
- •Запитання і завдання для самоконтролю
- •Література
Лабораторна робота «Кольорові реакції на білки і амінокислоти»
Кольорові реакції дають можливість встановити білкову природу речовини і довести наявність деяких амінокислот в різних білках. Відомі універсальні кольорові реакції, які дають всі білки (біуретова). Специфічні реакції, які обумовлені наявністю тільки певних амінокислот (ксантопротеїнова, Фоля, Мілона та інші).
Виконати лабораторні досліди:
Дослід 1. Біуретова реакція.
1а. В суху пробірку беруть небагато (0,5г) сечовини і підігрівають на вогні. пробірку охолоджують і додають рівний об’єм 10% розчину NaOH, збовтують. Потім додають 1-2 краплі 1% розчину Cu2SO4 і знову перемішати. Спостерігати за кольором розчину.
1б. В пробірку наливають 1-2 мл розчину білка, додають 1-2 мл 10% розчину NaOH і 1-2 краплини 1% розчину CuSO4. Розчин перемішують. Спостерігають за кольором розчину, порівнюють його з кольором біурету.
Дослід 2. Ксантопротеїнова реакція.
2а. В одну пробірку налити 1 мл 1% розчину фенолу, додати 1 мл HNO3(1:1). Обережно нагріти.
2б. В другу пробірку налити 1 мл розчину білка, додати 1 мл HNO3 (1:1). Обережно нагріти. Спостерігати появу осаду жовтого кольору. Пробірку охолодити, додати 2-3 мл 20% розчину NaOH.
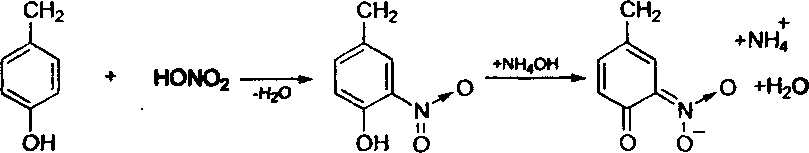
Дослід 3. Реакція Фоля на амінокислоти, які містять сірку.
У пробірку налити 1 мл 20% розчину NaOH і прокип’ятити з невеликою кількістю волосся. Пробірку охолодити і додати рівний об’єм 5% розчину оцтовокислого свинцю Pb(CH3COO)2.
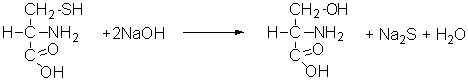
Na2S +Pb(CH3COO)2 PbS + 2CH3COONa
Звернути увагу на хімізм цих реакцій і їх застосування.
Запитання і завдання для самоконтролю
Що таке білки і в чому полягають їх біологічні функції?
Класифікація білків, характеристика основних груп (протеїни: альбуміни, глобуліни, протаміни, проламіни, гістони, протеїноїди; протеїди: нуклеопротеїди, хромопротеїди, глікопротеїди, ліпопротеїди).
Охарактеризувати структурну організацію білкової молекули і її хімічні зв’язки.
За допомогою яких кольорових реакції можна виявити: циклічні амінокислоти, сірковмісні амінокислоти, пептидний зв’язок у складі білків?
За допомогою яких хімічних реакцій можна відрізнити розчини яєчного білка, крохмалю, сахарози, глюкози?
Знати формули таких амінокислот: гістидин, аргінін, аспарагін, глютамін.
Література
Стеценко О.В., Виноградова Г.П. Біоорганічна хімія.-К.: Вища щкола,1992.- С. 9‑30, 50-58.
Боєчко Ф.Ф. Біологічна хімія. -К.: Вища школа, 1989.- С. 8-47.
Виноградова Г.П. та ін. Біологічна хімія. Практикум. -К.: Вища школа, 1977.-С. 7‑14.
|
|
|
Варіант 1 Напишіть пептид з таких амінокислот: фенілаланін, аспарагінова к-та, тирозин, гістидин. |
|
|
|
|
|
Варіант 2 Напишіть пептид з таких амінокислот: аргінін, цистеїн, аспарагін, лейцин. |
|
|
|
|
|
Варіант 3 Напишіть пептид з таких амінок-т: глютамінова к-та, триптофан, гістидин, метіонін. |
|
|
|
|
|
Варіант 4 Напишіть пептид з таких амінокислот: тирозин, глютамін, аргінін, фенілаланін. |
|
|
