- •1. Предмет, задачи и основные разделы токсик. Химии.
- •2. Возникновение и развитие токсикологической химии.
- •3. Особенности химико-токсикологического анализа. Методы токсикологической химии.
- •4. Организация судебно-химической экспертизы.
- •5. Основания для проведения судебно-химических экспертиз. Документация судебно-химических экспертиз.
- •6. Общие правила судебно-химического исследования. Консервирование вещественных доказательств.
- •7. Госуд. Медиц. Судебные эксперты-химики, их права и обязанности.
- •8. Методы токсикологической химии.
- •9. Методы изолирования ядовитых и сильнодействующих веществ из биологического материала.
- •10. Классификация метаболических превращений. Основные места метаболизма чужеродных соединений
- •11. Токсичность метаболитов. Фазы метаболизма
- •12. Основные пути метаболизма чужеродных соединений
- •13. Реакции биосинтеза (конъюгации)
- •14. Группа ядовитых и сильнодействующих веществ, изолируемых перегонкой с водяным паром.
- •15. Схема исследования дистиллята на наличие «летучих» ядов.
- •25. Газохроматографический анализ «летучих» ядов.
- •26. Методы минерализации биоматериала.
- •27. Минерализация серной и азотной кислотами.
- •28. Сравнительная характеристика методов минерализации.
- •29. Методы удаления окислителей из минерализата.
- •30. Методы количественного анализа минерализата.
- •31. Систематический метод анализа минерализата.
- •32. Дробный метод анализа минерализата.
- •33. Применение органических реагентов для обнаружения и количественного определения «металлических» ядов.
- •38. Характеристика веществ, экстрагируемых органическими растворителями из кислого раствора
- •39. Характеристика веществ, экстрагируемых органическими растворителями из щелочного раствора
- •41. Реакции окрашивания на алкалоиды
- •42. Производные барбитуровой кислоты. Общ.Хар-ка. Качеств. Обнар-е и колич. Определение барбитуратов (б). Токсикологическое значение (т.З).
- •43. Барбитал (б-л). Фенобарбитал (ф-л). Токсикологическое значение, изолирование, обнаружение и количественное определение.
- •44. Бутобарбитал, этаминал-натрия, барбамил. Изолирование, обнаружение, количественное определение. Токсическое значение.
- •45. Кофеин, теобромин, теофиллин. Токсикологическое значение. Изолирование. Обнаружение.
- •46. Алкалоиды(а) группы пиридина и пиперидина. Пахикарпин. Токсикологическое значение,изолирование,обнаружение,количественное определение.
- •47.Никотин, анабазин. Токсикологическое значение, изолирование, анализ.
- •48. Алкалоиды группы тропана (атропин, скополамин, кокаин). Токсикологическое значение, изолирование, качественное обнаружение.
- •49. Алкалоиды, производные хинолина (хинин). Токсикологическое значение, обнаружение в объектах биологического происхождения.
- •50. Алкалоиды, производные изохинолина (папаверин). Токсикологическое значение, изолирование, анализ.
- •54. Ациклические алкалоиды (эфедрин). Токсикологическое значение, изолирование, анализ.
- •55. Производные пиперидина (промедол). Токсик. Значение, изолирование, анализ.
- •56. Производные фенотиазина (аминазин, дипразин, левомепромазин, тиоридазин). Токсикологическое значение, изолирование, анализ.
- •60. Едкие щелочи, аммиак. Токсикологическое значение, изолирование, анализ.
- •62. Пестициды. Общая характеристика, классификация. Правила работы и техника безопасности.
- •66. Производные карбаминовой кислоты (севин). Токсикологическое значение.
- •69. Схема анализа веществ основного характера с использованием тсх-скрининга.
15. Схема исследования дистиллята на наличие «летучих» ядов.
Способы концентрирования и очистки дистиллята.
1. Экстракция орг. р-лями (диэтиловый эфир, СНСl3). Так конц-т изоамиловый спирт, анилин, фенол, крезолы.
Экстрагируя изоамиловый спирт эфиром, одновр-но проводят и очистку его от воды, т.к. р-цию на изоамиловый спирт проводят в отсутствии воды. Этиленгликоль из крови и мочи извлекают ацетоном, который затем испаряют. Такой способ позволяет увеличить конц-цию этиленгликоля по сравнению с исх-й при исследовании крови в 5-10 раз, мочи – 25-50 раз.
2. Фракционная (дробная) перегонка проводится в колбах с дефлегма-торами. Получаются фракции с близкими Ткип.
3. При изолировании этиленгликоля в колбу с биоматериалом приб-т бензол в качестве переносчика. Прибор имеет специальную насадку.
Схема исследования дистиллята химическим методом. Первый дистиллят иссл-т на наличие цианид-ионов. Наиболее доказательной явл-ся реакция образования берлинской лазури. Это высокочувствительная и избирательная р-ция, др. р-ции имеют вспомогат. значение.
Со вторым дистиллятом проводят исследование на:
1. Формальдегид – р-ция с фуксинсернистой или хромотроп. к-тами, при положит. рез-те р-ции – р-ция с реакт. Фелинга и р-ция восстан-ния Ag+.
2. Метанол – при отсутствии HCOH метанол окисляют до формальдегида (р-р K2Cr2O7 в H+), а затем проводят перечисл. р-ции на формальдегид. При обнаруж. формальдегида на метанол проводят только р-цию обр-ния метилсалицилата или опред-т метанол методом ГЖХ.
3. Алкилгалогениды: выполн-ся р-ция отщепления органич. связ. хлора (пров-ся после гидролиза этанольным р-ром NaOH). При положит. р-ции на Cl- проводят внутригруп. идент-цию алкилгалогенидов: р-ция обр-ния изонитрила; р-ция с резорцином; р-ция с реакт. Фелинга. При положит. р-ции отщепления органически связ. хлора и отриц-х р-циях (а, б, в) проводят спец. иссл-вание на дихлорэтан: р-ция переведения ДХЭ в этиленгликоль с послед. окислением его до формальдегида, на кот. проводят р-ции с фуксинсернистой или хромотроповой кислотами; вторая характерная р-ция на ДХЭ – образование ацетиленида меди, имеющего красную окраску.
Остаток второго дистиллята смеш-т с третьим и проводят р-ции на алкилгалогениды, т.е. при положит. предварит. р-циях проводится внутригруп. идентификация алкилгалог-дов.
При анализе дистиллята на фенолы и изоамиловый спирт дистиллят подщелачивают р-ром NaHCO3 и извлекают эфиром.
Эфирные экстракты соед-т, фильтруют, удаляют эфир и проводят исследование на фенолы и изоамиловый спирт. На фенолы проводят предварит. р-цию обр-ния трибромфенола. Эта р-кция более чувств-на, чем р-ция с FeCl3, и имеет отрицат. судебно-хим. значение. Если эта р-ция положит., то на фенолы проводят доп. р-ции (с хлоридом железа, образование индофенола).
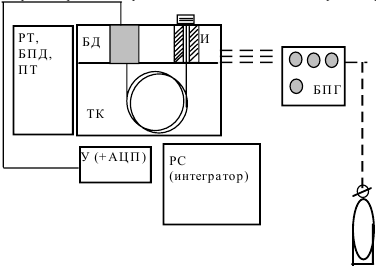
25. Газохроматографический анализ «летучих» ядов.
Газовая хроматография - это хроматографическое разделение веществ в системе газ - твердое тело или газ – жидкость. Исп. для анализа газов и летучих соед-ний.
|
|
Осн. блок: аналитический блок (БА), включ. 3 узла: 1) блок инжектора (устройства для ввода пробы; сост. из уплотнителя, узла крепления колонок и термостата испарителя (И)), 2) термостат колонок (ТК), 3) блок детекторов (БД). Для поддержания необх-й температуры служит регулятор температуры колонок, испарителя и детектора (РТ). Блок питания детек |
торов (БПД) служит для подачи электр. сигнала на детектор. Для работы в режиме программирования температуры служит программатор температуры (ПТ). Газовые системы предст. блоком подготовки газов (БПГ). Газ-носитель обычно подается из баллона редуктором, кот. снижает это давление.
Получаемый сигнал с детектора передается на блок усилителя (У), откуда передается либо непоср-но на аналоговый цифровой преобр-ль (АЦП) и далее на компьютер (РС).
Детектор – устр-во, реаг. на изменение опред-х св-в смеси «разделяемый компонент + газ-носитель». Требования: чувств-ть, селект-ть; динамич-й диапазон. В газовых хромат-фах наиболее широко исп-ся такие детекторы:
ДТП (детектор по теплопроводности) – принцип: электрическое сопротивление проводников изм-ся в зав-ти от теплопроводности газов (а она при изменении состава газа).
ДЭЗ (детектор электронного захвата) в камере ДЭЗ есть источник радиоактивного излучения. Молекулы газа-носителя (азот, аргон и др.) иониз-ся с освоб-м электрона. Молекулы, в состав кот. входят атомы P, S, N, Hal, захв-т эти электроны. Образ-ся ионы менее подвижны и ток детектора уменьш-ся.
ПИД (пламенно-ионизационный) в камеру детектора подаются водород в смеси с газом-носителем и воздух для поддержания пламени. В пламени чистого водорода нет ионов и фоновый ток детектора миним-й. При поступлении в пламя анализ. в-в они иониз-ся, число ионов увелич-ся, и сила тока возр-т.
ТИД (термоионный) работа основана на ионизации в пламени водорода паров соли щелочного металла (н., CsBr) и ее увеличении при попадании в пламя фосфорорг-х и азотсод-х (н-р, акилнитриты) соед-й. Сила тока зависит от кол-ва ионов, образ-ся в пламени.
Пробоподготовка при определении летучих в-в.
1. Анализ равновесной парогазовой фазы (ПГФ). пробу помещают в стекл. флакон, прибавляют хим. агент - безводный Na2SO4 для удаления паров воды, фосфорновольфрамовую или трихлоруксусную кислоту (осажд. белков). Затем флакон плотно укуп-т пробкой с фиксатором и нагр-т на водяной бане при Т на 5-10°С выше Ткип выделяемого в-ва. После этого пробку прокал-т и отбирают пробу шприцем (1-2 см3) и вводят в испаритель хроматографа. Метод универсален, экспрессен и прост.
2. Твердофазная микроэкстракция. закл-ся в адсорбции летучих компонентов р-ра на сорбционном волокне, напыл-м на штоке газохром. шприца. По хим. структуре волокна чаще всего силиконы или полиэтиленгликоли. Данный вариант отлич-ся от анализа равновесной ПГФ: 1) высокой степенью конц-ния целевых компонентов пробы, 2) более высокой степенью очистки пробы. Однако треб-ся оборудование со спец. устр-вом для ввода пробы.
3. Динамическая газовая экстракция. Через пробу продувают газ-носитель, кот. «уносит» летучие компоненты из жидкой фазы. Эти компоненты конц-ся двумя методами: на сорбентах (см. выше), а также при исп-нии устр-ва криогенной фокусировки - охлаждение зоны ввода пробы в колонку при температуре жидкого азота. Метод исп-ся чаще всего при анализе микрокомпонентов при определении загрязнений питьевых и сточных вод.
Особен-ти газохром. определения «летучих» ядов.
Алифатические спирты - этанол и его суррогаты: в молекулах спиртов гидроксильная группа способ-т адсорбции на твердой фазе, поэтому пики спиртов асимметричны, что снижает точность их количеств. определения. Поэтому переводят их в алкилнитриты. Они явл-ся летучими в-вами уже при Ткомн. Для разделения алкилнитритов исп-ся малополярные НФ - сквалан, полиметилфенилсиликон, винилин и др. Детекторы - ДТП или ДИП. Колич. определение спиртов вып-ся методом внутр. стандарта - т.е. в-ва, кот. в известной конц-ции доб-ся к пробе и к стандартным градуировочным р-рам. Величиной, пропорц-й конц-ции опред. спирта, явл-ся отн-ние высот или площадей пика спирта к высоте или площади пика внутр. стандарта.
Этиленгликоль (ЭГ). Два варианта: 1) определение ЭГ в нативном виде - ГАХ, сорбент - полисорб-1, высокая температура колонки (150-180°С), детектор - ДИП. Исп-ся при анализе технических жидкостей. 2) получение более летучих и менее полярных производных – н., с алкилборными кислотами.
Хлорсодержащие органические вещества. Опр-ся в нативном виде, для разделения исп-т малополярные НФ - сквалан и др. Детектор - ДЭЗ, ДИП.
Уксусная кислота. Два варианта: 1) определение по нативному соединению в присутствии фосфорной кислоты; 2) определение в виде сложных эфиров (метил-, этилацетат).
Фенол, крезолы. Три варианта: 1) определение по нативным веществам с помощью силиконовых НЖФ или ПЭГ и их сложных эфиров; 2) в виде силильных производных (цель их получения - снижение адсорбции на твердой фазе и увеличение летучести фенолов); 3) получение бромпроизводных - для повышения чувствительности определения (детектор - ДЭЗ).
Формальдегид. Полимер-ся в детектир. системе, => опр-т в виде производных – восстан-ние до метанола (метана), получ. азометинов или гидразонов.