- •Уровень в
- •2. Эквивалент. Закон эквивалентов уровень в
- •3. Способы выражения состава раствора уровень b
- •1. Плотность 6% водного раствора ортофосфорной кислоты равна 1,031 г/см3. Рассчитать:
- •2. Определить объем 16%-ного раствора карбоната калия плотностью 1,149 г/см3, необходимого для приготовления 3 л 0,2 м водного раствора данного вещества. Пояснить процесс приготовления раствора.
- •4. Энергетика химических реакций уровень b
- •3. Рассчитать теплотворную способность каменного угля, если известно, что в нем содержится 80% углерода, а в отходящих газах после сгорания угля содержится 14% со2 и 2% со по объему.
- •5. Скорость химических реакций и химическое равновесие уровень в
- •6. Физико-химические свойства растворов уровень в
- •3. Определить кажущуюся степень диссоциации соли, если водный раствор хлорида алюминия с массовой долей 1,5% кристаллизуется (замерзает) при температуре (-0,690с).
- •7. Растворы сильных и слабых электролитов. Уровень в
- •2. Определить, образуется ли осадок, если смешали 100 см0,01м водного раствора хлорида кальция и 200 см0,02м водного раствора карбоната натрия.
- •3.Вычислить рН 0,0im водного раствора hno2, содержащего, кроме того, 0,02 моль/л kno2.
- •8. Гидролиз солей уровень в
- •9. Окислительно - восстановительные реакции (овр) уровень в
- •1. Уравнять реакцию. Указать окислитель и восстановитель.
- •4 Г брома.
- •2. Уравнять реакцию. Указать окислитель и восстановитель:
- •3. Определить направление протекания реакции:
- •10. Гальванические элементы коррозия металлов. Уровень в
- •11. Электролиз растворов
- •Уровень в
- •12. Получение и химические свойства металлов уровень в
3. Рассчитать теплотворную способность каменного угля, если известно, что в нем содержится 80% углерода, а в отходящих газах после сгорания угля содержится 14% со2 и 2% со по объему.
|
Дано: ωC = 80% масс.
ω
ω |
|
Qкаменного угля - ? |
Теплотворной способностью топлива называется тепловой эффект, который соответствует сгоранию единицы массы (1 кг) для твердых и жидких видов топлив (Qр, кДж/кг).
Приводим уравнения горения углерода
С(к) + О2(г) = СО2(г) (4.8)
С(к) + ½ О2(г) = СО(г) (4.9)
Из приведенных уравнений (ур. 4.8 и 4.9) следует, что масса сгоревшего углерода пропорционально объемам образовавшихся газов. Поскольку в каменном угле содержится 80% углерода, то в 1000 г каменного угля содержится 800 г углерода и в СО2превратилось (ур 4.8)
![]() г углерода,
г углерода,
а в СО превратилось:![]() г углерода (ур. 4.8)
г углерода (ур. 4.8)
Исходя из того, что тепловые эффекты реакций (4.8) и (4.9) есть стандартные энтальпии образования СО2и СО (величины табличные), но взятые с противоположным знаком, посколькуDН= -Qр
DfНo(298 K, СО2) = - 393,5 кДж/моль
и DfНo(298 K, СО) = - 110,5 кДж/моль
рассчитываем количество теплоты, выделившейся при сгорании 700 г углерода до СО2 (ур. 4.8). Молярная масса углерода
МС = 12 г/моль.
При сгорании
12 г углерода выделяется 393,5 кДж
700 г углерода выделяется Qр(4.8) кДж
откуда:
Qр(4.7)
![]() кДж
кДж
Рассчитываем количество теплоты, выделившейся при сгорании 100 г углерода до СО (ур.4.9).
при сгорании
12 г углерода выделяется 110,5 кДж
100 г углерода выделяется Qр(4.9) кДж
откуда:
Qр(4.9)
![]() кДж
кДж
Следовательно теплотворная способность каменного угля
Qр = Qр(4.8) + Qр(4.9) = 22954 + 921 = 23875 кДж/кг
5. Скорость химических реакций и химическое равновесие уровень в
1. При погружении цинковой пластины в раствор хлороводородной кислоты за одно и то же время при температуре 293 К выделилось 8 см3 водорода, а при температуре 303 К – 13 см3 водорода. Водород собран над водой при давлении 740 мм рт. ст. Рассчитать энергию активации протекающей реакции. Давление паров воды при температуре 293 К составляет 17,54 мм рт. ст., а при температуре 303 К - 31,82 мм рт. ст.
|
Дано:
Т1
= 293 К,
Т2
= 303 К,
P
P
P
= 740 мм рт.ст.
|
РЕШЕНИЕ: Zn + 2HCl = ZnCl2 + H2↑ Из уравнения
энергию активации
|
Скорость гетерогенной реакции определяем по уравнению:
![]() ,
моль/(см2·мин)
(5.4)
,
моль/(см2·мин)
(5.4)
где
![]() -
количество моль выделяющегося водорода;
-
количество моль выделяющегося водорода;
S – площадь цинковой пластины, см2;
τ – время протекания реакции, мин.
Определяем отношение скоростей выделения водорода при двух различных температурах (площадь пластины и время протекания реакции постоянны):
![]() =
=![]() :
:![]() =
=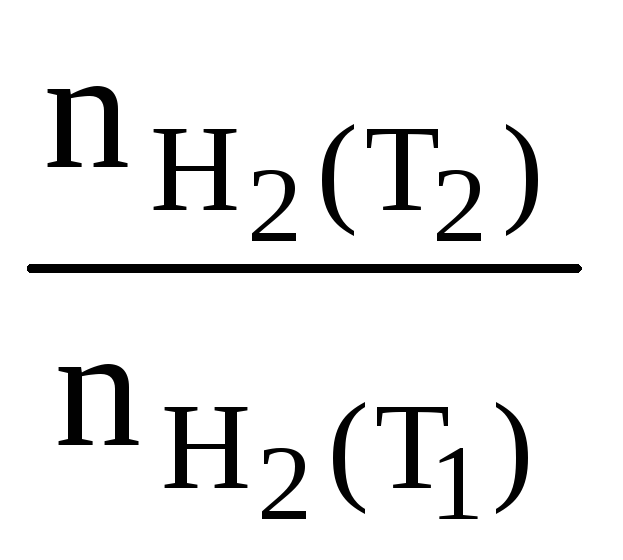 (5.5)
(5.5)
По уравнению Менделеева-Клапейрона
P![]() V
V![]() =n
=n![]() RT, а так какP
RT, а так какP![]() =(Р –P
=(Р –P![]() ),
то
),
то
(P–P![]() )V
)V![]() =n
=n![]() RT,
(5.6)
RT,
(5.6)
где Р – общее давление газов, мм. рт. ст;
P![]() -давление насыщенного
водяного пара при температуре опыта,
мм. рт. ст.;
-давление насыщенного
водяного пара при температуре опыта,
мм. рт. ст.;
V![]() - объем выделившегося водорода, см3;
- объем выделившегося водорода, см3;
Т - температура опыта, К;
R -универсальная газовая постоянная.
Из уравнения (5.6)
n![]() =(Р –P
=(Р –P![]() )V
)V![]() /RT(5.7)
/RT(5.7)
Подставив выражение (5.7) для температур Т1 и Т2 в отношение (5.5), получим
![]() =
=
![]() :
:![]()
=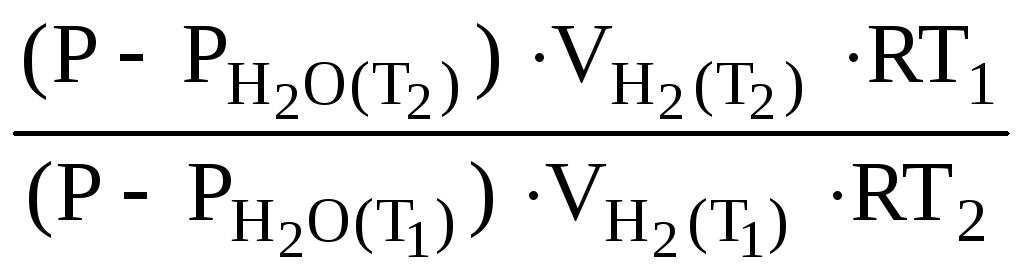
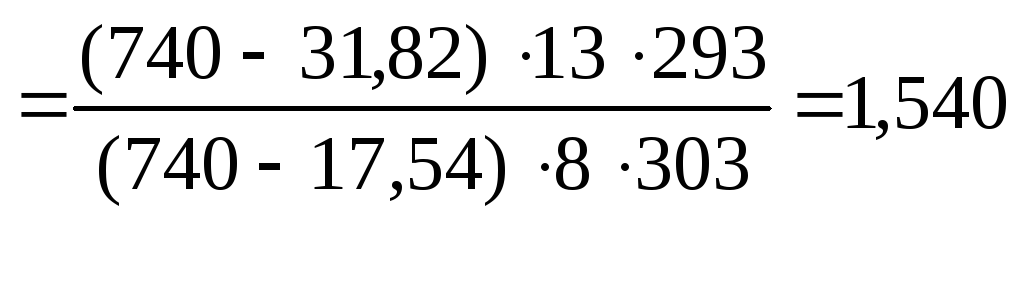
Откуда
![]() =
31834 Дж/моль =
=
31834 Дж/моль =
= 31,83 кДж/моль
Ответ:
![]() =
31,83 кДж/моль.
=
31,83 кДж/моль.
На основании принципа Ле Шателье определить, в каком направлении сместится равновесие:
2SO2(г) + O2(г) <=> 2SO3(г), ΔrH0(298K) = -284,2 кДж, при:
а) понижении температуры, б) повышении концентрации SO3, в) повышении давления. Записать выражение для константы равновесия реакции. Ответы обосновать.
|
Дано: Уравнение реакции ΔrH0(298K)=-284,2 кДж
Определить направление
смещения
равновесия
при изменении Т, Р, С |
РЕШЕНИЕ: Выражение константы равновесия реакции может быть приведено в зависимости от равновесных парциальных давлений газообразных участников реакции (5.8) или от их равновесных концентраций (5.9): |
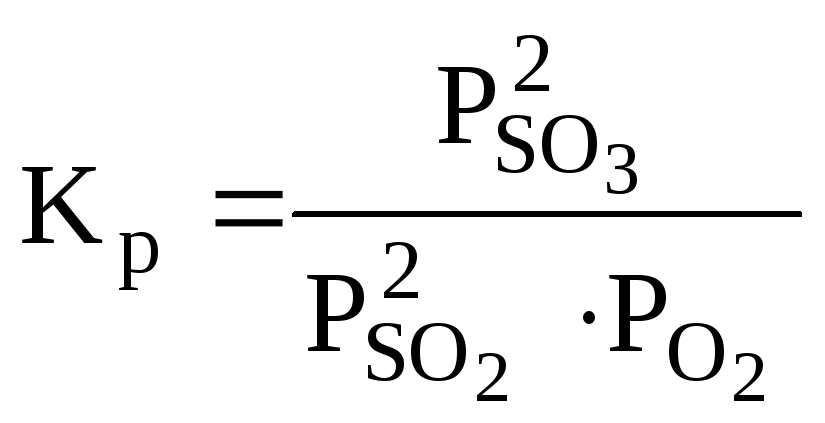 ,
(5.8)
,
(5.8)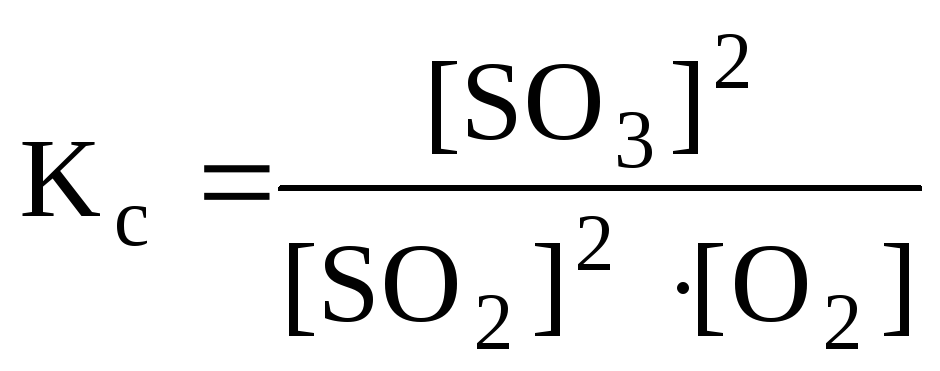 . (5.9)
. (5.9)
а) Выражение зависимости константы равновесия от термодинамических характеристик реакции имеет вид:
-2,3RTlgKP= ΔrH0(298K) –T.ΔrS0(298K), откуда
![]() .
Смещение равновесия реакции при изменении
температуры зависит от знака изменения
стандартной энтальпии реакции ΔrH0(298K).
Так как ΔrH0(298K)<0,
то при понижении температуры показатель
степени
.
Смещение равновесия реакции при изменении
температуры зависит от знака изменения
стандартной энтальпии реакции ΔrH0(298K).
Так как ΔrH0(298K)<0,
то при понижении температуры показатель
степени![]() возрастать.
возрастать.
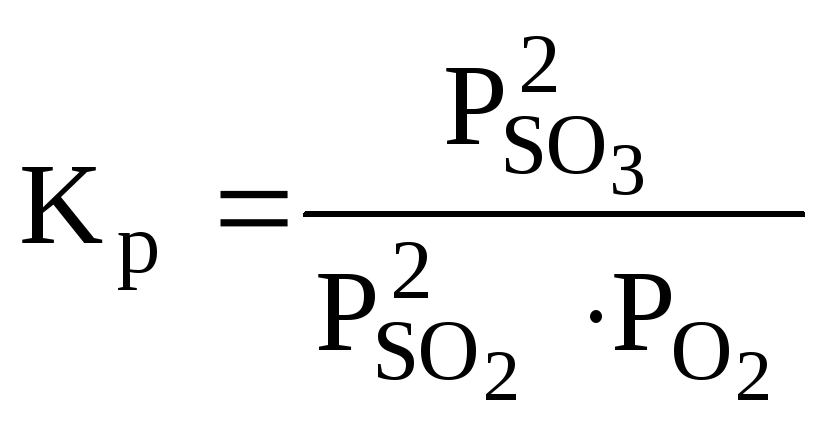 возрастает при увеличении числителя и
уменьшении знаменателя, а это возможно
при протекании прямой реакции, т.е
равновесие 2SO2(г)+O2(г)<=> 2SO3(г)будет смещено вправо (→).
возрастает при увеличении числителя и
уменьшении знаменателя, а это возможно
при протекании прямой реакции, т.е
равновесие 2SO2(г)+O2(г)<=> 2SO3(г)будет смещено вправо (→).
б) Константа равновесия
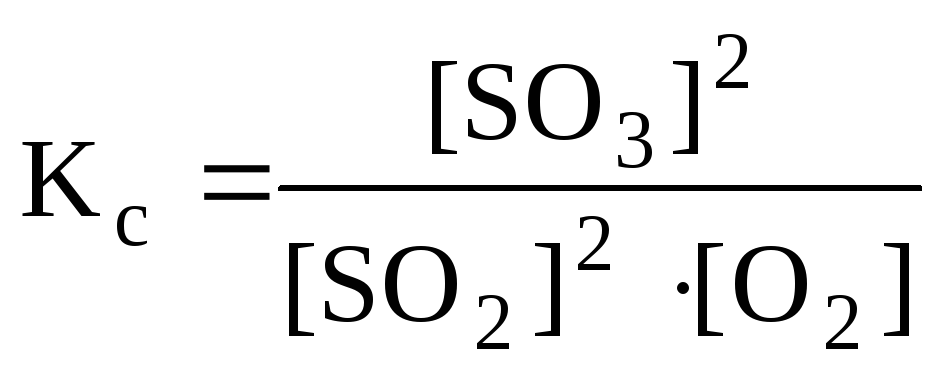 остается величиной постоянной при любом
изменении концентрации участников
реакции. Поэтому при повышении концентрацииSO3(числитель) при
неизменном значении КСдолжны
автоматически возрасти концентрации
исходных веществ (знаменатель), а это
возможно при протекании обратной
реакции, т.е. в этом случае равновесие
сместится влево (←).
остается величиной постоянной при любом
изменении концентрации участников
реакции. Поэтому при повышении концентрацииSO3(числитель) при
неизменном значении КСдолжны
автоматически возрасти концентрации
исходных веществ (знаменатель), а это
возможно при протекании обратной
реакции, т.е. в этом случае равновесие
сместится влево (←).
в) В соответствии с принципом Ле Шателье увеличение давления смещает равновесие в сторону той реакции, которая сопровождается уменьшением давления или уменьшением суммарного числа моль газообразных веществ.
![]() (газ)
(газ)
![]() =
2моль(газ)
=
2моль(газ)
Следовательно, при повышении давления равновесие системы смещается вправо (→).
Вычислить константу равновесия для гомогенной системы 4NH3(г) +3O2(г) <=> 2N2(г) + 6H2O(г), если исходные концентрации NH3(г) и O2(г) соответственно равны 6,0 и 5,0 моль/л, а равновесная концентрация N2(г) равна 1,8 моль/л.
|
Дано:
Уравнение
реакции,
[N2]
= 1,8 моль/л
Kс- ? |
РЕШЕНИЕ:
Расчет количеств прореагировавших и образовавшихся при установлении равновесия веществ проводится по уравнению реакции. Равновесная концентрация исходных |
веществ равна разности исходной концентрации и концентрации прореагировавших веществ. Равновесная концентрация продуктов реакции равна количеству образовавшихся продуктов реакции, т.к. в исходном состоянии их количество было равно нулю.
Обозначим через х количество моль
прореагировавших или образовавшихся
веществ. Тогда с учетом коэффициентов
в уравнении реакции отношения концентраций
во второй строке под уравнением реакции
равны: (![]() :
:![]() :
:![]() :
:![]() = 4:3:2:6).
= 4:3:2:6).
Последовательность расчетов равновесных концентраций веществ, участвующих в реакции, показана ниже:
|
|
4NH3+ 3O2 <=> 2N2 + 6H2O | ||||
|
Исходная концентрация веществ, моль/л |
6,0 |
5,0 |
|
0 |
0
|
|
Прореагирова-ло, моль/л |
- 4х
|
- 3х |
Образо-валось, моль/л
|
+ 2х
|
+
|
|
Равновесная концентрация веществ, моль/л |
6,0-4х |
5,0-3х |
|
2х |
6х |
По условию задачи равновесная концентрация N2равна 1,8 моль/л. В то же время [N2] = 2х. Следовательно, 2х = 1,8,
а х = 0,9. Тогда равновесные концентрации веществ равны, моль/л:
[NH3] = 6,0-4·0,9 = 2,4 моль/л,
[O2] = 5,0-3·0,9 = 2,3 моль/л,
[N2] = 1,8 моль/л,
[H2O] = 6,0·0,9 = 5,4 моль/л.
![]() =198,95.
=198,95.
Ответ: Kс= 198,95.

 -?
-?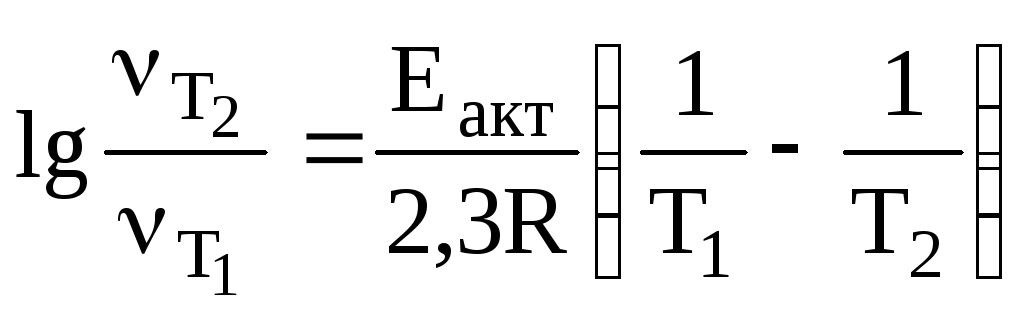 выражаем
выражаем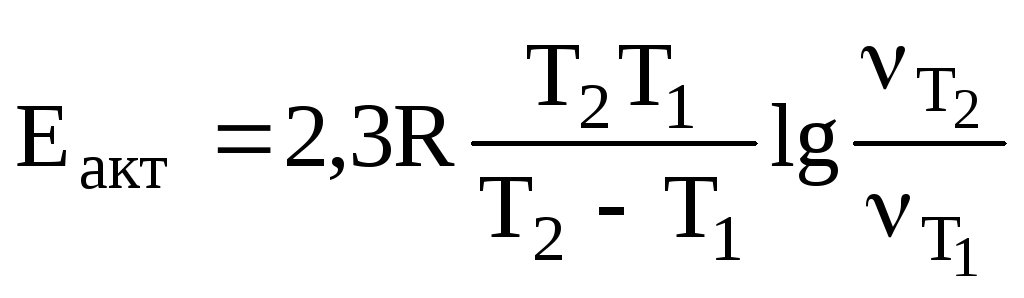 (5.3)
(5.3)

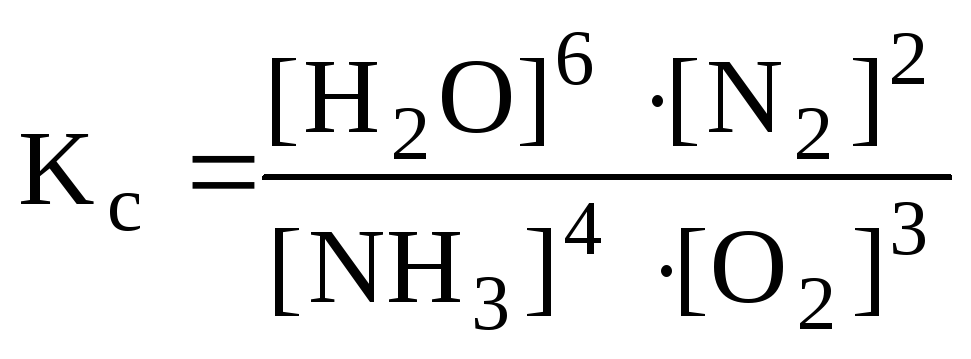 .
(5.11)
.
(5.11)



 6х
6х