
2 Молярного раствора гидроксида натрия
_________________________
40. ДЛЯ ТОГО, ЧТОБЫ рН РАСТВОРА УМЕНЬШИЛСЯ НА 2,
СЛЕДУЕТ СНИЗИТЬ КОНЦЕНТРАЦИЮ ИОНОВ ГИДРОКСИЛА В ____ РАЗ
_________________________
41. УСТАНОВИТЕ СООТВЕТСТВИЕ:
ДЛЯ ПРИГОТОВЛЕНИЯ ___________ РАСТВОРА
NaOH (молярная масса NaOH равна 40) НАДО
|
200 мл 1-молярного |
|
4г NaOH растворить в мерной колбе на 100 мл и довести водой до метки |
|
200 г 2-процентного |
8г NaOH растворить в мерной колбе на 100 мл и довести водой до метки | |
|
100 мл 1-молярного |
8г NaOH растворить в мерной колбе на 200 мл и довести водой до метки | |
|
100 мл 2-нормального |
4г NaOH растворить в 196 мл воды |
42. 48 ГРАММОВ КИСЛОРОДА
ЗАНИМАЮТ ОБЪЕМ ПРИ н.у.____ ЛИТРОВ
_________________________
43. Только полярные молекулы представлены в ряду…
( ) NH3,SO2,H2O
( ) BF3,CO2,SO2
( ) CO2,SO3,NH3
( ) CCl4,NO,NO2
44. Образование соли аммония возможно в химической реакции …
( ) Fe + HNO3 (конц.) >
( ) Zn + HNO3 (конц.) >
( ) Mg + HNO3 (разб.) >
( ) Cu + HNO3 (разб.) >
45. рН = 7 будет иметь водный раствор
( ) KCN
( ) Na2S
( ) Сu(NO3)2
( ) Ba(NO3)2
46. Число d-электронов в основном состоянии атома ванадия равно
_________________________
47. ДЛЯ РАСЧЕТА рН РАСТВОРА АЗОТНОЙ КИСЛОТЫ СЛЕДУЕТ ИСПОЛЬЗОВАТЬ ФОРМУЛЫ
[
] [H+]
=

[
] [H+]
=

[
]
pH =
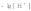
[
]
[H+]
=

48. КОНЦЕНТРАЦИЯ ИОНОВ ГИДРОКСИЛА РАВНА 10-11 .ЗНАЧЕНИЕ рН РАСТВОРА РАВНО
( ) 2.0
( ) 12.0
( ) 3.0
( ) 11.0
( ) 7.0
49. ПРИ УВЕЛИЧЕНИИ КОНЦЕНТРАЦИИ АЗОТА
В ТРИ РАЗА СКОРОСТЬ ПРЯМОЙ РЕАКЦИИ
N2 + O2 == 2NO
ВОЗРАСТЕТ В ____ РАЗА
_________________________
50. Число орбиталей на d-подуровне равно…(введите ответ)
_________________________
51. Число неспаренных электронов в ионе Со3+, находящемся в основном состоянии, равно …
_________________________
52. 100 ГРАММОВ ГИДРОКСИДА НАТРИЯ СОСТАВЛЯЮТ _____ МОЛЬ
_________________________
53. ЭЛЕМЕНТ, ИМЕЮЩИЙ ВАЛЕНТНЫЙ ЭЛЕКТРОННЫЙ СЛОЙ
5S2 называется _____
_________________________
54. ПЕРВОЕ ПРАВИЛО КЛЕЧКОВСКОГО:
( ) в атоме не может быть двух электронов, характеризующихся одинаковым набором квантовых чисел;
( ) заполнение атомных орбиталей происходит в последовательном возрастании суммы главного и орбитального квантового числа
( ) в пределах подуровня электроны заполняют максимальное количество орбиталей.
( ) тепловой эффект реакции зависит только от начального и конечного состояния системы и не зависит от промежуточных стадий процесса.
55. Формула высшего оксида элемента,
образующего водородное соединение ЭН2, имеет вид …
( ) ЭО4
( ) ЭО3
( ) ЭО
( ) ЭО2
56. Число неподеленных электронных пар на валентном энергетическом уровне атома азота в основном состоянии равно…
_________________________
57. Максимальное значение орбитального квантового числа для электронов
2 Энергетического уровня равно …
_________________________
58. НА ТИТРОВАНИЕ 50 мл 0,1 н РАСТВОРА HCl ПОТРЕБУЕТСЯ ____ мл децинормального РАСТВОРА NaOH
_________________________
59. 32 ГРАММА МЕДИ СОСТАВЛЯЕТ _______ МОЛЬ
_________________________
60. ПРОЦЕСС ОКИСЛЕНИЯ В РЕАКЦИИ
KBr + KВrO3 + H2SO4 ---> Br2 + K2SO4 + H2O
ВЫРАЖАЕТСЯ УРАВНЕНИЕМ:
( ) 2BrO3- + 12H+ - 1Oe == Br2 + 6H2O
( ) 2BrO3- + 12H+ + 1Oe == Br2 + 6H2O
( ) 2Br- + 2e == Br2
( ) 2Br- - 2e == Br2
61. Массовая доля серной кислоты в растворе, полученном добавлением 380мл воды к 1л 20%-ного раствора H2SO4 с плотностью 1,139 г/мл (с точностью до целых) равна… (введите ответ)
_________________________
62. ЭЛЕМЕНТ, ИМЕЮЩИЙ ВАЛЕНТНЫЙ ЭЛЕКТРОННЫЙ СЛОЙ
