
- •Содержание
- •Список условных обозначений
- •Предисловие
- •1. Способы выражения концентраций растворов
- •Задачи на нахождение массовой доли
- •Задачи на нахождение молярной концентрации
- •2. Теоретические основы биоэнергетики
- •2.1 Основные понятия термодинамики
- •2.2. Первый закон термодинамики
- •2.3. Тепловой эффект реакции. Закон Гесса
- •2.4. Энтропия. II закон термодинамики
- •2.5. Энергия Гиббса как критерий самопроизвольности процесса
- •3.Кинетика химических реакций
- •3.2.Факторы, влияющие на скорость химических реакций
- •3.3. Основные свойства ферментов
- •3.4. Ферментативный катализ
- •4. Кислотно-основное равновесие
- •4.1. Кислотность и основность среды
- •4.2. Буферные системы организма
- •5.Комплексные соединения
- •Биогенные элементы
- •Окислительно-восстановительные процессы
- •Высокомолекулярные вещества (вмс)
- •8.1.Общие понятия, классификация высокомолекулярных соединений
- •8.2. Общая характеристика растворов высокомолекулярных соединений
- •Водные растворы белков
- •Набухание высокомолекулярных соединений
- •Вязкость растворов высокомолекулярных соединений
- •Осмотическое (онкотическое) давление в растворах вмс
- •8.7. Мембранное равновесие Доннана
- •8.8. Специфические свойства растворов вмс
- •Классификация и номенклатура органических соединений
- •9.1. Классификация органических соединений
- •9.2. Номенклатура органических соединений
- •10. Пространственное строение органических соединений
- •10.3. Диастереомерия
- •11. Амины
- •Химические свойства
- •12. Спирты. Фенолы
- •Химические свойства спиртов
- •13. Альдегиды, кетоны
- •Химические свойства
- •4. Восстановление и окисление оксосоединений.
- •14. Карбоновые кислоты
- •Представители карбоновых кислот.
- •1. Монокарбоновые кислоты:
- •2. Дикарбоновые кислоты:
- •Изомерия
- •Химические свойства
- •15. Гетерофункциональные соединения
- •15.1. Аминоспирты
- •15.2. Гидроксикислоты
- •15.3. Оксокислоты
- •15.4. Гетерофункциональные производные бензола
- •15.5. Аминокислоты
- •Химические свойства
- •15.6. Пептиды. Белки
- •16. Углеводы
- •16.1. Моносахариды
- •Цикло-оксо-таутомерия
- •16.2. Производные моносахаридов
- •16.3. Дисахариды
- •16.4. Полисахариды
- •17. Гетероциклические соединения
- •17.1. Пятичленные гетероциклические соединения c одним гетероатомом
- •17.2. Пятичленные гетероциклы с двумя гетероатомами
- •17.3. Шестичленные азотсодержащие гетероциклы с одним гетероатомами
- •17.4. Шестичленные азотсодержащие гетероциклы с двумя гетероатомами
- •17.5. Конденсированные гетероциклы
- •18. Нуклеиновые кислоты
- •18.1. Нуклеозиды
- •18.2. Нуклеотиды
- •18.3. Нуклеиновые кислоты
- •19. Липиды
- •19.1. Омыляемые липиды
- •19.2. Неомыляемые липиды
- •19.2.1. Терпены
- •19.2.2. Стероиды
- •Эталоны ответов.
- •Литература
Химические свойства
Амины, являясь производными аммиака, имеют сходное с ним строение и проявляют подобные ему свойства. Амины, как и аммиак, обладают основными свойствами, а значит, способны взаимодействовать с кислотами с образованием соответствующих аммониевых солей.
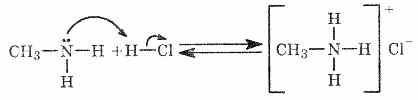
Аммониевые соли хорошо растворимы в воде, но плохо растворяются в органических растворителях. Водные растворы аминов обладают щелочной реакцией:

Амины вступают в реакции алкилирования с галогеналканами с образованием вторичных и третичных аминов. Алкилирование – это реакция введения в молекулу R- алкильного радикала.
CH3-NH2 + C2H5Br = CH3-NH-C2H5 +НBr (метилэтиламин)
При нагревании амины вступают в реакции ацилирования с карбоновыми кислотами и их ангидридами с образованием N-замещенных амидов. Ацилирование – это реакция введения в молекулу ацильного радикала (R-C=O)

Качественной реакцией на амины является реакция с азотистой кислотой с выделением газа азота и спирта.
C2H5NH2 + HNO2 → C2H5OH + N2↑+H2O
В ароматических аминах аминогруппа ориентирует другие заместители в орто- и пара-положения бензольного кольца. Поэтому галогенирование анилина происходит быстро и в отсутствие катализаторов, причем замещаются сразу три атома водорода бензольного кольца, и выпадает белый осадок 2,4,6-триброманилина (о,о,п-триброманилина):
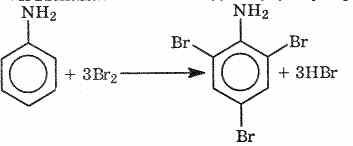
Эта реакция бромной водой используется как качественная реакция на анилин.
12. Спирты. Фенолы
Спиртами называют соединения, содержащие одну или несколько гидроксильных групп, непосредственно связанных с углеводородным радикалом.
Классификация спиртов разнообразна и зависит от того, какой признак строения взят за основу.
1. В зависимости от количества гидроксильных групп в молекуле спирты делят на: а) одноатомные (содержат одну гидроксильную ОН-группу), например, метанол СН3ОН, этанол С2Н5ОН, пропанол С3Н7ОН; б) двухатомные, например, этиленгликоль HO–СH2–CH2–OH; в) трехатомные - глицерин HO–СH2–СН(ОН)–CH2–OH и т.д..
2. По типу атома углерода, с которым связана группа ОН, спирты делят на:
а) первичные, у которых ОН-группа связана с первичным атомом углерода. Первичным называют атом углерода, связанный всего с одним углеродным атомом. Примеры первичных спиртов – этанол СH3–CH2–OH, пропанол СH3–CH2–CH2–OH.
б) вторичные, у которых ОН-группа связана с вторичным атомом углерода. Вторичный атом углерода связан одновременно с двумя атомами углерода, например, вторичный пропанол, вторичный бутанол.

в) третичные, у которых ОН-группа связана с третичным атомом углерода. Третичный углеродный атом связан одновременно с тремя соседними атомами углерода, например, третичный бутанол и пентанол.

У многоатомных спиртов, содержащих две или более ОН-групп, могут присутствовать одновременно как первичные, так и вторичные НО-группы, например, в глицерине или ксилите (рис. 3).

В зависимости от характера углеводородного радикала спирты делятся на алифатические, алициклические и ароматические, причем у последних гидроксильная группа не связана с атомом углерода бензольного кольца. Спирты, у которых гидроксильная группа связана с ароматическим кольцом, называются фенолами.
По систематической номенклатуре названия спиртов образуют, добавляя суффикс -ол к названию углеводорода с самой длинной углеродной цепью, включающей гидроксильную группу. Нумерацию цепи начинают с того края, ближе к которому расположена гидроксильная группа. Также часто встречаются тривиальные названия:
СН3–ОН – метанол, метиловый спирт;
СН3–СН2–ОН – этанол, этиловый спирт;
СН3–СН–СН3 – пропанол-2, изопропиловый спирт.
I
OH
Физические свойства спиртов зависят от строения углеводородного радикала, количества гидроксильных групп и их положения. Первые представители гомологического ряда спиртов — жидкости, высшие — твердые вещества. Метанол и этанол смешиваются с водой в любых соотношениях. С ростом молекулярной массы растворимость спиртов в воде падает. Высшие спирты практически нерастворимы в воде. Спирты обладают аномально высокими температурами кипения по сравнению с углеводородами, что объясняется сильной ассоциацией молекул спирта в жидком состоянии за счет образования достаточно прочных водородных связей:

Этим объясняется то, что уже первые члены гомологического ряда спиртов — жидкости, которые имеют сравнительно высокие температуры кипения. Образованием водородных связей между молекулами спирта и воды объясняется их хорошая растворимость в воде. Уменьшение же растворимости у последующих членов гомологического ряда вызывается увеличением числа атомов углерода в углеводородном радикале. Водородные связи — непрочные (17-22 кДж/моль) и при испарении спиртов легко разрываются.
