
По природе лиганда [править]
1) Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например: [Cu(NH3)4]SO4, [Co(NH3)6]Cl3, [Pt(NH3)6]Cl4 и др.
2) Аквакомплексы — в которых лигандом выступает вода: [Co(H2O)6]Cl2, [Al(H2O)6]Cl3 и др.
3) Карбонилы — комплексные соединения, в которых лигандами являются молекулы оксида углерода(II): [Fe(CO)5], [Ni(CO)4].
4) Ацидокомплексы — комплексы, в которых лигандами являются кислотные остатки. К ним относятся комплексные соли: K2[PtCl4], комплексные кислоты: H2[CoCl4], H2[SiF6].
5) Гидроксокомплексы — комплексные соединения, в которых в качестве лигандов выступают гидроксид-ионы: Na2[Zn(OH)4], Na2[Sn(OH)6] и др.
3.1. Общие структурные особенности аминокислот, входящих в состав белков
Общая структурная особенность аминокислот - наличие амино- и карбоксильной групп, соединённых с одним и тем же ?-углеродным атомом. R - радикал аминокислот - в простейшем случае представлен атомом водорода (глицин), но может иметь и более сложное строение.
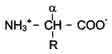
В водных растворах при нейтральном значении рН ?- аминокислоты существуют в виде биполярных ионов. В отличие от 19 остальных ?-аминокислот, пролин - иминокислота, радикал которой связан как с ?-углеродным атомом, так и с аминогруппой, в результате чего молекула приобретает циклическую структуру.

19 из 20 аминокислот содержат в ?-положении асимметричный атом углерода, с которым связаны 4 разные замещающие группы. В результате эти аминокислоты в природе могут находиться в двух разных изомерных формах - L и D. Исключение составляет глицин, который не имеет асимметричного ?-углеродного атома, так как его радикал представлен только атомом водорода. В составе белков присутствуют только L-изомеры аминокислот.

Чистые L- или D-стереоизомеры могут за длительный срок самопроизвольно и неферментатив-но превращаться в эквимолярную смесь L- и D-изомеров. Этот процесс называют рацемизацией. Рацемизация каждой L-аминокислоты при данной температуре идёт с определённой скоростью. Это обстоятельство можно использовать для установления возраста людей и животных. Так, в твёрдой эмали зубов имеется белок дентин, в котором L-аспартат переходит в D-изомер при температуре тела человека со скоростью 0,01% в год. В период формирования зубов в дентине содержится только L-изомер, поэтому по содержанию D-аспартата можно рассчитать возраст обследуемого.
Все 20 аминокислот в организме человека различаются по строению, размерам и физико-химическим свойствам радикалов, присоединённых к ?-углеродному атому.
Билет № 9
Предмет, задачи и основные понятия химической кинетики: система, фаза, процесс, механизм реакции, скорость реакции, средняя и истинная скорость химической реакции. Раздел химии, изучающий скорость и механизм протекания физико-химических процессов, называется химической кинетикой. Задачами химической кинетики являются: количественное описание процесса, установление факторов, влияющих на скорость реакций, установление механизма протекания реакций. Системой называют тело или совокупность 2 взаимодействующих тел, реально или мысленно выделенные в пространстве и способные обмениваться с окружающей средой или между собой энергией и (или) веществом. Часть системы, однородная во всех точках по составу, физическим и химическим свойствам и отделенная от других частей системы поверхностью, называется фазой. В зависимости от числа фаз различают гомогенные системы, состоящие из одной фазы, и гетерогенные — из двух или нескольких фаз. Изменение хотя бы одного из параметров состояния системы называется процессом. Механизм реакции – совокупность всех стадий, через которые происходит превращение исходных вещ-в в продукты реакции. Скорость реакции – число элементарных взаимодействий в единицу времени в единице реакционного пространства. Реакционным пространством в гомогенной системе служит объем сосуда, в котором происходит взаимодействие, в гетерогенной — поверхность раздела фаз. Средняя скорость реакции – изменение кол-ва вещества в единицу времени в единице реакционного пространства. Истинная (=мгновенная) скорость реакции – производная концентрации по времени.
Скорость химической реакции
Важным понятием химической кинетики является скорость химической реакции. Эта величина определяет, как изменяется концентрация компонентов реакции с течениемвремени. Скорость химической реакции — величина всегда положительная, поэтому если она определяется по исходному веществу (концентрация которого убывает в процессе реакции), то полученное значение домножается на −1. Например для реакции
![]() скорость
можно выразить так:
скорость
можно выразить так:
![]()
Молекулярность элементарной реакции — число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия.
Мономолекулярные реакции — реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д.):
H2S → H2 + S
Бимолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных):
СН3Вr + КОН → СН3ОН + КВr
Тримолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении трех частиц:
О2 + NО + NО → 2NО2
