
- •3. Водорастворимые витамины
- •3.1. Тиамин (витамин в1, антиневритный)
- •3.2 Рибофлавин (витамин в2)
- •3.3 Пантотеновая кислота (антидерматитный фактор)
- •Ниацин (витамин рр, антипеллагрический)
- •3.5 Пиридоксин (витамин в6)
- •3.6 Фолацин (витамин вс), фолиевая кислота
- •3.7 Кобаламин (витамин в12 антианемический)
- •3.8 Аскорбиновая кислота (витамин с, антискорбутный)
3.2 Рибофлавин (витамин в2)
Строение. В основе молекулы рибофлавина лежит гетероциклическое соединение – изоаллоксазин (сочетание бензольного, пиразинового и пиримидинового колец), к которому в положении 10 присоединен пятиатомный спирт рибитол (рис. 3.2.).
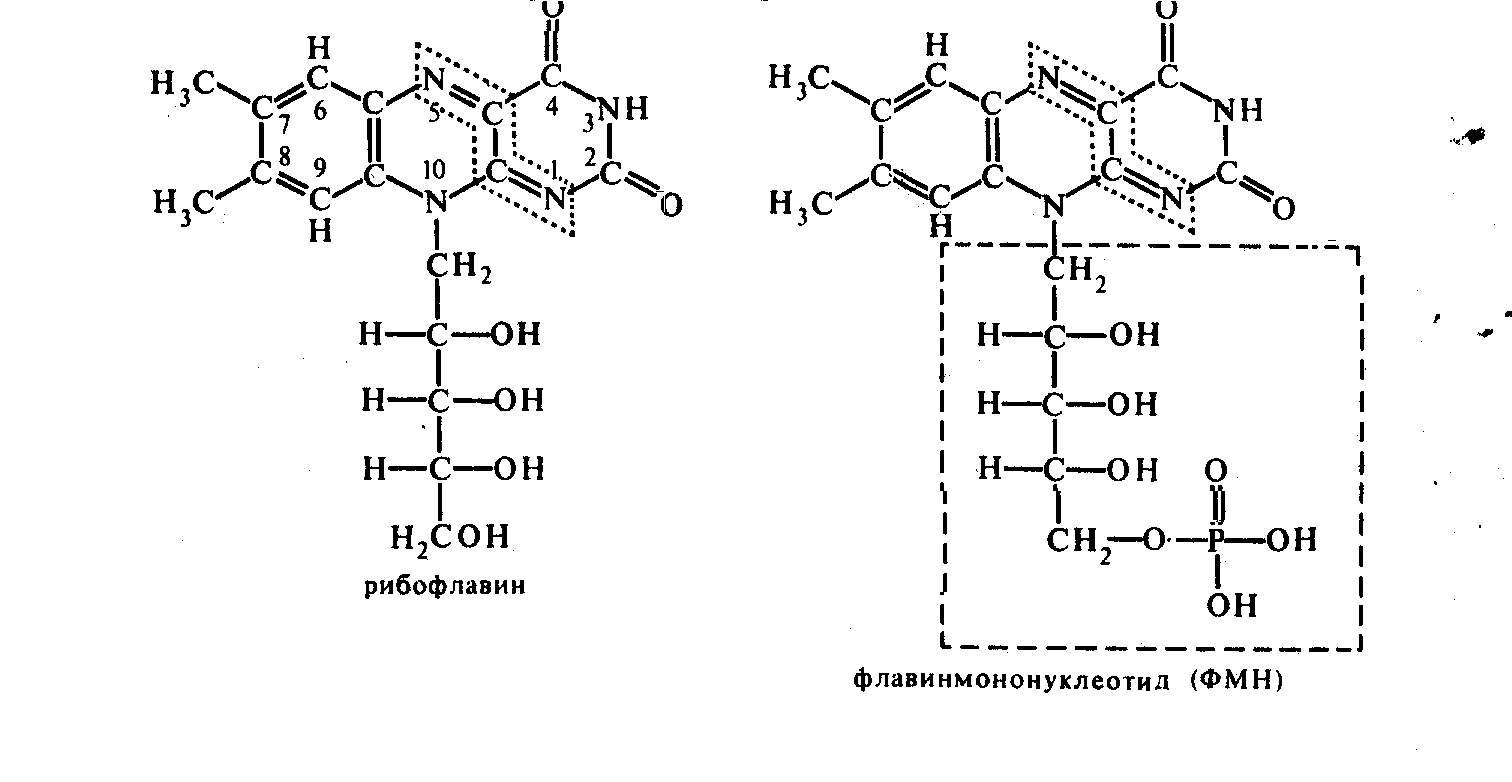
Рис 3.2. Структура рибофлавина
Рибофлавин хорошо растворим в воде, устойчив в кислых растворах, но легко разрушается в нейтральных и щелочных средах. Обладает желтым цветом и, экскретируемый из организма, придает окрашивание моче. На свету рибофлавин разрушается.
Пищевые источники. Источником витамина В2 для человека служат продукты питания и частично кишечные бактерии. Богаты рибофлавином печень, почки, желток яиц, пивные дрожжи, творог, сыр и молоко. Женское молоко содержит меньше рибофлавина, чем коровье. Поэтому детям, находящимся на естественном вскармливании, необходимо назначать витамин В2. Можно увеличить поступление рибофлавина в организм ребенка, назначая его матери. В пищевых продуктах рибофлавин находится не только в свободной форме, но и виде коферментных форм, связанных с белком.
Метаболизм и функции. В ЖКТ происходит освобождение рибофлавина, который всасывается путем простой диффузии в тонком кишечнике. В клетках слизистой тонкого кишечника, а также печени и клетках крови происходит образование коферментов ФМН и ФАД из рибофлавина по схеме
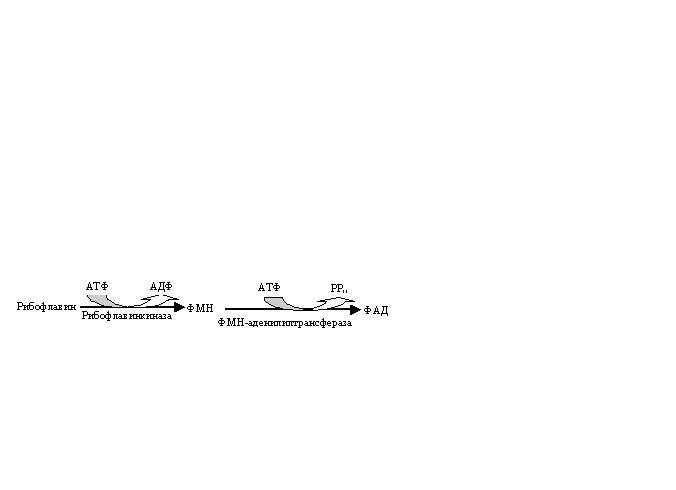
ФМН (рис. 3.3) или ФАД (рис. 3.4) в последующем прочно, но не ковалентно связываются с апоферментом. Многие флавопротеины содержат один или несколько металлов и известны как металлофлавопротеины. Так, молибден открыт в ксантиноксидазе и альдегидоксидазе, медь – в бутирилдегидрогеназе, железо – в НАДН-дегидрогеназе. Присутствие металла, по-видимому, повышает устойчивость семихинона (свободного радикала), являющегося промежуточной формой, в виде которой он функционирует как переносчик электронов.
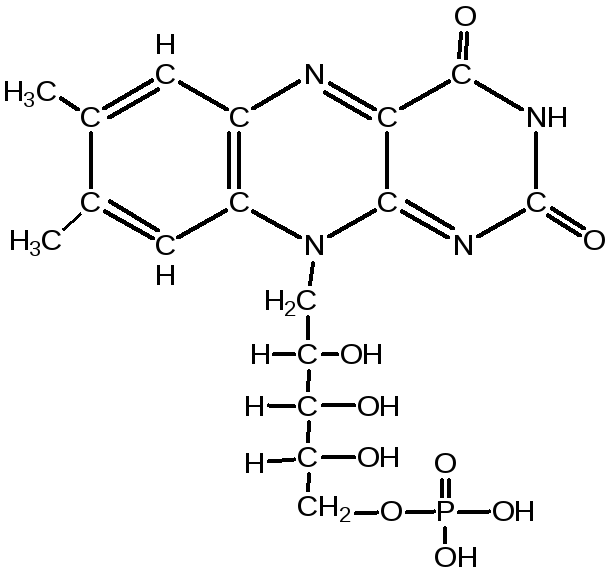
Рис 3.3. Структура флавинмононуклеотида (ФМН)
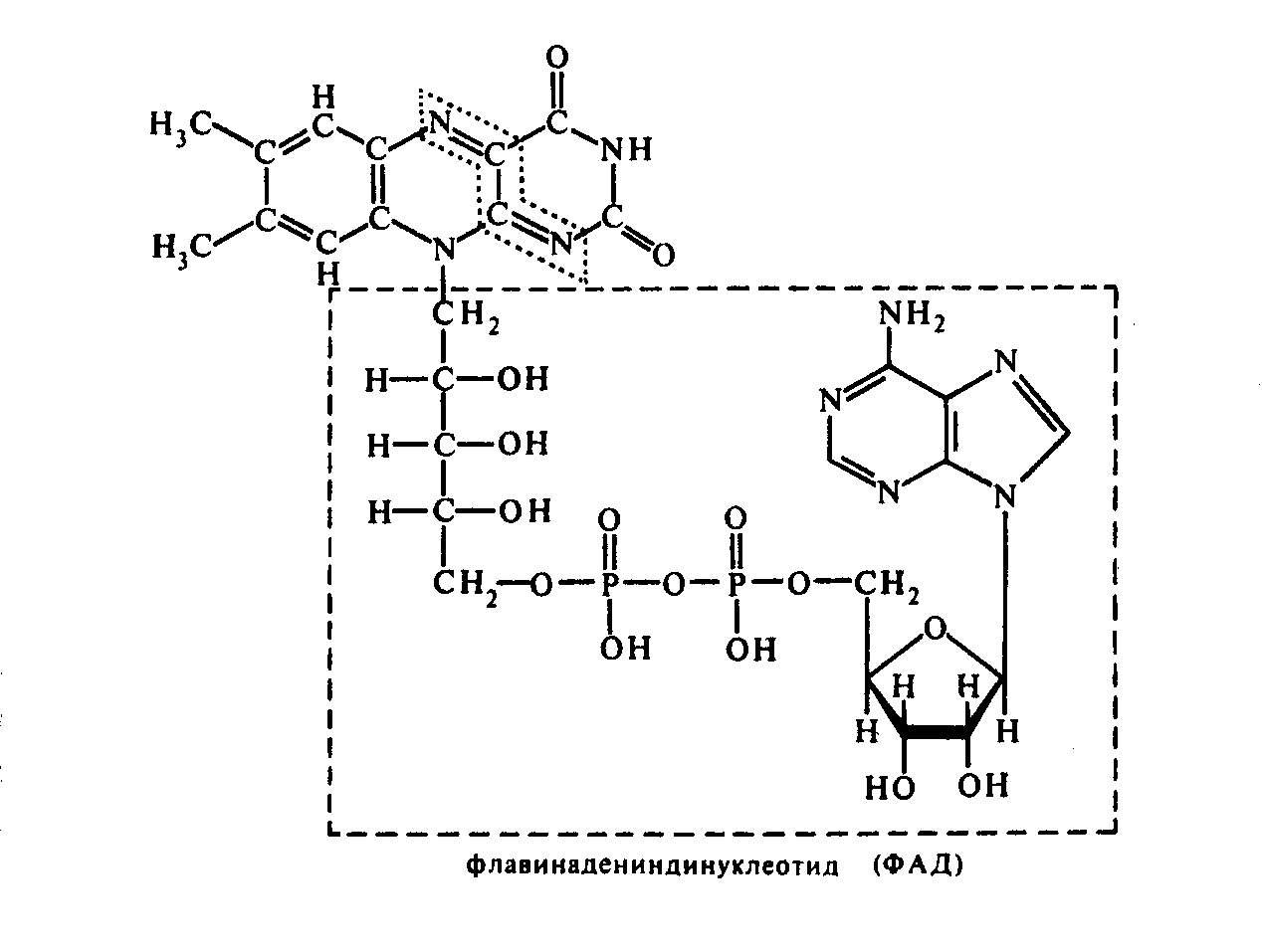
Рис.3.4. Структура флавинадениндинуклеотида (ФАД)
Способность легко принимать и отдавать протоны и электроны определяет участие этих коферментов в окислительно-восстановитель-ных реакциях (рис. 3.5). При восстановлении коферменты переходят в лейкоформу.
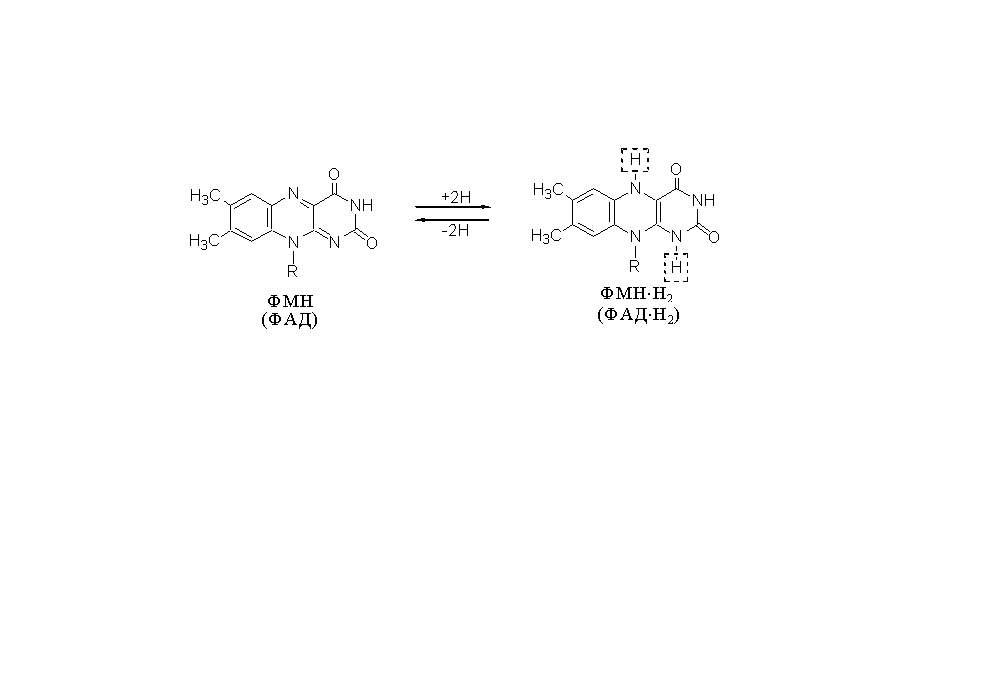
Рис. 3.5.Участие рибофлавина
в окислительно-восстановительных реакциях
Из организма рибофлавин выводится в основном в неизменном виде с мочой.
Участие витамина В2 в обмене веществ сводится к обслуживанию окислительно-восстановительных реакций в составе:
1. Ксантиноксидазы, участвующей в окислительном дезаминировании ксантина и гипоксантина с образованием мочевой кислоты. Этот фермент обнаружен в молоке, тонком кишечнике, почках и печени. Активность ксантиноксидазы сопровождается генерированием свободно-радикальных форм кислорода.
2. Альдегиддегидрогеназы, участвующей в деградации альдегидов с образованием кислот и перекиси водорода. Обнаружен в печени, кроме рибофлавина содержит молибден.
3. Глицерол-3-фосфатдегидрогеназы, участвующей в транспорте восстановленных эквивалентов из цитозоля в митохондрии. Она является составной частью глицеролфосфатного челночного механизма. Цитозольная глицерол-3-фосфатдегидрогеназа является НАДН-зависимой. Фермент катализирует восстановление дигидроацетонфосфата до глицерол-3-фосфата, который может проходить через мембрану митохондрий. Попав в митохондрии, глицерол-3-фосфат подвергается окислению ФАД-зависимой глицерол-3-фосфатдегидрогеназой. При срабатывании этого механизма происходит потеря АТФ на каждый потребленный НАДН. Такой челночный механизм работает в летательной мышце насекомых, белых мышцах, играет важную роль в печени.
4. Сукцинатдегидрогеназы цикла лимонной кислоты, осуществляющей окислительное превращение сукцината в фумарат.
5. Дегидролипоилдегидрогеназы, участвующей в дегидрировании восстановленного липоата (интермедиата при окислительном декарбок-силировании пирувата и 2-кетоглутарата)
6. НАДН-дегидрогеназы – важного компонента МЭТЦ, переносящего электроны от НАДН к более электроположительному компоненту – коэнзиму Ку
7. Ацил-КоА-дегидрогензы, участвующей в окислении жирных кислот
8. Глутатионредуктазы, которая переносит водород на окисленный глутатион, переводя его в восстановленную форму. Определение активности данного фермента используется для оценки обеспеченности организма (ФАД-эффект).
При недостатке рибофлавина отмечается снижение аскорбиновой кислоты вплоть до развития скорбута даже у синтезирующих витамин С собак. На скорбутогенной диете рибофлавин увеличивает время выживания морских свинок и замедляет снижение содержания аскорбиновой кислоты. При недостатке рибофлавина уменьшается уровень ДАК: по-видимому, она разрушается до дикетогулоновой кислоты.
При добавлении рибофлавина к диете без витамина В12, повышалось содержание этого витамина в печени. Считают, что рибофлавин повышает кишечный синтез витамина В12, являясь поставщиком предшественника имидазольной группы нуклеотидной части этого витамина. Показано также, что рибофлавин необходим для превращения витамина В12 в его коферментную форму. Недостаточность рибофлавина предрасполагает к развитию язвенного процесса. Так, в опытах по созданию стрессовых ситуаций язвы желудка возникали у 90 % стрессированных животных с недостаточностью рибофлавина и только у 10 % животных, обеспеченных данным витамином.
Суточная норма потребления рибофлавина в мг.
|
Младенцы Дети Подростки Взрослые Беременные и кормящие Пожилые |
0,4–0,6 0,9–1,4 1,5–1,7 1,5–2,4 1,6–2,3
1,3–1,6 |
Об обеспеченности витамином В2 судят по величине ФАД-эффекта – коэффициента активации витамин В2-зависимого фермента глутатионредуктазы в гемолизате эритроцитов при добавлении экзогенного ФАД. Адекватной обеспеченности витамином В2 соответствует величина ФАД-эффекта менее 1,20, глубокому дефициту – выше 1,30. Кроме того, может быть использован простой, удобный и точный метод определения концентрации рибофлавина в плазме крови с помощью специфического рибофлавинсвязывающего белка из куриного яйца. Оптимальной обеспеченности организма витамином В2 соответствует концентрация рибофлавина выше 10 нгмл, глубокому дефициту – ниже 5 нгмл. Экскреция рибофлавина с мочой, соответствующая нормальной обеспеченности организма составляет 14–30 мкг/час.
Гиповитаминоз. Недостаточность витамина В2 может быть следствием замедления его всасывания из жкт при энтеритах, назначении антибиотиков, дисбактериозе. Может развиваться при фототерапии и детей с гипербилирубинемией, которая увеличивает распад рибофлавина и его элиминацию. Дефицит рибофлавина проявляется ангулярным стоматитом, глосситом и специфической фуксиновой пигментацией языка, десквамацией эпителия у слизисто-кожной границы губ с покраснением, блеском и воспалением, себорейным фолликулярным кератозом в области носогубных складок, носа и лба, дерматитом в области половых органов и чувством жжения подошвенной поверхности. Часто наблюдаются конъюнктивит, блефароспазм, фотофобия, чувство жжения, слезотечение и васкуляризация роговицы со снижением остроты зрения.
Клиническое применение. В медицинской практике используются рибофлавин и коферментные препараты ФМН и ФАД (флавинат). Они употребляются при недостаточности витамина В2, а также при зудящих дерматозах, кератитах, конъюнктивитах, помутнении роговицы, неврастениях, а также как общеукрепляющее средство. Кроме того, рибофлавин употребляется при отравлениях дыхательными ядами (СО), поражении печени, интенсивной мышечной работе. Важен при лечении гипотрофий, гипохромной анемии, дисбактериоза (он необходим для жизнедеятельности нормальной микрофлоры), применяется при гипоксиях. Если возникает необходимость вводить витамин капельно, флакон должен быть обернут черной бумагой. Токсических эффектов при введении больших доз витамина не установлено.
