
4035
.pdf10
ра с обычным железным катализатором и работает под давлением ≈14 МПа. Содержание аммиака на выходе около 19 %.
Второе предложение касается новой системы теплообменного риформинга природного газа – Kellogg Reforming Exchanger System (KRES). При работе агрегата нагретая смесь природного газа и водяного пара поступает одновременно в два реактора: теплообменного и автотермического риформинга. Конвертированный газ из реактора автотермического риформинга с температурой 1000 ÁС поступает в межтрубное пространство теплообменного риформинга. Организация параллельного потока газов в реакторе теплообменного риформинга (внутри – поток газа на риформинг, снаружи – конвертированный газ после автотермического риформинга) снижает перепад давления на катализаторные трубы до 0,2 МПа. При этом открытая конструкция труб снимает последствия от теплового нагрева материала труб и облегчает загрузку и выгрузку катализатора. Содержание метана на выходе из реактора теплообменного риформинга не превышает 0,3 %. Сочетание процессов КААР/KRES при эксплуатации модернизированного агрегата снижает расход энергии на 5–10 % по сравнению с работой традиционного агрегата и расход энергии составляет всего 6,5–6,9 Гкал на тонну получаемого аммиака. Снижаются также и капитальные затраты (на 10 %) за счет использования более простого компрессорного оборудования.
Энергозатраты и себестоимость аммиака можно снизить и за счет других стадий технологии, например, на стадии очистки конвертированного газа от углекислого газа в его составе. Традиционно этот процесс ведут с помощью 20 %-го раствора моноэтаноламина (МЭА). Этот абсорбент обладает рядом достоинств, но есть и недостатки, среди которых высокая коррозионная способность, что не позволяет увеличить концентрацию раствора МЭА, а это в свою очередь увеличивает реакционные объемы жидкости, перекачиваемые насосами, а значит лишние энергозатраты. В настоящее время и за рубежом и на нескольких агрегатах в нашей стране сделана замена МЭА на метилдиэтаноламин (МДЭА). Последний обладает сравнительно низкой коррозионной активностью, что позволяет повысить концентрацию активной составляющей раствора до 45 %. Кроме того, МДЭА обладает очень низкой летучестью, что снижает расход этого вещества
11
на подпитку. Деградация МДЭА тоже значительно ниже, чем у МЭА, а все вместе снижает энергозатраты и себестоимость аммиака.
Все современные технологические схемы работают с помощью восьми различных катализаторов. Катализаторы – это еще один объект пристального внимания технологов, работы по созданию оптимальных составов катализаторов всех стадий продолжаются до сих пор. Особенно это касается наиболее дорогих катализаторов медь- и никельсодержащих, которые к тому же очень чувствительны к ядам.
2. Получение неконцентрированной азотной кислоты
Основная масса получаемого аммиака идет для переработки в азотную кислоту, производство которой во всем мире ежегодно прирастает. В отличие от получения аммиака в производстве разбавленной азотной кислоты не сложился ©классический° вариант технологии. Производства азотной кислоты прежде всего делят на агрегаты под единым давлением и агрегаты комбинированной схемы. Имеется в виду, что давление на стадиях конверсии аммиака и абсорбции оксидов азота может быть одинаковым, а может быть разным.
Мощности агрегатов тоже сильно различаются и могут составлять от 50 до 360 тыс. т/год и выше.
В связи с высокой токсичностью оксидов азота особое внимание в технологии отводится очистке выхлопных газов. Решается эта проблема по-разному. Имеются системы высокотемпературной каталитической очистки, потребляемые природный газ в качестве восстановителя, есть системы с низкотемпературной селективной каталитической очисткой, использующие аммиак, а есть агрегаты, работающие без специальной очистки, и при этом концентрация оксидов в выбросах не превышает санитарные нормы. В свою очередь способ очистки выхлопных газов влияет на энергетическое оформление агрегата. Но есть и общие принципы технологии:
–в качестве исходного вещества используют аммиак;
–применение металлов платиновой группы как катализаторов окисления аммиака;
12
– в основу агрегатов положен энерготехнологический принцип.
У нас в стране в настоящее время работают установки под единым давлением 0,716 МПа мощностью 120 тыс. т/год азотной кислоты и агрегаты АК-72 комбинированной схемы мощностью 360-380 тыс. т/год. Обе технологии разработаны и внедрены ГИАП.
Из зарубежных следует отметить французскую фирму Сосьете Шимик де ла Гранд Паруасс, создавшую ряд установок производства азотной кислоты (60 %-й) по комбинированной схеме такой же мощности, что и АК-72. Эти установки характеризуются отсутствием потребления природного газа, замкнутым энергетическим балансом и отсутствием специальной очистки выхлопных газов.
ГИАП и фирма Гранд Паруасс совместно разработали агрегат по комбинированной технологической схеме мощностью 360 тыс. т/год с низкотемпературной каталитической очисткой выхлопных газов и замкнутым энергетическим балансом.
3. Производство серной кислоты
Серная кислота является одним из основных продуктов химической промышленности и занимает одно из первых мест среди химических веществ. Серная кислота – наиболее сильная и самая дешевая из кислот. Она широко используется в производстве минеральных удобрений, различных солей, всевозможных органических продуктов, красителей, взрывчатых веществ, в нефтяной, металлургической, текстильной промышленности, применяется в качестве осушающего средства, в процессах нейтрализации, травления и для других целей.
Увеличение выпуска серной кислоты сопровождается усовершенствованием ее технологии и аппаратурного оформления. При этом значительно возросла степень использования серосодержащего сырья, снизились условные капитальные вложения и эксплуатационные затраты, единичные мощности сернокислотных систем повысились со 120 до 360 тыс. т/год при работе на колчедане и со 100 до 500 и более тыс. т/год на сере.
Источниками сырья для производства серной кислоты являются руды самородной элементарной серы; сернистые соеди-
13
нения металлов, в том числе колчеданы; сернистые соединения природных горючих газов, нефти и угля; сульфаты; серосодержащие отходы различных производств.
Наибольшее распространение в нашей стране и за рубежом получил контактный метод, позволяющий получить серную кислоту высокой концентрации и олеум.
Менее распространен нитрозный метод, в котором процесс окисления диоксида серы осуществляется при помощи нитрозы – серной кислоты с растворенными в ней оксидами азота, являющимися переносчиками кислорода.
Контактный метод производства серной кислоты включает следующие основные стадии:
–получение SO2-содержащего газа (печное отделение);
–очистка газа от примесей (промывное отделение);
–окисление диоксида серы в серный ангидрид SO3 на катализаторе (контактное отделение);
–абсорбция серного ангидрида (абсорбционное отделение). При обжиге серосодержащего сырья выделяется значитель-
ное количество тепла вследствие протекания экзотермических процессов. Поэтому для его утилизации печное отделение сернокислотного производства оборудуют котлами-утилизаторами для получения перегретого пара либо используют энерготехнологические агрегаты, сочетающие печь и котел-утилизатор.
Конверсию SO2 в SO3 осуществляют в контактных аппаратах, содержащих для достижения высокой степени превращения 4-5 слоев катализатора марок СВС, СВД, ИК на основе соединений ванадия. В последние годы внедряют и более эффективные ванадиевые катализаторы с цезиевым промотором.
Контактное отделение функционирует по технологической схеме ОК (одинарное контактирование) или ДК (двойное контактирование), выбор которой зависит от качества применяемого сырья, способов отвода тепла реакции, производительности установки, заданной степени превращения и других факторов.
При использовании схемы ОК SO2-содержащий газ проходит все слои катализатора с промежуточным охлаждением в теплообменниках, после чего направляется на абсорбцию образовавшегося SO3. Степень превращения SO2 при этом достигает 98,0–98,5 %.
14
Процесс окисления SO2 по схеме ДК осуществляется в две стадии: на первой стадии газ, пройдя часть слоев катализатора контактного аппарата, поступает на абсорбцию для выделения из него SO3. После этого газ, содержащий неокисленную часть SO2, направляется на вторую стадию контактирования и проходит последние слои катализатора. При этом степень превращения на первой стадии катализа обычно составляет 93–95 %, на второй – 95–97 %, а общая – 99,5–99,8 %, что значительно повышает эффективность производства и снижает содержание диоксида серы в выхлопных газах.
Абсорбцию SO3 осуществляют в олеумных и моногидратных абсорбентах, которые орошаются 20 %-м олеумом и концентрированной 98,3 %-й серной кислотой. Отходящий газ, пройдя брызгоуловитель, поступает в очистную установку для поглощения SO2 сульфитно-содовым раствором.
Дальнейшее техническое развитие производства ведется в следующих направлениях: разработка метода получения серной кислоты из концентрированного газа (до 50–70 % SO2), проектирование мощных систем, работающих под давлением и с применением технического кислорода. Окисление концентрированного газа из-за высокого удельного тепловыделения осложняет отвод тепла из зоны реакции в агрегатах с фильтрующими слоями катализатора. В связи с этим предложено на первой ступени конверсии SO2 использовать контактный аппарат с одним кипящим слоем износоустойчивого катализатора.
При совершенствовании производства большое внимание уделяется снижению металлоемкости агрегатов и расхода электроэнергии, использованию вторичных энергоресурсов, уменьшению выбросов в атмосферу вредных веществ с выхлопными газами и созданию практически безотходных сернокислотных систем.
15
ВАРИАНТЫ КОНТРОЛЬНЫХ РАБОТ
Вариант № 1
1.Сероочистка природного газа, используемого для конверсии в производстве аммиака. Назначение стадий, химические реакции, равновесие и кинетика процесса гидрирования, технологические параметры и катализаторы.
2.Основные стадии производства серной кислоты контактным методом. Физико-химические основы горения серы: химические реакции, энтальпия процесса, факторы, влияющие на скорость окисления серы.
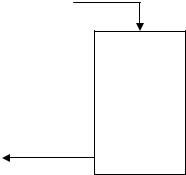
3.Рассчитать материальный баланс контактного аппарата производства азотной кислоты. Исходные данные: производительность агрегата 4800 кг/ч (100 % НNO3); выход по окислению аммиака ηк = 0,975, выход по абсорбции ηа = 0,985; содержание аммиака в аммиачно-воздушной смеси (АВС) 10,5 %; содержание водяных паров в воздухе после промывки 4,60 % (по объему).
АВС
нитрозные
газы
Вариант № 2
1.Риформинг природного газа в производстве аммиака, уравнения реакций и условия их осуществления в производстве. Технологический режим I ступени конверсии.
2.Основные стадии производства серной кислоты и олеума контактным методом. Физико-химические основы обжига серного колчедана: химические реакции и энтальпия, факторы, влияющие на скорость горения серного колчедана. Оптимальные условия процесса.

16
3. Рассчитать материальный баланс контактного аппарата производства азотной кислоты. Исходные данные: производительность агрегата 6400 кг/ч (100 % НNO3), выход по окислению аммиака ηк = 0,970, выход по абсорбции оксидов ηа = 0,985. Содержание аммиака в аммиачно-воздушной смеси 9,5 %, содержание водяных паров в воздухе после промывки водой 4,42 % (по объему).
АВС
нитрозные
газы
Вариант № 3
1.Промышленные способы получения водорода. Достоинства и недостатки их. Значение каждого способа в современных технологиях.
2.Обжиг серосодержащего сырья: физико-химические основы обжига серы и серного колчедана.
3.Рассчитайте материальный баланс абсорбционной колонны производства азотной кислоты. Исходные данные: давление в
колонне 1,16 МПа, степень превращения оксидов азота α = 0,98. Состав нитрозного газа на входе в колонну:
газ |
NO2 |
NO |
O2 |
N2 |
H2O |
%, об. |
6,17 |
0,25 |
3,88 |
89,03 |
0,67 |
Производительность агрегата 1150 т/сут 100 %-й HNO3. Давление паров воды над 60 %-й HNO3 при 30 ÅС составляет 1,37.103 Па. Из промывной колонны в виде конденсата в абсорбционную колонну поступает 453 т/сут HNO3 (в пересчете на 100 %) в виде 40 %-го конденсата HNO3.

17
газ на каталитическую очистку
вода
конденсат HNO3
нитрозный
газ
60 %-ная HNO3
Вариант № 4
1.Технологический режим II ступени конверсии природного газа. Назначение II ступени, катализаторы и основной аппарат II ступени конверсии.
2.Состав газа при обжиге серосодержащего сырья. Как осуществляют очистку обжигового газа от пыли и тумана?
3.Рассчитайте материальный баланс абсорбционной колонны производства азотной кислоты. Исходные данные: производи-
тельность агрегата 980 т/сут 100%-й HNO3; давление паров воды над 60%-й HNO3 составляет 1,37.103 Па при 30 ÅС; из промывной колонны в виде 40%-го конденсата в абсорбционную колонну поступает 386 т/сут HNO3 (в пересчете на 100 %); давление в ко-
лонне 1,16 МПа; степень превращения оксидов азота α = 0,985. Состав нитрозного газа на входе в колонну:
газ |
NO2 |
NO |
O2 |
N2 |
H2O |
%, об. |
6,17 |
0,25 |
3,88 |
89,03 |
0,67 |
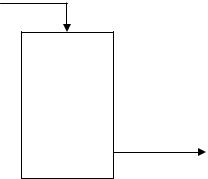
газ на каталитическую очистку
вода
конденсат HNO3
нитрозный
газ
60 %-ная HNO3
18
Вариант № 5
1.Конверсия оксида углерода (II) водяным паром в производстве аммиака, назначение стадии, особенности технологических параметров первой ступени конверсии, катализаторы.
2.Сорта серной кислоты. Как осуществляют хранение, разливку и перевозку серной кислоты? Каковы мероприятия, обеспечивающие технику безопасности при работе с серной кислотой
иолеумом?
3.Рассчитайте материальный баланс контактного аппарата производства азотной кислоты. Исходные данные: производительность агрегата 5200 кг/ч 100%-й кислоты; выход по окисле-
нию аммиака ηк = 0,97, выход по абсорбции оксидов азота ηа = 0,98. Содержание аммиака в АВС (аммиачно-воздушная смесь) 9,8 %. Содержание водяных паров в воздухе после промывки его водой 4,3 % (концентрации газов даны по объему).
АВ
Нитрозные газы
Вариант № 6
1.Стадия очистки конвертированного газа производства аммиака от диоксида углерода. Объясните необходимость этой стадии, укажите особенности процесса хемосорбции, достоинства
инедостатки моноэтаноламина и метилдиэтаноламина как сорбентов.
2.Производство серной кислоты нитрозным методом. Теоретические основы процесса, схема и технологический режим башенных систем.
3.Рассчитайте материальный баланс контактного аппарата производства азотной кислоты. Исходные данные: производи-
19
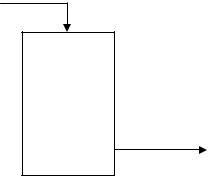
тельность агрегата 1100 т/сут 100%-й HNO3; выход по окислению аммиака ηк = 0,972, выход по абсорбции оксидов азота ηа = 0,985; содержание аммиака в аммиачно-воздушной смеси (АВС) 10 %, содержание водяных паров в воздухе после промывки его водой 4,3 % (концентрации газов даны по объему).
АВС
нитрозные
газы
Вариант № 7 1. Назначение стадии метанирования оксидов углерода в
производстве аммиака. Какие реакции описывают этот процесс; какие катализаторы обеспечивают скорость реакции? Укажите параметры стадии, принципиальную технологическую схему и конструкционные особенности основного оборудования.
2. Контактное отделение сернокислотного производства: принципиальная схема отделения и конструкционные особенности контактных аппаратов с промежуточным охлаждением между слоями.
3. Рассчитайте материальный баланс абсорбционной колонны производства неконцентрированной азотной кислоты.
Исходные данные: производительность агрегата 820 т/сут 100 % НNO3; давление в колонне 1,16 МПа; давление паров воды над 60 % НNO3 при 30 ®С составляет 1,37Æ103 Па; из промывной колонны в абсорбционную колонну поступает 323 т/сут (в пересчете на 100 % НNO3) НNO3 в виде 40%-го конденсата НNO3. Степень превращения оксидов α = 0,983. Состав нитрозного газа на входе в колонну:
газ |
NO2 |
NO |
O2 |
N2 |
H2O |
%, об. |
6,20 |
0,23 |
3,85 |
89,04 |
0,68 |
