
- •Содержание:
- •Тема №1: Строение металлических сплавов.
- •1.1. Фаза металлических сплавов.
- •1.2. Понятие диаграммы состояния сплава.
- •1.3. Построение диаграмм состояния термическим методом.
- •Тема №2: Основные типы диаграмм состояния двух компонентных сплавов.
- •2.1. Диаграммы состояния для сплавов с неограниченной растворимостью компонентов в твёрдом состоянии.
- •2.2. Правило отрезков.
- •2.3. Диаграмма состояния для сплавов образующие механические смеси из чистых компонентов.
- •2.4. Диаграммы состояния для сплавов с ограниченной растворимостью компонентов в твёрдом состоянии.
- •2.5. Диаграммы состояния для сплавов компоненты которых образуют химическое соединение.
- •2.6. Диаграммы состояния для сплавов, компоненты которых испытывают полиморфные превращения.
- •Тема №3: Диаграмма состояния железо-углеродистых сплавов.
- •3.1. Структурные составляющие сплавов железа с углеродом.
- •3.2. Диаграмма состояний железоуглеродистых сплавов.
- •3.3 Фазовые превращения в сталях.
- •3.4. Фазовые превращения в чугунах.
- •Тема №4: Углеродистые стали и чугуны.
- •4.1. Общая характеристика и получение сталей и чугунов.
- •4.2. Влияние углерода и постоянных примесей на структуру и свойства углеродистых сталей.
- •4.3. Классификация и маркировка углеродистых сталей.
- •4.4. Микроструктура и свойства чугунов.
- •4.5. Образование графитных включений в чугунах.
- •Тема №5: Теоретические основы термической обработки.
- •5.1. Общие сведения по теоретической обработке сталей.
- •5.2. Образование аустенита из перлита при нагреве углеродистых сталей.
- •5.3. Превращение аустенита в перлит при равновесном охлаждении сплава. Диаграмма изотермического распада аустенита.
- •5.4. Мартенситное превращение аустенита.
- •5.5. Превращения при отпуске закалённых сталей.
- •Тема №6: Технология термообработки углеродистой стали.
- •6.1. Отжиг и нормализация.
- •6.2. Закалка и отпуск углеродистых сталей.
Содержание:
Стр.
Тема №1: Строение металлических сплавов. 3
1.1. Фаза металлических сплавов. 4
1.2. Понятие диаграммы состояния сплава. 5
1.3. Построение диаграмм состояния термическим методом. 6
Тема №2: Основные типы диаграмм состояния двух компонентных сплавов. 7
2.1. Диаграммы состояния для сплавов с неограниченной растворимостью компонентов в твёрдом состоянии. 7
2.2. Правило отрезков. 8
2.3. Диаграмма состояния для сплавов образующие механические смеси из чистых компонентов. 9
2.4. Диаграммы состояния для сплавов с ограниченной растворимостью компонентов в твёрдом состоянии. 11
2.5. Диаграммы состояния для сплавов компоненты которых образуют химическое соединение. 15
2.6. Диаграммы состояния для сплавов, компоненты которых испытывают полиморфные превращения. 16
Тема №3: Диаграмма состояния железо-углеродистых сплавов. 17
3.1. Структурные составляющие сплавов железа с углеродом. 18
3.2. Диаграмма состояний железоуглеродистых сплавов. 19
3.3 Фазовые превращения в сталях. 20
3.4. Фазовые превращения в чугунах. 22
Тема №4: Углеродистые стали и чугуны. 24
4.1. Общая характеристика и получение сталей и чугунов. 24
4.2. Влияние углерода и постоянных примесей на структуру и свойства углеродистых сталей. 25
4.3. Классификация и маркировка углеродистых сталей. 26
4.4. Микроструктура и свойства чугунов. 27
4.5. Образование графитных включений в чугунах. 28
Тема №5: Теоретические основы термической обработки. 29
5.1. Общие сведения по теоретической обработке сталей. 29
5.2. Образование аустенита из перлита при нагреве углеродистых сталей. 30
5.3. Превращение аустенита в перлит при равновесном охлаждении сплава. Диаграмма изотермического распада аустенита. 31
5.4. Мартенситное превращение аустенита. 33
5.5. Превращения при отпуске закалённых сталей. 33
Тема №6: Технология термообработки углеродистой стали. 34
6.1. Отжиг и нормализация. 34
6.2. Закалка и отпуск углеродистых сталей. 35
Материаловедение – это наука о некоторых материалах, широко используемых в современной технике (металлы и сплавы).
Основной задачей материаловедения является установление взаимосвязи между составом, структурой и свойствами материала, а так же разрабатывания путей целенаправленного взаимодействия на эти свойства (стали и чугуны).
Тема №1: Строение металлических сплавов.
Сплавами называются вещества, получаемые сплавлением двух и более элементов.
Элементы сплавов принято называть компонентами. Компоненты сплавов, взаимодействуя друг с другом образуют те или иные фазы.
Фаза – это однородная часть сплава, обладающая своим собственным составом, структурой, свойствами и отделённая от других частей сплава поверхностью раздела или границей. Фазы могут быть жидкими или твёрдыми. В сплаве могут существовать одна, две и больше фаз. Число фаз и их тип определяет состояние сплава.
1.1. Фаза металлических сплавов.
Если основу сплава составляет металлы и сплав обладает ярко выраженными металлическими свойствами (металлический блеск, высокая электро и теплопроводностью и пластичностью), то такие сплавы называются металлическими. В металлических сплавах могут быть образованы следующие фазы: различные жидкие растворы компонентов, в чистом состоянии, а так же твёрдые растворы компонентов.
В жидком расплавленном состоянии компоненты металлических сплавов, обычно образуют неограниченные жидкие растворы (т.е. в любых соотношениях растворяются друг в друге). В таком случае сплав является однородным, однофазным и состоит только из одного жидкого раствора. В редких случаях компоненты растворяются друг в друге ограниченно или совсем не растворяются. Тогда сплав будет состоит из двух частей, а точнее из двух не смешивающихся слоёв (если сплав двух компонентный). Верхний слой образует менее тонкий компонент. В твёрдом состоянии компоненты сплавов могут образовывать химические соединения, либо растворяться друг в друге, либо выделяться в чистом виде.
Если сплав двух компонентный, то химическое соединение, образующееся в сплаве в общем случае может быть записано: An Bm. Где A и B − компоненты сплава, n и m − целые числа.
В химическом соединении наблюдается определённое соотношение компонента, которое отображает его химическая формула. В одном сплаве может образовываться несколько химических соединений с различной формулой: AB2; A2B3 …. Химическое соединение имеет свою собственную структуру и свойства, отличные от структуры и свойств компонентов, образующих это соединение (Fe3C - цементит). Если компоненты A и B растворяются друг в друге в твёрдом состоянии, то тогда в сплавах наблюдается образование различных твёрдых растворов (A(B), B(A)).
В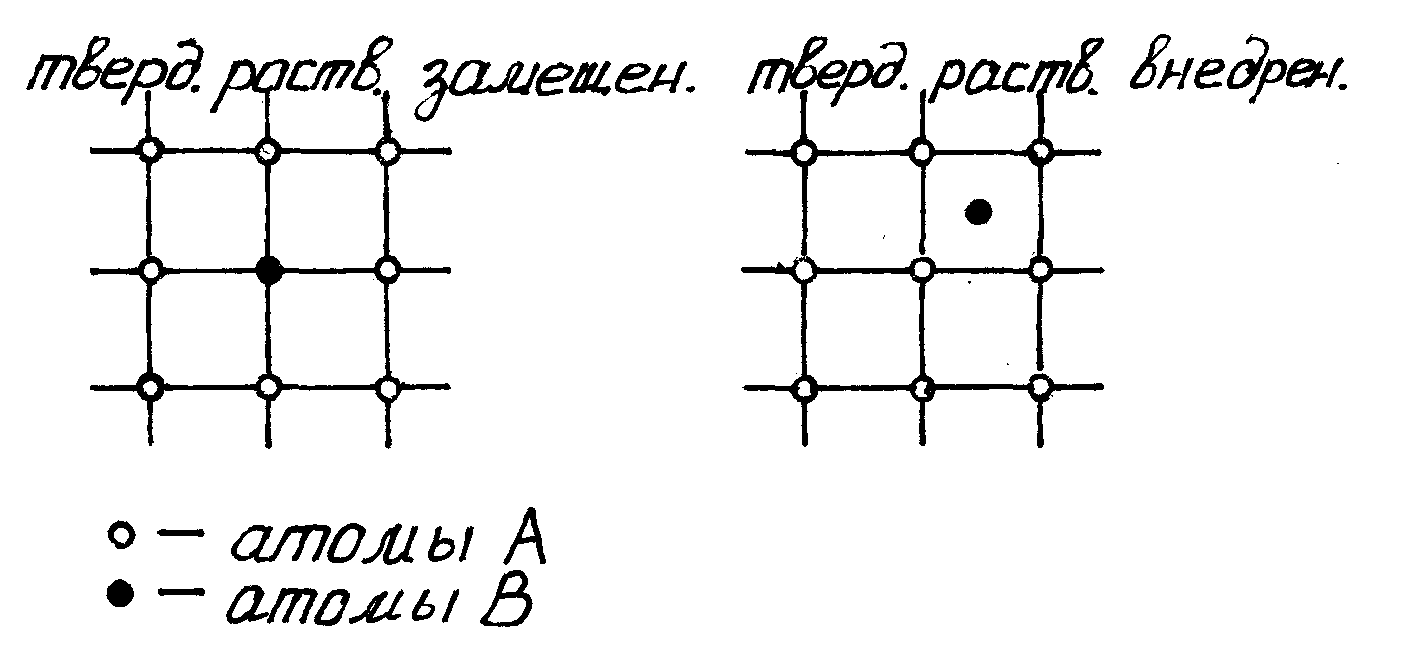 первом случае:A
− растворитель,
B
− растворённое
вещество. Во втором случае всё наоборот.
В общем случае:
первом случае:A
− растворитель,
B
− растворённое
вещество. Во втором случае всё наоборот.
В общем случае:
![]() .
.
При образовании твёрдых растворов, у фазы сохраняется кристаллическая структура компонента растворителя. Возможны два типа твёрдых растворов: твёрдые растворы замещения и твёрдые растворы внедрения.
При образовании твёрдого раствора замещения, атомы растворителя компонента замещают атомы растворителя в узлах его кристаллической решётки. При образовании твёрдого раствора внедрения, атомы растворённого компонента размещаются в порах или междоузлиях кристаллической решётки компонента растворителя.
Твёрдые
растворы замещения чаще всего образуют
элементы, чей атомные радиус меньше
атомного радиуса элемента растворителя.
Например, углерод и азот, растворяясь
в железе образуют твёрдый раствор
внедрения. Растворённые атомы всегда
искажают кристаллическую решётку
компонента растворителя. При некоторой
концентрации растворённых атомов эти
искажения могут достичь своего придельного
значения, что ведёт к ограничению
растворимости. Твёрдые растворы внедрения
всегда ограничены. Максимальная
концентрация растворённых атомов в них
не превышает 1−2%. Твёрдые растворы
замещения могут быть как ограниченные,
так и не ограниченные. Не ограниченные
растворы образуются в том случае, если
оба компонента имеют одинаковый тип
кристаллической решётки, близкий атомный
радиус и свойства. Например, золото и
платина имеют ГЦК решетку и близкие
свойства, поэтому не ограничено
растворяются друг в друге. В этом случае:
![]() .
Твердые растворы могут образовываться
не только на базе чистых компонентов,
но и на базе химических соединений. В
таком случае химические соединения
выступают в роле растворителя, в которых
растворяется какой-то третий компонент
.
Твердые растворы могут образовываться
не только на базе чистых компонентов,
но и на базе химических соединений. В
таком случае химические соединения
выступают в роле растворителя, в которых
растворяется какой-то третий компонент![]()
Например:
![]() -
это раствор хрома, азота, углерод.
-
это раствор хрома, азота, углерод.
Е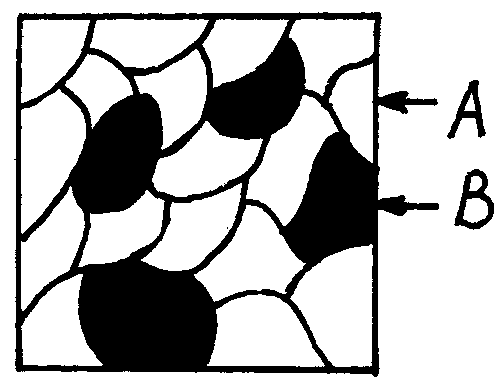 сли
компонентыA
и B
не растворяются друг в друге в твёрдом
состоянии и химически не взаимодействуют
друг с другом, то тогда наблюдается
образование двух фаз чистых компонентов,
находящихся в твёрдом состоянии. В этом
случае микроструктура сплава представляет
собой механическую смесь зёрен или фаз
чистого компонента A
и чистого компонента B.
сли
компонентыA
и B
не растворяются друг в друге в твёрдом
состоянии и химически не взаимодействуют
друг с другом, то тогда наблюдается
образование двух фаз чистых компонентов,
находящихся в твёрдом состоянии. В этом
случае микроструктура сплава представляет
собой механическую смесь зёрен или фаз
чистого компонента A
и чистого компонента B.
Здесь каждое зерно это чистый компонент A и чистый компонент B.
Свойства всего сплава в целом определяется простой суммой свойств A и B пропорционально их количеству.
