
- •1. Изохорный процесс изменение состояния идеального газа.
- •4. Адиабатный пр-с изм сост ид газа.
- •7. PV диаграмма водяного пара.
- •12. Изобарный пр-с изм сост водяного пара.
- •13. Изотермический пр-с изм сост водяного пара.
- •17. Цикл Карно во влажном воздухе и его недостатки. Pv,ts диаграммы
- •18. Цикл Ренкина. Схема. Диаграммы.
- •19. Полезная работа цикла Ренкина. Работа питательного насоса. Термический кпд цикла Ренкина.
- •20. Влияние параметров пара на термодинамический кпд цикла Ренкина.Ts ,hS диаграммы.
- •21.Цикл Ренкина с промежуточным перегревом пара.
- •22.Принципиальная схема действующей тэц.
- •26. Принципиальная схема прямоточных котлов.
- •27. Принципиальная схема современного парового котла. Ее работа.
- •28 Цикл паровой компрессорной хол уст-ки
- •29 Абсорбционные хол уст-ки
- •30 Источники геотермальной энергии
- •31 ГеоТэс на сухом паре
- •32 ГеоТэс с бинарным циклом
- •34 Солнечное излучение
- •35 Солнечн эл ст башенного типа с т/д циклом
- •36 Солн эл ст с пцк солн излучения
- •37 Накопитель солн энергии, осн на синтезе аммиака
- •38 Солн фотоэл-кие преобразователи
- •39 Энергия с косм электростанций
- •41.Принципиальная схема одноконтурной аэс, ее работа. Достоинства и недостатки.
- •42.Принципиальная схема двухконтурной аэс, ее работа.
- •43.Принципиальная схема энергоблока рбмк – 1000, описание ее работы.
- •44.Физические основы работы пэс. Преимущества и недостатки пэс, их воздействие на окружающую среду.
- •45.Состояние и перспективы использования пэс.
- •46.Физические основы работы океанических гидроэлектростанций на основе морских течений. Основные типы турбин, требования к ним предъявляемые.
- •47.Преобразование энергии морских течений в электрическую энергию. Схема роторной электростанции. Достоинства и недостатки огэс.
- •48.Состояние и перспективы огэс.
- •49.Назначение гидроэнергетической установки, основные типы.
- •50.Основные схемы использования водной энергии. Их принципиальные схемы.
- •51.Физические основы работы ветроэнергетических установок. Величина мощности, развиваемой потоком воздуха. Основные направления развития ветроэнергетики.
- •52.Классификация вэу. Характерные рабочие скорости ветра. Энергетические характеристики вэу.
- •53.Технико-экономические показатели вэс в России и зарубежных странах. Экономическая эффективность и экологичность вэс.
1. Изохорный процесс изменение состояния идеального газа.

Для получения значения энергии запишем 1ое начало термодинамики.

T-S
диаграмма используется для определения
количества подведенного или отведенного
тепла. Т.к Т2>Т1 в процессе 1-2, то тепло
подводится, если Т2<Т1 то тепло отводится.
Кол-во подведенного и отведенного тепла
определяется как площадь под кривой
1-2. Удельная располагаемая работа
обозначается
![]() .
.
Изменение удельной энтропии найдем из 1го и 2ого Н Т/Д.

Количество полной теплоты идет на изменение энергии.
2. Изобарный процесс изм сост ид газа. р=соnst, dp=0



Часть теплоты подведенной к рабочему телу идет на изменение внутренней энергии, а часть на совершение работы.

При изобарном процессе 28,5% всей подведенной теплоты расходуется на совершение работы, 71,5%-идет на изменение внутренней энергии тела.
![]() Теплота
подведенная к рабочему телу идет на
увелич энтальпии, а кол-во подведенной
теплоты определяется как площадь под
кривой на TS
– диаграмме.
Теплота
подведенная к рабочему телу идет на
увелич энтальпии, а кол-во подведенной
теплоты определяется как площадь под
кривой на TS
– диаграмме.
Изменение энтропии.
Т.к. Ср>Сv , то изменение энтропии при изобарном процессе будет больше чем при изохорном. Изобара 1-2 при одинаковой температуре Т1 и Т2 более пологая чем изохора 1,2’.

3. Изотермический пр-с изм сост ид газа. Т=const. dT=0



В изотермическом пр-се идеальная работа газа, располагаемая работа, изменение объема и удельное количество теплоты равны между собой.
Изменение энтропии:

4. Адиабатный пр-с изм сост ид газа.
Адиабатным процессом наз пр-с происходящий без теплообмена с окруж средой.


Первое Н Т/Д:

Адиабата идет круче чем изотерма.
![]()
В адиаб пр-се работа совершается за счет убыли внутр энергии рабочего тела.
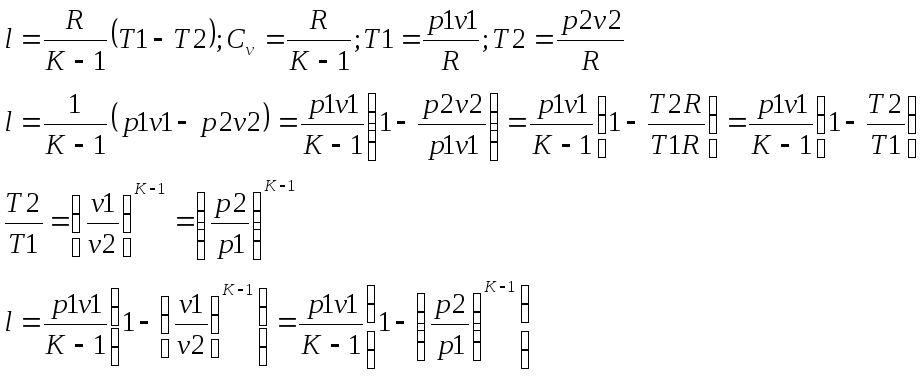
Располагаемая
работа l0
для адиаб пр-са в К раз больше удельной
работы расширения газа и противоположна
ей по знаку.
![]()
Из ур-я адиабаты видно, т.к. K>1, то адиабата идет круче чем изотерма. Т.к. адиабата идет круче чем изотерма то адиаб пр-с идет без теплообмена с окр средой и расширение газа происходит только за счет падения ее внутр энергии, в изотерм пр-се расширение газа происходит за счет подведения теплоты. Если от т А сжать газ, то адиабата А1 располагается круче изотермы А1’, т.к. при адиабатном пр-се теплота не отводится и температура газа с увеличением давления растет больше чем в изотермическом пр-се.
5. Политропный пр-с – прс-с в котором удельная теплоемкость остается постоянной. График процесса политропы – это кривая которая описывает газовые пр-сы, в кот-ых происходит изменение всех термодинамических параметров.
Кол-во подведенной
теплоты:

Если n=![]() то
v=сonst;
n=0
– p=const;
n=1
– T=const;
n=k
– уравнение адиаб пр-са S=const.
Политропный пр-с обобщает все раннее
рассмотренные пр-сы.
то
v=сonst;
n=0
– p=const;
n=1
– T=const;
n=k
– уравнение адиаб пр-са S=const.
Политропный пр-с обобщает все раннее
рассмотренные пр-сы.
Соотношение
параметров. Заменим
показатель адиабаты на показатель
политропы. Получим,
![]()
Работа в политропном
пр-се. Для работы в политропном пр-се
используется выражение работы в адиаб
пр-се заменим K
на n.

Располагаемая
работа l0
в n
раз больше удельной работы:
![]()
Теплоемкость:
![]()

Пр-сы начинающиеся в т А и проходящие с расширением рабочего тела имеют положительную работу. Пр-сы в области 5,6,7,8 имеют отрицат работу, т к рабочее тело в этих областях сжимается. Для 1,2,3,8 проходят при подводе теплоты, а в области 4,5,6,7 – с отводом теплоты. Пр-сы происходящие во 2ой, 7,8 сопровожд повышением температуры раб тела. 3,5,6,4 – температура понижается. 3 – при подводе теплоты происходит падение температуры раб тела, 7 – происходит повыш темпер, при отводе теплоты к раб телу.
Вывод изменения энтропии:
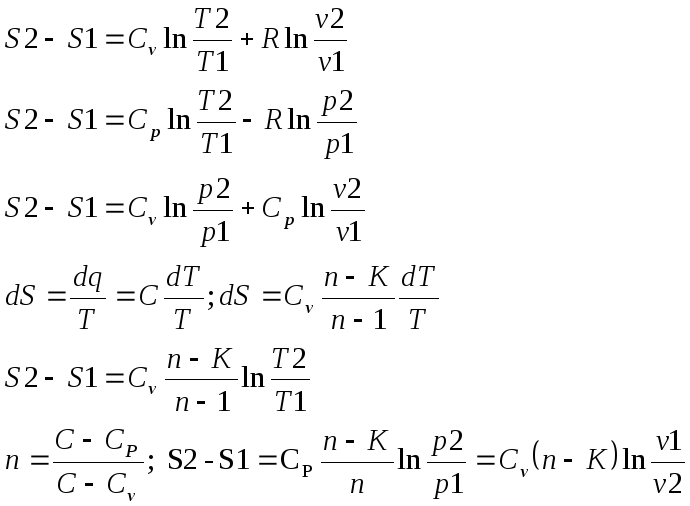
6. Термодинамическая фазовая рТ-диаграмма. Все прямые фазовые переходы требуют подвода теплоты и происходят при постоянном давлении и постоянной температуре. Переход из одного агрегатного состояния в другое принято рассматривать на РТ-диаграмме. Если взять в кач-ве независимого параметра Т, то есть три линии:
p=f1(T)-AK – соответ. равновесному состоянию Ж и Г фазы- испарение
p=f2(T)-AC
p=f3(T)-AB.
Эти линии представляют геометрич место точек
в которых находится в равновесном состоянии
любая пара из 3х агрегатных состояний.
АС-соответствует равновесному состоянию
Т и Г фазы (сублимация по прямому пр-су)-
десублимация.
АВ-соответ равновесному состоянию Т и Ж фазы –
плавление (кристаллизация)
Температура при котором происходит переход из Твердого состояния в Ж – Тпл, Ткрист.
Кол-во теплоты
подведенное в этом пр-се – теплота
плавления (кристаллиз). Температура
перехода в-ва из Ж в Г – Ткип, (Тконд).
Теплота в этом пр-се которое выделяется
или поглощается – теплота парообразования
или теплота конденсации. Температура
из Т в Пар – температура сублимации.
Теплота подведенная или отведенная
назыв теплотой сублимации. Кривая на
которых происходит в зависимости от
давления и температуры переход из Ж
состояния в Г заканчивается в точке К
– это критическая точка. В т К исчезает
физическое различие между жидким и
газообразным состоянием в-ва, а точнее
плотности пара водяной смеси равной
плотности жидкости. Критическое давление
– Рк = 22,12 МПа, Тк = 374,16 С. Все три кривые
пересекаются в т А которая наз тройной
точкой. В этой точке исчезает различие
между тремя фазами Т Ж Г. Изобарная
теплоемкость для фазового перехода
равна бесконечности.
![]()
Коэффициент
изобарного (объемного) расширения:
![]()
Коэффициент
изотермического сжатия:
![]()
![]()
Уравнение Клайперона-Клазиуса связывает температуру, давление, удельный объем с теплотой фазового перехода
![]() ,
где
,
где ![]() -произведение от
давления по температуре взятое на кривой
фазового перехода,
-произведение от
давления по температуре взятое на кривой
фазового перехода, ![]() -теплота фазового
перехода, dT
– температура фазового перехода, v′′-
удельный объем пара, v′-
удельный объем жидкости или твердого
тела. В общем виде ур-е характеризуется
изменением давления фаз находящихся в
равновесии от Т. Для плавления (линия
АВ):
-теплота фазового
перехода, dT
– температура фазового перехода, v′′-
удельный объем пара, v′-
удельный объем жидкости или твердого
тела. В общем виде ур-е характеризуется
изменением давления фаз находящихся в
равновесии от Т. Для плавления (линия
АВ):![]() -
удельная теплота плавления, v′-удельный
объем тв тела; Для парообразования (АК):
q
–удельная теплота парообразования, Т
– удельная температура парообразования,
v′-удельный
объем жидкости; При сублимации (АС) – q
–удельная теплота сублимации, Т –
температура сублимации, v′-
удельный объем тв тела. С помощью этого
ур-я можно установить наклон линии
плавления, парообразования, сублимации
в тройной точке
-
удельная теплота плавления, v′-удельный
объем тв тела; Для парообразования (АК):
q
–удельная теплота парообразования, Т
– удельная температура парообразования,
v′-удельный
объем жидкости; При сублимации (АС) – q
–удельная теплота сублимации, Т –
температура сублимации, v′-
удельный объем тв тела. С помощью этого
ур-я можно установить наклон линии
плавления, парообразования, сублимации
в тройной точке
![]() -
для всех в-в кроме воды. Проведенные
касательные к А для 3-х линий: АК, АВ, АС.
α1, α2, α3 – углы наклона касательной
кривой. АВ, АК и АС в т.А к оси Т <90˚ .v′′-
v′
<0 для всех
в-в. Для воды
-
для всех в-в кроме воды. Проведенные
касательные к А для 3-х линий: АК, АВ, АС.
α1, α2, α3 – углы наклона касательной
кривой. АВ, АК и АС в т.А к оси Т <90˚ .v′′-
v′
<0 для всех
в-в. Для воды ![]() <
0 и поэтому α4>90˚. Для всех нормальных
жидкостей для которых разница > 0 все
линии фазового перехода отклонены
вправо. А для воды с повышенным давлением
линия отклонена не вправо, а влево.
<
0 и поэтому α4>90˚. Для всех нормальных
жидкостей для которых разница > 0 все
линии фазового перехода отклонены
вправо. А для воды с повышенным давлением
линия отклонена не вправо, а влево.
