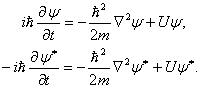Атомка1
.doc|
1.Атомные спектры. Комбинационный приницп.
|
2.Классическая модель атома.Модель Томсона.
оква |
|
|
3.Опыты Резерфорда по рассеянию альфа-частиц.
|
4.Формула Резерфорда.Ядерная модель атома.
|
|
|
5.Теория атома Бора.
|
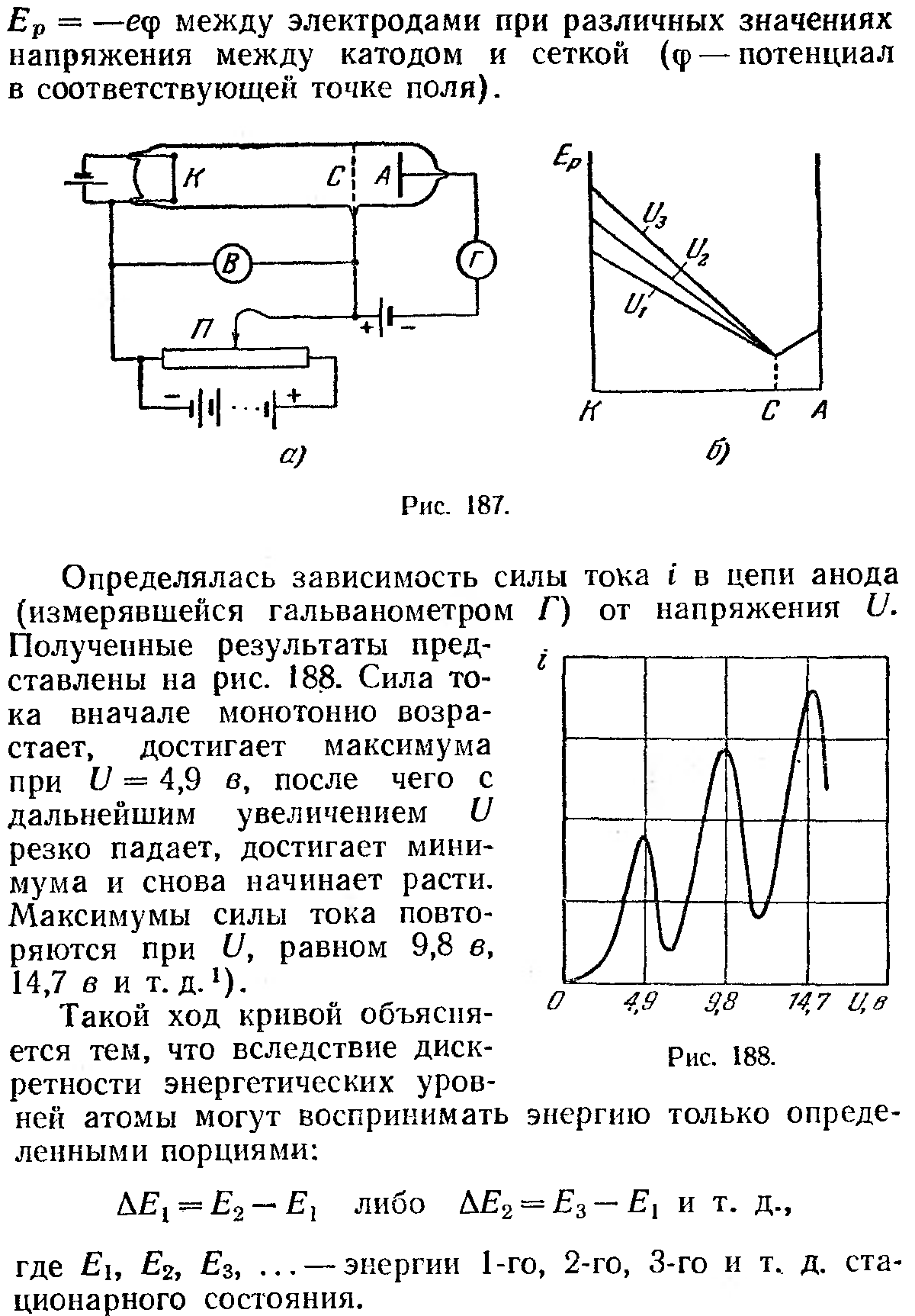
8.Опыты Франка и Герца.
|
|
|
6.Водородоподобные атомы по Бору.
|
7.Уровни энергии атома водорода и способы их возбуждения.
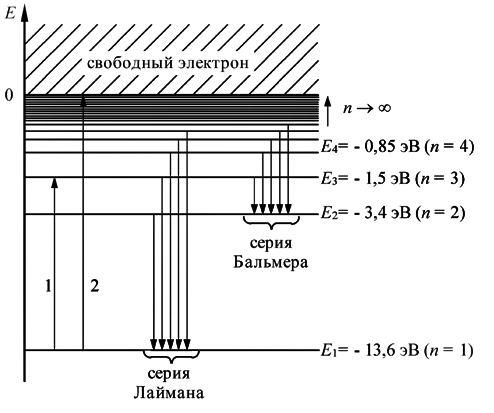
На рисунке 5.5 в соответствии с (5.12) изображен энергетический спектр электрона в атоме водорода. В области положительных энергий энергетический спектр свободного электрона является сплошным спектром. В области отрицательных значений полной энергии энергетический спектр связанного с атомом электрона становится дискретным. Для наглядности на рис. 5.5 каждому возможному значению энергии соответствует энергетический уровень. В стационарном состоянии электрон может находится на одном из этих дискретных энергетических уровней. Переход электрона с одного уровня на другой на этом рисунке может быть изображен соответствующей стрелкой, начало и конец которой указывают энергетические уровни, между которыми происходит переход. Обычно
атом находится в основном состоянии
с наименьшим значением энергии,
равным Если атому сообщить дополнительную энергию, то он может перейти в возбужденное состояние (переход 1 на рис. 5.4). Электрон при этом переходит на орбиту большего радиуса. Возбуждение атомов может инициироваться различными способами, например, столкновением атомов газа в хаотическом тепловом движении, пропусканием через газ потока высокоэнергетических частиц (электронов, альфа-частиц и др.) и, наконец, поглощением атомами излучения. Если энергия, переданная электрону будет достаточно велика, то электрон может преодолеть силу притяжения к ядру и оторваться от атома. Такой процесс называют ионизацией атома. Из рис. 5.4 видно, что минимальная энергия, необходимая для ионизации атома водорода (переход 2), равна
Это значение хорошо согласуется с экспериментальными данными для энергии ионизации атома водорода. Возбуждение атома водорода происходит при нагревании, электроразряде, поглощении света и т. д., причём в любом случае атом водорода поглощает определённые порции — кванты энергии, соответствующие разности энергетических уровней электронов. |
|
|
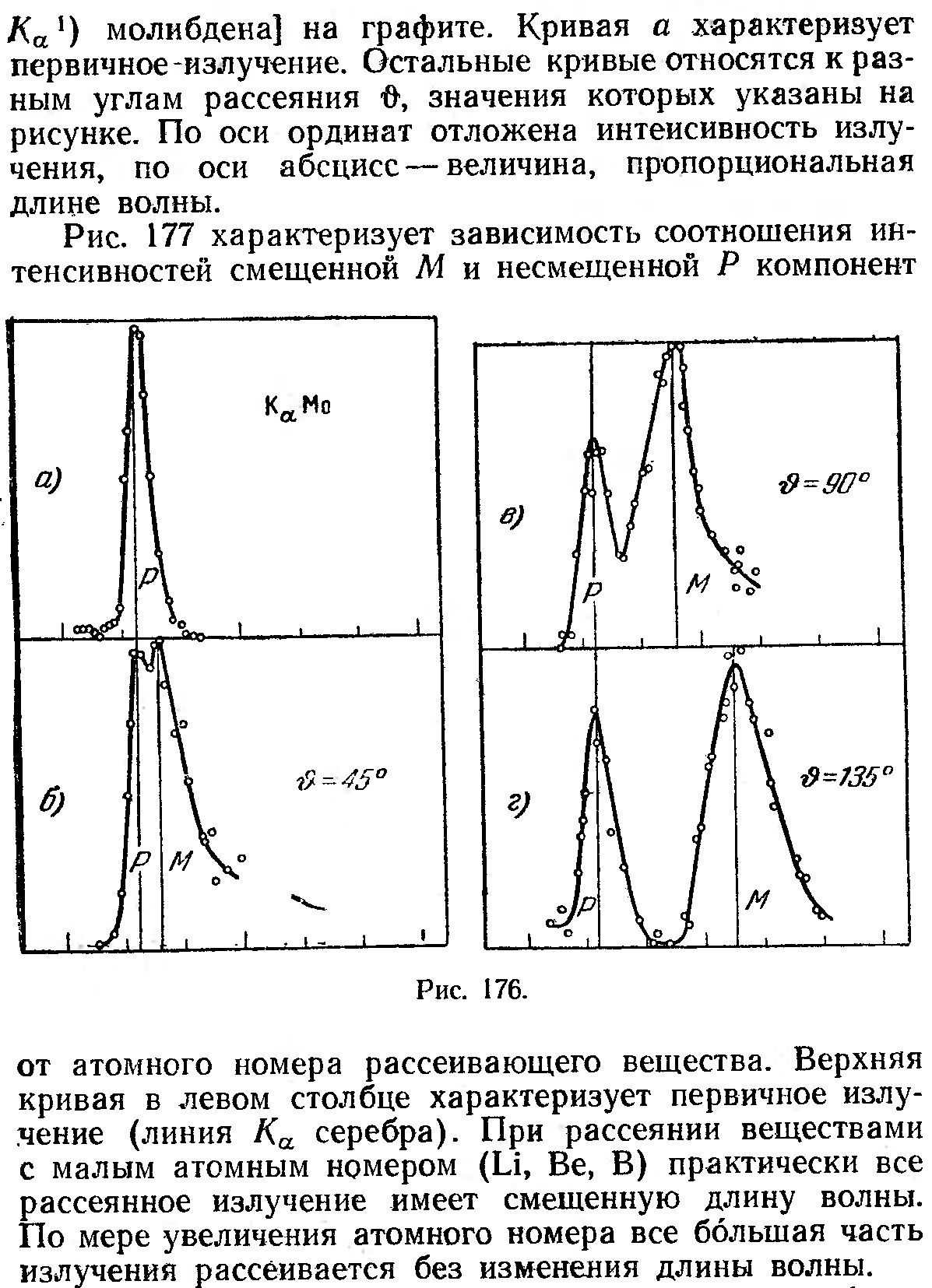
9.Эффект Комптона.
|
10.Гипотеза Луи-де-Бройля
|
|
|
11.Свойства волн де Бройля
|
14.Соотношение неопределенности.
|
|
|
13.Вероятностная интерпретация волновой функции. квадрат
модуля Указанная
вероятностная интерпретация волновой
функции – один из основных постулатов
квантовой теории, который подтвержден
всей совокупностью проведенных
экспериментов.
Покажем, что из УШ
вытекает закон сохранения вероятности.
Запишем уравнения для
Умножив
первое уравнение на
Введем
плотность
В результате находим уравнение непрерывности (ср. с электродинамикой, ч. 1 курса):
Удалив
получим
или
Для физически реализуемых состояний всегда можно выбрать такую нормировку волновой функции, что
Это соотношение означает, что вероятность обнаружить частицу во всем пространстве равна единице, как и должно быть. Замечание.
Плотность
Функции
|
12.Волновая функция электрона.
|
|
|
15.Ядерная модель атома.
|
|
|