
Герпес
.docНАЦІОНАЛЬНИЙ МЕДИЧНИЙ УНІВЕРСИТЕТ
ІМЕНІ О.О. БОГОМОЛЬЦЯ
Кафедра мікробіології, вірусології та імунології
ІНДИВІДУАЛЬНА РОБОТА СТУДЕНТА
З дисципліни «Мікробіології, вірусології та імунології»
на тему:
«hERPESVIRIDAE. ЗНАЧЕННЯ У ЖИТТІ ЛЮДИНИ»
-
Студентки II курсу 1 групи
стоматологічного факультету
Лисенко Анни Олександрівни
Викладач: Настенко Володимир Борисович
Київ - 2014
План
-
Герпетичні вірусні захворювання – актуальна проблема сучасної медицини.
-
Патогенні представники вірусу герпесу людини.
-
Шляхи інфікування вірусом герпесу.
-
Клінічна симптоматика, патогенез та діагностика герпетичної хвороби.
-
Протигерпетичне лікування.
Віруси – неклітинні форми життя, які є внутрішньоклітинними абсолютними паразитами. В житті людини вірус герпесу відіграє виключно негативну роль.
Г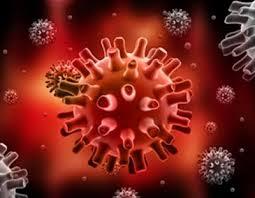
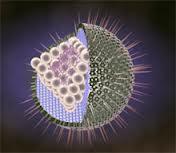 ерпесвіруси
(Herpesviridae) —
родина ДНК-вмісних вірусів, які можуть
уражати людину і різноманітних тварин.
Натепер відомо близько 200 вірусів в цій
родині. Вони спричиняють хронічні
ураження з довічною персистенцією в
організмі уражених. Відомо 8 типів
герпесвірусів, що спричиняють хвороби
у людини.
ерпесвіруси
(Herpesviridae) —
родина ДНК-вмісних вірусів, які можуть
уражати людину і різноманітних тварин.
Натепер відомо близько 200 вірусів в цій
родині. Вони спричиняють хронічні
ураження з довічною персистенцією в
організмі уражених. Відомо 8 типів
герпесвірусів, що спричиняють хвороби
у людини.
Герпетичні вірусні захворювання – одна з актуальних проблем сучасної клінічної медицини. В організмі людей герпес-віруси, як правило, довгий час перебувають безсимптомно. І в разі розвитку имуносупресії можуть спричиняти тяжкі ускладнення з смертельним результатом. За даними ВООЗ, в структурі смертності від вірусних захворювань герпес знаходиться на другому місці (15,8%) після вірусних гепатитів (35,8%).
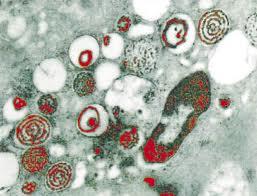

За сучасними оцінками, інфікованість населення вірусом простого герпесу (ВПГ) наближається до 100%, що підтверджується сероепідеміологічними дослідженнями. Герпес все частіше створює комплекс медичних, соціальних, психологічних і косметичних проблем. ВПГ обумовлює захворювання статевих органів у чоловіків і жінок, викликає висхідні і екстрагенітальні ураження (очей, нервової системи, внутрішніх органів). Відмічається тенденція до зростання латентних форм герпетичної інфекції (ГІ) осіб, що ведуть безладне сексуальне життя. Різко зросла кількість хворих на рецидивуючу статеву герпес-вірусну інфекцію.
Простий герпес займає провідне місце серед вірусних хвороб людини, а 95% населення є носіями вірусу. Згідно з даними ВООЗ в останні роки збільшується захворюваність на цю інфекцію, а також кількість ускладнених форм. Збудник - вірус простого герпесу. Розрізняють два типи вірусу. Перший тип передається повітряно-крапельним, рідше контактним, шляхом і спричиняє ураження шкіри обличчя /особливо навколоротової ділянки/. Другий тип вірусу передається переважно статевим шляхом і є причиною розвитку генітального герпесу. Характерною особливістю герметичної інфекції людини є те, що після першого контакту з нею вірус пожиттєво зберігається у латентному стані в регіонарних сенсорних гангліях. У розвитку інфекційного процесу має значення стан макроорганізму, у третині випадків хвороба рецидивує до 6-8 і більше разів на рік. Після інфікування в організмі утворюються антитіла до вірусу простого герпесу і в подальшому впродовж усього життя зберігаються на відносно постійному рівні. Рецидиви хвороби ці антитіла не попереджують. Найчастіша локалізація: губи, обличчя, кон`юнктива і рогівка ока, сідниці. Первинний ГЕНІТАЛЬНИЙ ГЕРПЕС виникає після 1-10-денного інкубаційного періоду і проявляється у жінок гострим везикульозним вульвовагінітом або ендоцервіцитом, у чоловіків - гострим герметичним баланопоститом.
Як уже вказувалось, вірус простого герпесу тип 2 (ВПГ-2) є чинником герпесу статевих органів. Основною ознакою герпетичної інфекції є отримання на все життя прихованої інфекції, яка може повторно активізуватися, спричинюючи один чи більше витків захворювання. Прихована інфекція ВПГ-2 в першу чергу з’являється в нейронах, що містяться в корінцях нервових гангліїв. Клінічний спектр ВПГ-2 включає первинну інфекцію, що характеризується появою пухирців на вульві або пенісі, які через деякий час розриваються, залишаючи дрібні, болючі виразки. Виразки загоюються через 1-3 тижня, хоча у імуноскомпрометованих пацієнтів загоєння може перебігати дуже повільно. За різними оцінками, частка симптоматичних інфекцій дорівнює від 13% до 37% і ймовірно є ще вищою у ВІЛ-позитивних осіб. Субклінічна інфекція може бути пов’язана зі зниженням інфекційного вірусного навантаження. Вірус передається з виділеннями статевих органів. Передача ВПГ-2 новонародженим під час пологів може привести до руйнівної системної інфекції та енцефаліту. На щастя, ризик герпесу новонароджених у ВІЛ-негативних вагітних жінок, які мешкають у промислово розвинутих країнах, низький (менше 3%).
Герпес статевих органів – одне з найрозповсюдженіших захворювань, при якому виникає виразка статевих органів. За оцінками, у США, наприклад, ВПГ-2 уражені від 40 до 60 мільйонів людей, при відсотковому співвідношенні 1-2 мільйони інфекції і 600-800 тисяч клінічних випадків на рік. Розповсюдженість у популяції 30-40-літніх людей складає приблизно 30%. У цілому, у жінок розповсюдженість вища, ніж у чоловіків, особливо серед молоді. Однакові незалежні фактори інфекції ВПГ-2 були ідентифіковані у осіб обох статей: старший вік, більш вища кількість сексуальних партнерів за життя, позитивна серологія ВІЛ і позитивна серологія сифілісу. Розповсюдженість у розвинутих країнах може варіювати від 2% до 74% в залежності від країни, віку, статі або міського, або сільського району. До 40% випадків зафіксовано у жінок у віці від 15-19 років у сільській місцевості Коста-Ріки, Кенії (Кисуму) та Мексики (Мехико). Дослідження, проведене на водіях вантажівок в Бангладеші, показало більш високу розповсюдженість ВПГ-2 (25,8%) у порівнянні з сифілісом (5,7%), гонореєю (2,1%) і хламідіями (0,8%).
Нарешті, з’явились цілком достатні свідчення того, що інфекція ВПГ-2 є головним супутнім фактором інфекції ВІЛ. У розвинутих країнах, де інфікованість ВПГ-1 у дитячому віці знизилась, серорозповсюдженість ВПГ-2 збільшилась, припускається можливість захисного ефекту ВПГ-1 проти зараження ВПГ-2, хоча ВПГ-1, вочевидь, фактично не впливає на ризик ураження на ВПГ-2.
Перспективи розробки вакцини проти ВПГ-2, яка могла б забезпечити стерильну імунність, вважається нереальною. Мета розробки такої вакцини складає скоріше в запобіганні встановленої прихованої інфекції, блокуючи доступ вірусу до чутливих гангліїв, зниження тяжкості симптомів або зменшення кількості рецидивів.
Шляхи зараження:
-
Основний шлях зараження – проникаючий секс без презерватива.
-
Інфікування вірусом може відбуватися при поцілунках, доторкуваннях до уражених ділянок.
-
Передача вірусу можлива від інфікованої матері до дитини.
Розвиток захворювання
Інкубаційний період при генітальному герпесі становить у середньому від 2 до 10 днів, досягаючи іноді 3 тижнів.
Симптоми
-
Відчуття поколювання, пекучого болю або свербіння в генітальній або анальній ділянці. У чоловіків ці явища спостерігаються на шкірі статевого члена, навколо заднього проходу або в прямій кишці. У жінок зазвичай уражається генітальна ділянка, включаючи піхву, а також пряма кишка.
-
Загальне нездужання може супроводжуватись підвищенням температури і, можливо, появою болю в ногах або в паху.
-
Пізніше у зоні ураження з’являються маленькі червоні вузлики, що перетворюються на пухирці (везикули), наповнені прозорою рідиною.
-
Пухирці лопаються з утворенням невеликих червоних виразок, що можуть бути болючими.
-
Якщо виразки розташовані на сухих ділянках шкіри, то через 1-2 тижні вони гояться з утворенням кірочок.
-
Якщо ранки контактують із сечею, то сечовипускання може бути болючим.
Інфекція тривалий час може перебігати зовсім безсимптомно. Однак у разі переохолодження, вираженої фізичної і психоемоційної втоми вірус нагадує про себе. Рецидивує у 50-75% хворих. Серед провокуючих чинників стреси, менструація, переохолодження тощо.
Наслідки: Вірус герпесу впливає на перебіг вагітності, нерідко призводить до мимовільних викиднів і загибелі плоду, інфікування немовлят. Оскільки знищити сам вірус поки що неможливо, лікування спрямоване на зменшення болю під час загострень та на запобігання рецидивів хвороби.
Обстеження проводиться шляхом визначення рівня антитіл методом імуноферментного аналізу та іншими. Одним з найбільш ефективних засобів профілактики захворювання є презервативом.
Увагу клініцистів привертає частота герпетичних уражень ґеніталій і у дівчат. Досить складною і соціально значимою є проблема венеричної герпес-віруної інфекції, пов'язаної з її поширенням серед вагітних жінок, що спричиняє спонтанні аборти, передчасні пологи, ураження плоду і новонароджених дітей, появу у них природженої неонатальної і постнатальної патології.
Неонатальний герпес є наслідком зараження у внутріутробному і постнатальному періоді. Встановлено, що маніфестні форми ГІ у вагітних, як правило, грають істотну роль у формуванні патології плоду і новонародженого. Проте несприятливий результат вагітності може бути пов'язаний і з безсимптомною формою ГІ матері. Не спричиняючи особливих розладів здоров'я, ВПГ у ряді випадків можуть проникати в плаценту, ембріон або плід і викликати тяжкі ураження плоду і новонародженого.
На цей час відкрито і вивчено більше 80 представників сімейства герпес-вірусів. Серед вірусів герпесу людини є 8 патогенних представників: вірус простого герпесу типу 1 (ВПГ-1); вірус простого герпесу типу 2 (ВПГ-2); вірус варицелла-зостер (вірус вітряної віспи) (ВВЗ); вірус Епштейн-Барра (ВЕБ); цитомегаловірус (вірус герпесу людини типу 5); вірус герпесу людини типу 6 (ВПГ-6); вірус герпесу людини типу 7 (ВПГ-7); вірус герпесу людини типу 8 (ВПГ-8).
Статистично достовірні дані про поширеність захворювань, спричинених ВПГ, відсутні, оскільки можливості лабораторного і епідеміологічного нагляду в багатьох країнах ще недостатні. Сьогодні більше 95% дорослого населення мають антитіла до вірусу того або іншого типу. Найбільш поширені ВПГ-1 і ВПГ-2, антитіла до яких є у 90-99% дорослого населення Землі.
Дані обстежень, проведених в Інституті дерматології і венерології АМН України, дозволяють припустити, що захворюваність ґенітальним герпесом (ГГ) в Україні досягає 200 випадків на 100 000 населення. При цьому частота виявлення цього захворювання значно варіює залежно від низки чинників (віку, характеру сексуального життя, соціально-культурного рівня пацієнтів тощо).
Захворювання, обумовлені ВПГ, як, правило, відмічаються довільним перебігом і вельми контагіозні. Збудники герпетичної хвороби передаються різними шляхами, але інфікування в більшості випадків відбувається при близьких фізичних контактах, передаючись від хворого здоровому: горизонтальний шлях передачі інфекції здійснюється повітряно-краплинним або статевим шляхом; вертикальний шлях – від матері плоду.
Поширення герпес-вірусної інфекції відбувається при ґенітальних, ороґенітальних і анальних статевих , а також під час пологів, коли зараження новонародженого походить від інфікованої матері. Можливо і внутріутробне трансплацентарне інфікування плоду. Внутріутробна герпетична інфекція може бути причиною перинатальної летальності, мимовільних викиднів, передчасних пологів або ранньої інвалідності дітей (глухота, сліпота, епілепсія, мікроцефалія, вади серця, гепатоспленомегалія і ін.).
До 70% випадків захворюваності неонатальним герпесом, що має латентну форму, пов'язані з інфікуванням дитини від матері. Маніфестна форма інфекції у новонароджених дітей зазвичай відбувається в перших 2 тижні життя і перебігає у вигляді диссемінованих захворювань з ураженням шкіри, слизистих оболонок, легенів, ЦНС, печінки, які супроводжуються тромбогеморагічним синдромом. Летальність у новонароджених досягає 50-80%.
Інфікування ВПГ-1 зазвичай відбувається в перших 3 роки життя дитини, а ВПГ-2 – в період статевого дозрівання. Рано потрапляючи в організм людини, ВПГ довічно персистирує в ньому, періодично рецидиви різної тяжкості. Герпес-віруси перебувають в латентному стані в паравертебральних сенсорних гангліях. В період загострення вони активізуються і по периферичних нервах досягають місця ураження.
Персистенція герпес-вірусу в організмі людини пов'язана з його здатністю «вислизати» від імунного преса. Віруси герпесу володіють здатністю ушкоджувати клітинний імунітет, виявляючи иммуносупресивну дію. Тривала персистенція вірусів призводить до вторинного імунодефіциту, який, у свою чергу, сприяє їх активації. У зв'язку з цим в патогенезі захворювання велике значення має імунокомпетентність організму.
ВПГ можуть асоціюватися з іншими збудниками, коли не унеможливлено розмноження одного або всіх компонентів асоціації. Генітальний герпес часто (у 49,3% випадків) перебігає в змішаній інфекції: з хламідіями, мікоплазмами, трихомонадами. У 33% пацієнтів спостерігається поєднане інфікування ВПГ-1, ВПГ-2 і вірусом Епштейн-Барра (ВЕБ).
При ґенітальній інфекції, викликаній вірусом герпесу і хламідіями, відмічається легший або, навіть, латентний перебіг інфекції. Поєднане інфікування ВПГ-1, ВПГ-2 і ВЕБ 75,4% хворих обумовлювало тривалі і часті рецидиви. У таких пацієнтів спостерігалися: температурна реакція, хронічні осередки інфекції в рото- і носоглотці, астенічні прояви (стомлюваність, млявість, слабкість), негативне ставлення до можливостей медицини і ефективності лікування.
Основною особливістю герпес-вірусних захворювань є їх хронічна рецидивуюча течія. Герпес характеризується клінічним поліморфізмом, його прояви варіюють від обмежених уражень шкіри і слизових оболонок до ґенералізованих форм. Спостерігаються ураження внутрішніх органів, нервової системи, очей. У літературі описані порушення функцій кісткового мозку, надниркових, дихальної і серцево-судинної систем, а також опорно-рухового апарату.
Клінічна симптоматика герпетичної хвороби не завжди патогномонічна і специфічна. Клінічні форми захворювань більшою мірою залежать від типу вірусу і характеру інфекції (первинне зараження або реактивація після латенції). Причиною активації ГІ нерідко бувають гормональні зміни, імунний і ендокринний дисбаланс, які призводять до активації головних генів ВПГ і швидкій продукції вірусних білків. Важливу роль в інфікуванні і активації вірусу грають умови життя і харчування пацієнтів.
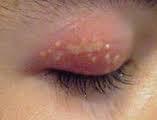
ВПГ-1, як правило, спричиняє герметичний дерматит, оральні і окулярні ураження: рецидивуючий орально-лабіальний герпес, ларингіт, гінгівостоматит, кон'юнктивіт, герпес-вірусний кератит. Рідко бувають енцефаліт, езофагіти, гепатити, а також неонатальна інфекція, обумовлені ВПГ-1.
Дерматит – це запалення шкіри, спричинене подразнюючою чи сенсибілізуючою дією екзогенних чинників. Причини розвитку дерматитів надзвичайно різноманітні. Розрізняють простий контактний (артифіціальний) дерматит і алергійний контактний дерматит.
Простий контактний дерматит.
Частіше розвивається гостро, після першого ж впливу певного чинника і має тенденцію до зворотного розвитку при його усуненні, в більшості випадків виникає тільки на місці контакту з відповідним чинником, іноді точно повторюючи його форму. За клінічними проявами розрізняють дерматити: еритематозні (еритемо-сквамозні), папульозні, везикульозні, бульозні і некротичні. Часто елементи висипки комбіновані (папуло-везикульозний, еритемо-бульозний тощо). Слід відзначити, що при локалізації на обличчі і геніталіях дерматит часто супроводжується значним набряком, що дуже лякає хворих і що необхідно враховувати при призначенні терапії.
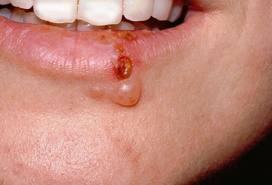
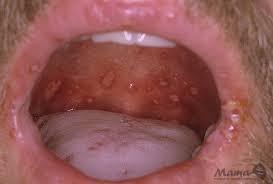
ВПГ -2 індукує в основному ураження статевих органів: ґенітальний герпес, ґеніто-ректальный герпес, крижовий радикуліт, менінгіт, енцефаліт, неонатальний герпес.
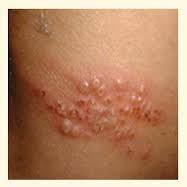
Вірус варицелла-зостер (ВВЗ) спричиняє вітряну віспу і рецидив оперізуючого лишая, а також персистируючий неврит, відомий як постгерпетична невралгія. ВВЗ – етіологічний чинник виразково-некротичної форми невралгії, яка є індукторною для СНІДУ ознакою. ВВЗ-інфекція у дорослих нерідко спричиняє пневмонію, тривалу фебрильну лихоманку і персистируючу віремію. У вагітних може провокувати природжені захворювання плоду і навіть його внутріутробну загибель.
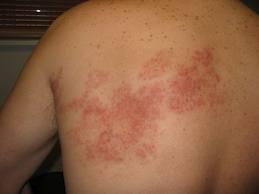
Вірус Епштейн-Барра може спричиняти енцефаліт у новонароджених, інфекційний мононуклеоз, лімфоїдну інтерстиціальну пневмонію у дітей, лімфому Біркета. Проведені клінічні спостереження вказують на можливість інфікування урогенітального тракту лімфотропним герпес-вірусом Епштейн-Барра з появою на статевих органах ерозивно-виразкових елементів.
При цитомегаловірусі (ВПГ-5) у випадках внутріутробного інфікування нерідко в патологічний процес залучаються відразу декілька органів: печінка, легені, шкіра, наднирники. При асоціації з ВІЛ-інфекцією, інших виражених імунодефіцитах у пацієнтів буває маніфестна вірусна інфекція (інтерстиціальна пневмонія, енцефаліт, полірадикулопатія, езофагіт, нефрит, коліт).
ВПГ-6 може бути причиною гепатиту, пневмонії, гематологічних порушень, уражень сполучної тканини; ВПГ-7 грає етіологічну роль при синдромі хронічної слабкості, лімфаденопатії. У дітей можливий висип – мономорфний, частіше поліморфний висип у вигляді короподібних елементів, пухирів, геморагій, які з'являються після вираженої температурної реакції; ВПГ-8 асоціюється з саркомою Капоши, злоякісною лімфомою.
Групою ризику при герпес-вірусній інфекції є особи зі штучною або природною імуносупресією. До них відносяться пацієнти, що перенесли бактерійні або вірусні інфекції, радіальне опромінення, тяжкі соматичні захворювання, а також хворі, що отримували імуносупресивну хіміотерапію, мають гематологічну патологію, ВІЛ-інфекцію.
Дані, отримані на сучасному етапі, свідчать про існування можливого тісного зв'язку між злоякісними пухлинами і ВПГ. Сероепідеміологічні дослідження дозволили встановити зв'язок герпес-вірусної інфекції із злоякісними пухлинами. Доведена роль герпес-вірусів (зокрема ВПГ-2) в розвитку карциноми шийки матки, назофарингеальних карцином (ВЕБ). Очевидна роль герпесу в розвитку атеросклерозу і природженої патології у новонароджених дітей. Герпес-вірусні інфекції при тяжкому перебігу є індикаторними для СНІДу захворюваннями.
Стає очевидним, що висококонтагіозні герпес-віруси викликають поліморфні патологічні стани, з якими може зіткнутися лікар будь-якої спеціальності. Герпес-віруси здатні уражати практично всі органи і системи організму людини.
За прогнозами Всесвітнього банку інформації, проблема герпетичних інфекцій на найближче майбутнє визначається як «глобальна проблема людства». Особливого значення ВПГ набувають у зв'язку з їх довічним інфікуванням людей в будь-якому віці.
Важливими аспектами цієї проблеми є своєчасна діагностика герпес-вірусної інфекції, лікування і профілактика. При цьому необхідно враховувати особливості герпес-вірусної інфекції, а саме те, що інфікування відбувається через пошкоджену шкіру і слизові оболонки, повітряно-краплинним, трансфузійним, статевим, побутовим, трансплацентарним і інтранатальним шляхами. Не виключено зараження при трансплантації органів і тканин.
Патогенез герпетичних уражень пов'язаний з клінічними проявами і епідеміологією. Потрапляючи в організм людини, ВПГ довічно персистирує в ньому, періодично викликаючи рецидиви різної тяжкості. Найбільш високий ризик інфікування відмічається при розвитку рецидивів з місцевими проявами захворювання або ж в його продромальний період.
Діагностика захворювання складається на основі даних анамнезу (виявлення груп ризику), клінічного огляду, імуносерологічних і молекулярно-генетичних методів виявлення віріона, генома і антигенів вірусів відповідно. Труднощі діагностики виникають у зв'язку з тим, що герпес-віруси є низькоімуногенними і умовно-патогенними, тому реактивуються під впливом безлічі чинників, але, як правило, за наявності дефектів в ланках противірусного захисту.
На сьогоднішній день ще не визначена вирішальна роль якого-небудь одного із захисних імунологічних механізмів в результаті герпетичного процесу.
З одного боку, імунна відповідь організму на укорінення ВПГ опосередкована чинниками імунітету, пов'язаними не лише з участю антитіл, але і моноцитів, макрофагів, лімфоцитів, нейтральних лейкоцитів, ендотеліальних клітин, кровоносних судин, в яких відбуваються специфічні синтетичні процеси, що вимагають урахування складного патогенезу ГІ і чутливості хворих до використовуваних препаратів при розробці конкретних лікувально-профілактичних заходів для елімінації вірусу. З іншого – не береться до уваги та обставина, що при використанні імуномодулюючих препаратів лікар не знає точної «мішені» в організмі хворого, функціонального резерву окремих компонентів імунної системи та і всієї системи в цілому, а тому не може гарантувати зміни імунної відповіді організму в потрібному напрямі.
Парадоксальність герпес-вірусної персистенції полягає і в тривалому збереженні вірусу в організмі, незважаючи на інтенсивну спочатку і різноманітну імунну відповідь. Біологічні особливості збудника герпесу обумовлюють періодичні клінічні загострення.
Тривалий хронічний герпетичний процес приводить до негативної імунної перебудови – вторинного імунодефіциту. У свою чергу, розвиток вторинної імунної недостатності сприяє активації герпес-вірусів, тобто утворюється своєрідне замкнуте коло, в якому первинним може бути кожен з основних компонентів этіопатогенезу. Раціональна терапія має на меті розірвати цей коло за допомогою ліків етіотропної та імуномодулюючої дії. Препарати для лікування хворих герпесом вельми численні і варіюють за механізмом дії.
Найбільш активними антивірусними препаратами є ацикловір і його сімейство: вальтрекс, вектавір, фамвір, цимевен.
Розрізняють два способи застосування противірусних препаратів: епізодичне призначення (при загостреннях ГВІ) і супрессивна або превентивна терапія. У першому випадку препарат призначають коротким курсом (5-10дней), у другому щоденний прийом засобу протягом декількох місяців і навіть років. Ефективність етіотропної терапії буде максимальною при лікуванні в період передвісників або ініціальних проявів (у продромальному періоді) захворювання – в перших 48 ч реактивації вірусів.
Слід сказати і про те, що оптимальний клінічний ефект досягається за наявності синергізму між противірусними препаратами і захисними силами організму, які регулюються за допомогою імуномодуляції. Останнім часом інтерес лікарів до імунотропних препаратів помітно підвищився. Зазвичай використовують універсальні імуномодулятори, здатні утворення антитіл, проліферацію клонів клітин, стимулювати продукціюінтерферонів.
При тяжких формах вісцеральної патології, гематологічних порушеннях, герпетичних ураженнях сполучної тканини, органів зору, центральної нервової системи, коли відмічаються виражені порушення метаболічних процесів організму, обумовлені внутріклітинним паразитуванням ВПГ, разом з призначенням противірусних препаратів, проводиться інфузійна терапія, направлена на корекцію метаболічних реакцій організму і систем гомеостазу.
При появі сомато-метаболических порушень, рецидивуючого перебігу герпесу, уражень внутрішніх органів, нервової системи у хворих спостерігаються прихована депресія, різні форми неврозів, обумовлені стресами, експансивним переживанням факту своєї недуги. Пацієнти скаржаться на слабкість, стомлюваність, болі різної локалізації, причиною яких є емоційний і фізіологічний дисбаланс, що вимагає відповідної корекції при призначенні лікування основного захворювання.
Література
-
Белугина И.Н., Сосновский А.Т, Яговдик Н.З. Дерматологический справочник.– Минск, 2001.
-
Зовнішнє лікування хворих на псоріаз (Методичні рекомендації). Харків, 2002.
-
Калюжна Л.Д., Міхньова Є.М. Мозковий кровообіг та біоелектрична активність мозку у жінок менопаузального періоду, хворих на андрогенетичну алопецію // Дерматологія та венерологія. – 2007. – №1 (35). – С. 22 – 25.
-
Клименко В.А. Особливості харчової сенсибілізації дітей, які страждають на атопічний дерматит // Дерматологія та венерологія. – 2007. – №2 (36). – С. 33 – 37.
-
Коган Б.Г. Демодикоз: раціональна класифікація клінічних форм захворювання. Вплив імунних та гормональних зрушень на перебіг дерматозу //Укр. журн. дерматології, венерології, косметології. – 2002. – №1. – с. 62 – 64.
-
Кутасевич Я.Ф. Современные подходы к применению топических глюкокортикостероидов // Журн. Дерматологии и венерологии. -2000. - № 1(9). – С. 95-99.
-
Лікування вульгарних вугрів (Методичні рекомендації). Київ, 2002.
-
Принципи здорового харчування. Посібник для поліпшення якості роботи. Київ. 2001.
-
Пшеничникова Т.Я. Бесплодие в браке. - М.: Медицина, 1991. - 320 с.
-
Романенко И.М., Кулага В.В., Афонин С.Л. Лечение кожних и венерических болезней - М.. – 2006. - 2Т – С. 431-437
-
Соціальна медицина та організація охорони здоров'я / Під заг. ред. Ю.В. Вороненка, В.Ф. Москаленка. - Тернопіль: Укрмедкнига, 2000. - 680 с.
-
Федотов В.П., Братусь-Сухорукова Е.Ю., Погребняк Л.А., Плоская Л.М., Чайка Т.Н. Применение дипросалика и элокома в наружной терапии псориаза у лиц пожилого возраста // Дерматовенерология, косметология, сексопатология. - 2001. - № 1(4). – С. 198-199.
-
Чистякова И.А., Хапилова В.И., Авербах Е.В. Кортикостероидные гормоны в дерматологии. Сообщение II: Топическое применение кортикостероидов // Вестн. Дерматологии и венерологии. – 2000. - № 6 – С. 16-17.
-
Abramovits W. Atopic dermatitis. J Am Acad Dermatol. Jul 2005;53(1 Suppl 1):S86-93.
-
Baumer JH. Guideline review: atopic eczema in children, NICE. Arch Dis Child. Apr 1 2008
-
Bieber T. Atopic dermatitis. N Engl J Med. Apr 3 2008;358(14):1483-94.
-
Boguniewicz M, Eichenfield LF, Hultsch T. Current management of atopic dermatitis and interruption of the atopic march. J Allergy Clin Immunol. Dec 2003;112(6 Suppl):S140-50.
-
Callard RE, Harper JI. The skin barrier, atopic dermatitis and allergy: a role for Langerhans cells?. Trends Immunol. Jul 2007;28(7):294-8.
-
Heller M, Shin HT, Orlow SJ, Schaffer JV. Mycophenolate mofetil for severe childhood atopic dermatitis: experience in 14 patients. Br J Dermatol. Jul 2007;157(1):127-32.
-
Horii KA, Simon SD, Liu DY, Sharma V. Atopic dermatitis in children in the United States, 1997-2004: visit trends, patient and provider characteristics, and prescribing patterns. Pediatrics. Sep 2007;120(3):e527-34.
-
Irvine AD. Fleshing out filaggrin phenotypes. J Invest Dermatol. Mar 2007;127(3):504-7.
-
Lebwohl M, Friedlander S. New strategies for optimizing the treatment of inflammatory dermatoses with topical corticosteroids in an era of corticosteroid-sparing regimens. J Am Acad Dermatol. Jul 2005;53 (1 Pt 2):S1-S2.
-
Leung DY, Bieber T. Atopic dermatitis. Lancet. Jan 11 2003;361(9352):151-60.
-
Leung DY, Boguniewicz M, Howell MD, Nomura I, Hamid QA. New insights into atopic dermatitis. J Clin Invest. Mar 2004;113(5):651-7.
-
Morar N, Willis-Owen SA, Moffatt MF, Cookson WO. The genetics of atopic dermatitis. J Allergy Clin Immunol. Jul 2006;118(1):24-34; quiz 35-6.
-
Novak N, Bieber T, Leung DY. Immune mechanisms leading to atopic dermatitis. J Allergy Clin Immunol. Dec 2003;112(6 Suppl):S128-39.
-
Sandilands A, Smith FJ, Irvine AD, McLean WH. Filaggrin's fuller figure: a glimpse into the genetic architecture of atopic dermatitis. J Invest Dermatol. Jun 2007;127(6):1282-4.
-
Simpson EL, Hanifin JM. Atopic dermatitis. J Am Acad Dermatol. Jul 2005;53(1):115-28.
-
Weston S, Halbert A, Richmond P, Prescott SL. Effects of probiotics on atopic dermatitis: a randomised controlled trial. Arch Dis Child. Sep 2005;90(9):892-7.
-
Williams HC. Clinical practice. Atopic dermatitis. N Engl J Med. Jun 2 2005;352(22):2314-24.
-
Williams H, Flohr C. How epidemiology has challenged 3 prevailing concepts about atopic dermatitis. J Allergy Clin Immunol. Jul 2006;118(1):209-13.
-
Zutavern A, Hirsch T, Leupold W, Weiland S, Keil U, von Mutius E. Atopic dermatitis, extrinsic atopic dermatitis and the hygiene hypothesis: results from a cross-sectional study. Clin Exp Allergy. Oct 2005;35(10):1301-8.
