
- •Примеры тестовых заданий по физике
- •Содержание
- •Механика
- •2) Выше поднимется полый цилиндр
- •1) Равна 1 м при любой его ориентации
- •Молекуярная физика и термодинамика
- •2) С ростом температуры максимум кривой смещается вправо.
- •2) Положение максимума зависит от природы газа (массы молекул)
- •3. Электричество и магнетизм
- •4. Колебания и волны
- •2) Амплитуда волны обратно пропорциональна расстоянию до источника колебаний (в непоглащающей среде)
- •2) Свободных незатухающих колебаний
- •5. Волновая и квантоваяоптика
- •6. Квантовая физика и физика атома. Элементы ядерной физики и физики элементарных частиц
- •3) Частицы среды колеблются в направлении распространения волны
1) Равна 1 м при любой его ориентации
2) изменится от 1 м до 1,67 м
3) изменится от 0,6 м до 1 м
4) изменится от1 м до 0,6 м
Оба космонавта находятся в корабле и стержень неподвижен относительно них, поэтому его длина неизменна и равна 1 м.
В тоже время длина стержня с точки зрения
наблюдателя, находящегося вне корабля,
мимо которого корабль пролетает,
увеличится в соответствии с законом
![]() , и станет 1,67 м.
, и станет 1,67 м.
 Наблюдатель следит в трубу за пролетающим
мимо слева направо со скоростью близкой
к скорости света космическим кораблем.
На борту корабля нарисована эмблема:
наблюдатель ее увидит…
Наблюдатель следит в трубу за пролетающим
мимо слева направо со скоростью близкой
к скорости света космическим кораблем.
На борту корабля нарисована эмблема:
наблюдатель ее увидит…
1
 )2) 3) 4)
)2) 3) 4)


Наблюдатель увидит эмблему 1),поскольку размеры тел, движущихся со
скоростями близкими к скорости света,
сокращаются в направлении движения:![]() .
.
Молекуярная физика и термодинамика
|
1 |
Распределения Максвелла и Больцмана |
|
2 |
Средняя энергия молекул |
|
3 |
Второе начало термодинамики. Энтропия. Циклы |
|
4 |
Явления переноса |
На рисунке представлено распределение молекул по скоростям (распределение Максвелла), где f(V) = dN/NdV – доля молекул, скорости которых заключены в интервале от V до (V +dV).
f(V)
f(V)
Т1
Т2>
Т1
Т2
Vвер
v
V
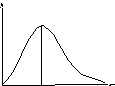
Для этой функции верным утверждением является …
1) С ростом температуры величина максимума растет.
2) С ростом температуры максимум кривой смещается вправо.
3) С ростом температуры площадь под кривой растет.
Или вариант
1) С ростом температуры площадь кривой изменяется
2) Положение максимума зависит от природы газа (массы молекул)
3) При понижении температуры величина максимума уменьшается
Наиболее вероятная скорость (положение
максимума) определяется уравнением:
Vвер=![]() .
При увеличении температуры максимум
распределения будет смещаться вправо,
в область более высоких скоростей, при
этом величинаf(V)
будет меньше, так как суммарная
площадь под кривой должна остаться
равной общему числу молекул.
.
При увеличении температуры максимум
распределения будет смещаться вправо,
в область более высоких скоростей, при
этом величинаf(V)
будет меньше, так как суммарная
площадь под кривой должна остаться
равной общему числу молекул.
Зависимость от массы молекулы будет обратной: с ростом массы максимум будет смещаться влево, поскольку масса стоит в знаменателе.
Правильные варианты ответов:
С ростом температуры максимум кривой смещается вправо.
Положение максимума зависит от природы газа (массы молекул).
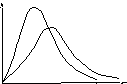
В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение скоростей молекул гелия будет описывать кривая (приведены три кривые аналогичные предыдущей).
Согласно предыдущему примеру с ростом массы молекул максимум будет смещаться влево, поскольку масса стоит в знаменателе.
Средняя кинетическая энергия молекул газа при температуре Т зависит от их структры, что связано с возможностью различных видов движения атомов в молекуле. Средняя кинетическая энергия молекул гелия (Не) равна …
1) (5/2)kT 2) (1/2)kT 3) (3/2)kT 4) (7/2)kT
Средняя кинетическая энергия молекул газа при температуре Т равна Ек = (i/2) kT, где i – число степеней свободы молекулы.
Числом степеней свободы телаiназывают число независимых координат, полностью определяющих положение тела в пространстве.
а) молекулы, состоящие из одного атома, можно представить материальной точкой, положение которой полностью определяется заданием трех ее координат. Одноатомные молекулы (He,Ar) имеетi= 3, ответ3).
б )
Положение двухатомной молекулы полностью
определяется заданием трех координат
центра инерции (x,y,z)
и двух углов θ и ψ вращения вокруг осейOXиOZ.
Вращением вокруг оси ОУ можно пренебречь,
т.к. момент инерции её относительно оси
ОУ пренебрежительно мал. Двухатомная
молекула имеетi= 5: три
степени свободы поступательные и две
– вращательные.
)
Положение двухатомной молекулы полностью
определяется заданием трех координат
центра инерции (x,y,z)
и двух углов θ и ψ вращения вокруг осейOXиOZ.
Вращением вокруг оси ОУ можно пренебречь,
т.к. момент инерции её относительно оси
ОУ пренебрежительно мал. Двухатомная
молекула имеетi= 5: три
степени свободы поступательные и две
– вращательные.
в) молекулы из трех и более жестко связанных атомов, не лежащих на одной прямой, полностью определяются тремя координатами центра инерции (x,y,z) и тремя углами вращения (θ, γ, ψ) вокруг осей (OX,OY,OZ).
N– атомная молекула (N≥ 3) имеетi= 6: три степени поступательные и три – вращательные.
г) если многоатомная молекула N≥ 2 имеет упругую связь, то в системе может возникнуть колебательное движение. Нужно учесть и его колебательные (от 1 и более). Колебательная степень свободы должна иметь энергию, вдвое большую по сравнению с поступательной или вращательной. Это объясняется тем, что колебательное движение связано с наличием кинетической и потенциальной энергий. На колебательные степени свободы приходится энергия в два раза больше: Еколеб=kT. Колебательные степени свободы возбуждаются при высоких температурах, что должно специально оговариваться.
Средняя кинетическая энергия молекул газа при температуре Т равна Ек = (i/2) kT, где i – число степеней свободы молекулы: поступательного, вращательного и колебательного движений молекулы. При условии, что имеют место только поступательное и вращательное движение, для водорода (Н2) число i равно …
1) 3 2) 53) 7 8)
При условии, что имеют место только поступательное и вращательное движение, для водяного пара (Н2O) число i равно
1) 3 2) 5 3) 64) 8
Состояние идеального газа определяется значением параметров T0,p0иV0. Определенное количество газа перевели из состояния (3p0,V0) в состояние (p0, 2V0) при этом его внутренняя энергия …
1) не изменилась 2) увеличилась 3) уменьшилась
Уравнение состояния идеального газа pV=vRT. Первому состоянию соответствует изотерма Т1= (3p0V0)/vR, второму – Т2= (2p0V0)/vR. Внутренняя энергия идеального газа пропорциональна температуре. Поскольку Т1> Т2, внутренняя энергия газауменьшилась.
Если U– изменение внутренней энергии идеального газа, А – работа газа,Q– теплота, сообщаемая газу, то для изобарного нагревания газа справедливы соотношения …
1) Q> 0; А > 0;U= 02) Q > 0; А = 0; U > 0
3) Q> 0; А > 0;U> 0 4)Q= 0; А < 0;U> 0
Согласно первому началу термодинамики Q=U+ А – тепло переданное системе идет на увеличение ее внутренней энергии и совершение работы. При изобарном нагревеQ> 0, давление постоянно, т.е. работаdА =PdV= 0 не совершается. Правильный ответ 2)Q > 0; А = 0; U > 0.
В процессе обратимого адиабатического нагревания постоянной массы идеального газа его энтропия …
1) уменьшается 2) не изменяется3) увеличивается
Для обратимого процесса dS=dQ/T. При адиабатическом процессе обмена теплом не происходит:dQ= 0, значит, энтропия не меняется.
На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия.
Теплота подводится к системе на участке…
1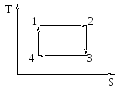 )
1-2 2) 2-3 3) 3-4 4) 4-1
)
1-2 2) 2-3 3) 3-4 4) 4-1
Цикл Карно состоит из двух изотерм: 1-2, 3-4 и двух аддиабат: 2-3, 4-1. При адиабатическом процессе система по определению не обменивается теплом с внешней средой. При изотермическом процессе энтропия (степень «беспорядка») будет расти с ростом температуры, то есть на участке 1-2.
На той же диаграмме адиабатное расширение происходит на участке …
1) 1-2 2) 2-3 3) 3-4 4) 4-1
При адиабатическом расширении температура падает, значит. расширению будет соответствовать участок 2-3.
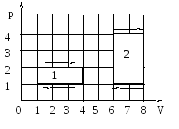 На (р,V)
диаграмме изображены два циклических
поцесса.
На (р,V)
диаграмме изображены два циклических
поцесса.
Отношение работ, совершенных в каждом цикле А1/А2 будет равно …
1) 2 2) -1/2
3) -2 4) 1/2
На диаграмме р-V работа А = рdV равна площади под кривой и будет отрицательна, если объем уменьшается. Работа в первом цикле А1 = 3 «клетки», во втором цикле А = 6 «клеток» и в обоих случаях положительна. А1/А2 = ½.
Работа отрицательной в любом из циклов при изменении направлении обхода контура.
На (р,V) диаграмме изображен циклический поцесс.
На каких участках температура
р
А Б
Д С
V
2) уменьшается
3) остается постоянной
При изобарных процессах (АБ и СД)
PV = RT, Р = RT/V т.е. Т растет, где растет V и наоборот.
На изохорных участках ДА и БС
PV = RT, V = RT/ Р
т.е. температура растет с возрастанием давления и наоборот.
