

Министерство здравоохранения и социального развития Российской Федерации
Государственное бюджетное образовательное учреждение высшего профессионального образования
«Саратовский государственный медицинский университет имени В.И. Разумовского» Министерства здравоохранения и социального развития Российской Федерации
(ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития России)
П.В. Решетов, Н.В. Неврюева, О.П. Семенова, С.Б. Орлов
Основные типы химических реакций и процессов в функционировании живых систем
Методическое пособие к лабораторно – практическому занятию для студентов медицинских специальностей
Саратов
2013
1

Министерство здравоохранения и социального развития Российской Федерации
Государственное бюджетное образовательное учреждение высшего профессионального образования
«Саратовский государственный медицинский университет имени В.И. Разумовского» Министерства здравоохранения и социального развития Российской Федерации
(ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития России)
П.В. Решетов, Н.В. Неврюева, О.П. Семенова, С.Б. Орлов
Основные типы химических реакций и процессов в функционировании живых систем
Методическое пособие к лабораторно – практическому занятию для студентов медицинских специальностей
Саратов
2013
2
УДК 546 /07/541.6
Методическая разработка является руководством к выполнению модуля по теме:
«Основные типы химических реакций и процессов в функционировании живых систем».
Разработка составлена для студентов медицинских специальностей.
В методической разработке вопросы теории и практики соединены в единую форму занятий. Широко представлен тестированный контроль, благодаря которому студент сможет проверить свои знания. Последовательность расположения заданий служит установлению логической связи между основными понятиями и раскрытию обобщающих закономерностей.
Авторы-составители: П.В. Решетов, доктор химических наук, профессор, зав.
кафедрой общей и биоорганической химии СГМУ, Семенова О.П., кандидат медицинских наук, ассистент кафедры общей и биоорганической химии, Н.В. Неврюева, кандидат химических наук, ассистент кафедры общей и биоорганической химии СГМУ, С.Б. Орлов,
старший преподаватель кафедры общей и биоорганической химии СГМУ.
Под общей редакцией профессора Решетова П.В.
Рецензенты:
Рекомендовано к изданию ЦМКС СГМУ
© Решетов П.В., Семенова О.П., Неврюева Н.В., Орлов С.Б.
© Саратовский государственный медицинский
университет,
2013 г
3
Техника безопасности при работе в химической лаборатории Общие правила работы
1.Категорически запрещается работать в лаборатории одному. Приступать к работе можно только в присутствии преподавателя или лаборанта.
2.Запрещается работать в лаборатории в неустановленное время без разрешения преподавателя.
3.В лаборатории следует работать в халате из хлопчатобумажной ткани, застегивающемся спереди. Необходимо иметь мыло, полотенце, тряпку, спички.
4.Во время работы в лаборатории необходимо соблюдать чистоту, тишину и порядок. Беспорядочность, поспешность или неряшливость часто приводят к повторению работы и даже к несчастным случаям.
5.Запрещается посещение студентов, работающих в лаборатории, посторонними работами или разговорами.
6.Категорически запрещается производить какие бы то ни было работы, не связанные с выполнением задания, полученного от преподавателя.
7.Рабочее место следует содержать в чистоте и порядке; нельзя загромождать его посудой, бумагой. Запрещается держать на лабораторном столе портфели, сумки и другие посторонние предметы.
8.Категорически запрещается пить в лаборатории воду, принимать
пищу.
9.Приступать к каждой работе можно только с разрешения преподавателя, после полного усвоения всех ее операций и знакомства со свойствами применяемых в синтезе веществ(токсичность, огнеопасность и другие.)
10.Прежде чем взять необходимое количество вещества для синтеза, нужно внимательно прочитать надпись на этикетке.
11.Органические вещества нельзя брать незащищенными руками. Кристаллические вещества следует отбирать сухим шпателем или специальной ложкой. При взвешивании сухих реактивов нельзя высыпать их прямо на чешку весов.
12.Запрещается пробовать химические вещества на вкус, а также всасывать ртом в пипетки любые органические вещества и их растворы. Определять запах соединения можно, осторожно направляя к себе его пары легким движением руки.
13.Перед проведением каждой операции нужно тщательно осмотреть аппаратуру и посуду, убедиться в том, что установка или прибор собран правильно.
14.Нельзя нагревать закупоренными никакие сосуды или аппараты, кроме специально предназначенных для такого нагревания. При перегонках нельзя наглухо присоединять приемник – это может вызвать взрыв.
4
15.Во время нагревания органических веществ в пробирках или колбах нельзя направлять отверстие сосуда на себя или на соседей, а также заглядывать в пробирки и колбы сверху, так как в случае выброса нагретого вещества может произойти несчастный случай.
16.Категорически запрещается оставлять действующие установки без присмотра.
17.Нельзя работать в грязной посуде. Посуду следует мыть сразу же после окончания опыта.
18.Запрещается выливать в раковины остатки кислот, щелочей, растворителей, смол, сильно пахнущих веществ. Указанные вещества нужно сливать в специальные склянки, находящиеся в вытяжных шкафах.
19.Не разрешается бросать в раковины бумагу, битое стекло, вату, песок и другие твердые вещества.
20.Во время работы не следует касаться руками лица: многие органические вещества сильно раздражают кожу, а при попадании на слизистую оболочку глаз вызывают воспаление.
21.Склянки с веществами нельзя поднимать или переносить, держа за горло. Их берут за горлышко, поддерживая другой рукой дно склянки.
22.Не следует оставлять без надобности горящие газовые горелки или включенные электроприборы. Необходимо экономить газ, электричество, воду, реактивы.
23.Следует соблюдать осторожность при работе со стеклянными трубками, капиллярами, приборами.
Вставляя стеклянную трубку, стеклянную палочку, термометр в пробку, нужно предварительно оплавить концы трубки (палочки), смазать отверстие пробки глицерином и, взяв трубку (палочку, термометр) как можно ближе к вставляемому концу, ввести ее поступательно-вращательным движением.
24.Необходимо пользоваться защитными очками при выполнении работ, связанных с опасностью для глаз, в частности:
- при работе с концентрированными кислотами и щелочами; - с концентрированным раствором аммиака; - с взрывчатыми веществами;
- при возможном разбрызгивании и разбрасывании едких веществ (перемешивание кислот и щелочей, дробление твердой щелочи, хлорида цинка, оплавление);
- при дроблении металлических сплавов; - при работе с металлическим натрием;
- при изготовлении стеклянных капилляров; - при перегонке в вакууме и работе с вакуум - приборами.
25.По окончании работы необходимо:
-вымыть посуду и сдать лаборанту;
-положить лапки, кольца, подставки, бани в отведенные для них места;
-вытереть поверхность стола;
-выключить воду, газ и электричество.
5
Работа с легковоспламеняющимися, взрывоопасными
иядовитыми веществами
1.Все работы с легковоспламеняющимися жидкостями (диэтиловый эфир, спирт, ацетон, петролейный эфир, бензин, бензол) должны проводиться только вдали от открытого огня и включенных электроплиток.
2.Запрещается нагревание легковоспламеняющихся жидкостей на открытом пламени. Нельзя нагревать горючие жидкости в открытых сосудах. Эти вещества следует нагревать или перегонять в колбах, снабженных водяными холодильниками, на электрической водяной или воздушной бане со скрытыми нагревательными элементами.
Эфир можно перегонять на водяной бане, предварительно нагретой вдали от места перегонки на другом столе. Приемник для эфира нельзя помещать рядом с включенной электроплиткой или горящей горелкой.
3.Перед разборкой приборов, в которых содержаться легковоспламеняющиеся вещества, следует потушить горелки, находящиеся по близости.
4.Нельзя проводить перегонку досуха, так как многие вещества (диэтиловый эфир, диоксан) образуют взрывчатые пероксиды.
5.Диэтиловый эфир, диоксан и другие простые эфиры перед использованием необходимо проверять на содержание в них пероксидов.
6.Категорически запрещается выливать эфир, эфирные растворы и другие легковоспламеняющиеся вещества в раковины. Эти вещества сливаются в специальные склянки, хранящиеся в вытяжных шкафах.
7.Перекристаллизацию из легковоспламеняющихся растворителей следует проводить в колбах, снабженных обратным холодильником.
8.Особую осторожность необходимо соблюдать при работе с металлическим натрием. Все работы с натрием должны проводиться в защитных очках и резиновых перчатках вдали от открытых водопроводных кранов и приборов с действующими водяными холодильниками.
Нельзя допускать соприкосновения натрия с водой – в результате бурной реакции может произойти взрыв и пожар.
Хранить натрий нужно под слоем керосина в банке, закрытой корковой пробкой.
Резать натрий следует на сухой фильтровальной бумаге вдали от других работающих.
Нельзя брать металлический натрий руками, а только пинцетом или щипцами.
Категорически запрещается бросать обрезки натрия в раковины и оставлять их на столе открытыми. Обрезки натрия собирают в банку с керосином.
9.Все работы с ядовитыми и сильнопахнущими веществами должны проводиться в вытяжном шкафу. Шторка секций шкафа, где ведется работа, должна быть поднята лишь на одну треть. Шторки у не-используемых секций шкафа следует опустить. Категорически запрещается просовывать голову внутрь вытяжного шкафа.
6
10.Работы с бромом можно проводить только в вытяжном шкафу, обязательно в резиновых перчатках, защитных очках или маске.
Необходимо помнить, что бром действует на слизистые оболочки и при попадании на кожу дает трудно заживающие ожоги.
11.При работе с кислотами и щелочами необходимо помнить следующее:
- работать с кислотами и щелочами нужно в защитных очках и резиновых перчатках;
- категорически запрещается кислоты и щелочи затягивать ртом в пипетки;
- разбавлять серную кислоту можно только, прибавляя небольшими порциями кислоту к воде, при перемешивании и охлаждении;
- смешивать азотную кислоту с серной, приливая азотную к серной небольшими порциями;
- растворять гидроксиды натрия и калия следует медленным прибавлением их к воде небольшими порциями; запрещается брать твердую щелочь руками.
Тушение местного пожара и горящей одежды
Каждая лаборатория оснащена средствами противопожарной защиты: ящиком с песком, кошмой (противопожарным одеялом), огнетушителем.
1.При возникновении пожара необходимо выключить газ и электроприборы, убрать все горючие вещества подальше от огня, засыпать пламя песком, прикрыть противопожарным одеялом или воспользоваться огнетушителем.
Не следует заливать пламя водой, так как во многих случаях это приводит лишь к расширению очага пожара.
2.Если на ком-то загорится одежда, пострадавшего следует облить водой или немедленно повалить на пол и накрыть противопожарным одеялом.
Можно потушить на себе горящую одежду быстрым перекатыванием по полу.
3.В случае сильного пожара следует вызвать пожарную команду по телефону 01.
Первая помощь при несчастных случаях
Каждый работающий должен знать, где в лаборатории находится аптечка, содержащая все необходимое для оказания первой помощи.
1.При термических ожогах нужно немедленно делать длительную примочку обожженного места 0,5%-ным раствором перманганата калия или этиловым спиртом, затем нанести на пораженный участок мазь от ожогов.
2.При ожогах кислотами пораженное место необходимо промыть 10-15 минут проточной водой, а затем 3%-ным раствором гидрокарбоната натрия
(NaHCO3).
7
Если поражены глаза, то после длительного промывания водой их следует обработать 2-3%-ным раствором гидрокарбоната натрия и обязательно направить пострадавшего к врачу.
3.При ожогах едкими щелочами нужно хорошо промыть обожженное место проточной водой, затем 1%-ным раствором уксусной кислоты.
При попадании щелочи в глаза необходимо их сразу же обильно промыть водой, затем 0,5%-ным раствором борной кислоты и немедленно, обратиться к врачу.
4.При попадании брома на кожу следует быстро смыть его спиртом или обработать пораженное место раствором тиосульфата, а затем смазать глицерином или мазью от ожогов.
Вслучае вдыхания паров брома следует обильно смочить спиртом вату
иглубоко вдыхать пары спирта, а затем выйти на свежий воздух.
5.Если на кожу попадает разъедающее органическое вещество, то промывание водой в большинстве случаев бесполезно. Нужно промыть пораженный участок подходящим растворителем (спиртом, эфиром). Применять растворитель надо по возможности быстро и в большом количестве.
6.При ожогах фенолом пораженное место обрабатывают спиртом.
7.При порезах стеклом следует удалить из раны видимые осколки стекла, обработать рану 3%-ным спиртовым раствором йода и наложить повязку. При сильном непрекращающемся кровотечении, особенно в случае повреждения артерии, рекомендуется наложить жгут выше раны, после чего пострадавшего направить к врачу.
Занятие 1.Протолитические реакции. Гетерогенные реакции в растворах электролитов.
Цель занятия:
Познакомить студентов с кислотностью и основностью; с условиями образования и растворения осадков.
Студент должен знать:
Протонная теория кислот и оснований. Теория Льюйса; константы кислотности, основности. Ионное произведение воды, рН растворов; гидролиз солей, степень и константа гидролиза. Амфолиты. Кислотность желудочного сока. Константа растворимости. Общая константа совмещенного гетерогенного равновесия. Условия образования и растворения осадков. Явление изоморфизма. Применение реакции осаждения в клиническом анализе, в анализе фармацевтических препаратах.
Студент должен уметь:
Расчитывать рН растворов, записывать уравнение гидроза различных
солей.
8
1.1.Основные типы химических реакций.
Аналитическими являются только те реакции, которые сопровождаются каким-нибудь внешним эффектом, позволяющим установить, что химический процесс связан с выпадением осадка, изменением окраски анализируемого раствора, выделением газообразных веществ.
Вклассической химии реакцию между кислотой и основанием с образованием соли и воды называют кислотно-основной реакцией.
Окислительно-восстановительными называют реакции, идущие с изменением степени окисления атомов. Реакции, в результате которых происходит образование комплексных соединений, называют реакциями
комплексообразования.
Также часто используются процессы осаждения и растворения. Реакции осаждения - это реакции, идущие с выпадением осадков. Наоборот, реакции, сопровождающиеся растворением осадков, называются реакциями растворения. Цель операции - количественно перевести определяемую весовую часть в малорастворимое соединение - в осаждаемую форму.
1.2.Теория кислот и оснований.
Внастоящее время не существует однозначного определения понятий кислоты и основания, которое в равной степени можно было бы использовать для характеристики кислотно-основных взаимодействий в любых растворителях. Для характеристики электролитов в водных растворах в настоящее время можно использовать понятия кислоты и основания, данные Аррениусом.
Согласно теории Аррениуса кислотой считается соединение, при электролитической диссоциации которого образуются катионы водорода, а основанием считается соединение, в результате диссоциации которого образуется гидроксид-ион. Амфолитом (амфотерным гидроксидом) называют электролит, диссоциирующий в растворе с образованием как катионов водорода, так и гидроксид – ионов. К амфолитам относят гидроксиды цинка, алюминия, хрома и других аммфотерных элементов, а так же аминокислоты, белки, нуклеиновые кислоты.
Таким образом, свойства кислот обусловлены наличием в их растворах водород - ионов, а свойства оснований - присутствием в их растворах гидроксид - ионов. Однако такой взгляд на кислоты и основания применим только для водных растворов. Ограниченность понятий кислоты и основания,
данных Аррениусом, можно проиллюстрировать примерами:
1.Молекула NH3+ не содержит иона ОН-, а молекула СО2- иона H+, однако в водном растворе первая проявляет свойства основания, а вторая - кислоты.
2.Безводный хлорид водорода, состоящий только из молекул, реагирует с безводными основаниями.
9
3. Многие электролиты, содержащие водород, в одном растворителе диссоциируют как кислоты, а в другом – как основания. Например, СН3СООН в воде – слабая кислота:
СН3СООH 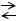 СН3СОО-+ H+
СН3СОО-+ H+
а в жидком фториде водорода - основание:
НF+СН3СООH 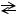 СН3СООH2++F-
СН3СООH2++F-
Исследования подобного типа реакций, и в особенности реакций, протекающих в неводных растворителях, привело к созданию более общих теорий кислот и оснований.
Протонная теория кислот и оснований. В 1923г И. Бренстед и Т.
Лоури разработали протонную теорию кислот и оснований. Согласно этой теории
кислотой называют любое вещество, молекулярные частицы которого (в том числе ионы) способны отдавать протон, т.е. быть донором протонов;
основанием называют вещество, молекулярные частицы которого (в том числе и ионы) способны присоединять протоны, т.е. быть акцептором протонов.
Такие определения кислот и оснований позволяют включать в их число не только молекулы, но и ионы. Например, карбонат-ион согласно протонной теории является основанием, т.к. в водном растворе он присоединяет протон:
СО32- + H+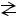 HCO3-
HCO3-
Согласно протонной теории кислоты подразделяют на три типа:
1. Нейтральные кислоты, например HCl, H2SO4, H3PO4 и др.
H2SO4 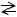 H++ HSO4-
H++ HSO4-
2.Катионные кислоты, представляющие собой положительные ионы, например NH4+ , Н3О+:
NH4+ 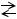 NH3+Н+
NH3+Н+
3.Анионные кислоты, представляющие собой отрицательные ионы,
например, HSO4-, H2PO4-, HPO42- и др.:
HSO4- 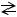 H++ SO42-
H++ SO42-
Подобного типа классификация имеется и для оснований:
1. Нейтральные основания, например, NH3,Н2О, С2Н5ОН и др.:
10
