
- •Глава1.Обзорлитературы 11
- •Глава2.Материалыиметодыисследования 36
- •Глава3.Результатысобственных исследований 55
- •Глава1.Обзорлитературы
- •РазвитиепредставленийодиагностикеГм
- •Гистологическоеисследование
- •КритериидиагностикиГм
- •Глава2.Материалыиметодыисследования
- •Общаяхарактеристикабольных
- •Проведениедиагностическойбиопсиикожи
- •Гистологическоеисследование
- •.Непрямойиммуногистохимическийметодисследования
- •2.4Статистическийанализ
- •Глава3.Результатысобственных исследований
- •Глава4.Заключение
Глава1.Обзорлитературы
РазвитиепредставленийодиагностикеГм
СовершенствованиедиагностикиГМявляетсяактуальнойнаучнойзадачейвнастоящеевремя.Этоопределяетсянеспецифичностьюклиническойкартинызаболеваниякакнаначальнойстадии,посколькуклиническиепроявленияблизкисомногимидоброкачественнымидерматозами[8,10,159],такивпрогрессирующихслучаях, когдаболезньимеетнеклассическоетечение[207].
Вусловияхкожно-венерологическогоотделениявоенногогоспиталяна600коек,главных,центральныхгоспиталяхиВоенно-медицинскойакадемииосуществляетсялечениебольныхБПиГМ.Современныхтенденцииксокращениювременинахождениянастационарномлечениибольныхопределяютнеобходимостьнаиболеебыстрогоустановлениядиагнозаэтихзаболеванийдлярешениявопросаодальнейшемместеиспособахлечениятакихпациентов.
УчитываяотсутствиепатогномоничныхпризнаковГМ,высокуюзначимостьприобретаютинструментальныеметодыисследования.Обзоримеющихсялитературныхданныхпоказал,чтонаходящиесявраспоряжениидерматологаметодыдиагностикиневсегдапозволяютустановитьдиагнозлимфопролиферативныхзаболеваний[65,159, 191,207].
Такимобразом,сохраняетсяактуальностьпоискановыхисовершенствованияимеющихсядиагностическихпроцедур.
Клиническоеобследование
Считается,чтопервоеописаниеГМбылоданов1806годуД.Алиберомподназванием«грибовиднаяфрамбезия»,апозжепереименованона«грибовидный
микоз»,чтоизакрепилосьдонашеговремени[40].Заболеечемдвавеканакопленбогатыйматериал,отражающийклиническиепроявленияГМ.
ВнастоящеевремяГМподразделяютнаклассическуюформу,описаннуюАлиберомидополненнуюБазеномстадиямизаболевания[48],имножествоегоразновидностей.Симптомы,характерныедляпятнистойстадииклассической(Алибера-Базена)формыГМ,детальноописаныивключаютзудящиепятнавариабельнойформыиразмеров,чащемножественные,больше5смвдиаметре,расположенныеназакрытыхотсолнца участкахтеласявлениямипойкилодермииинапоминающие«пергаментнуюбумагу».Длявторой(бляшечной)стадиихарактернопоявлениеуплотненныхшелушащихсякрасно-коричневыхбляшек.Третья(опухолевая)стадияхарактеризуетсяузлами,имеющимисклонностькизъязвлению[18,41,92,105, 153,193].
ВдиагностическомпланенаиболеетруднойявляетсяпятнистаястадияГМ[41,153,193].Необходимоучитыватьособенностьтечениязаболевания,аименнопериодическоенередкоодновременноевозникновениепрогрессированияоднихирегрессадругихвысыпаний, чтоявляетсяважнымдиагностическимпризнаком.
Гистологическоеисследование
СледующимисторическимэтапомизученияисовершенствованиядиагностикиГМявляетсявнедрениегистологическогоисследованиявовторойполовинеXIXвека.ИменносэтоговремениГМсталрассматриватьсякаконкологическоелимфопролиферативноезаболевание,чемуспособствовалиработыHeinrichKobner,XavierGillotиLouisAntoineRanvier,которыеоднимиизпервыхописалигистологическиеособенностилимфомкожи[93].ВXXвекегистологическоеисследованиеГМсталооднимизважнейшихметодовдиагностикиэтогозаболевания[204].НаоснованиигистологическойкартиныпоявиласьвозможностьдифференцироватьГМсдоброкачественными
хроническимидерматозами,имеющимисходныеклиническиепроявления[32,66].
В70-х–90-хгодахXXвекаоднимизосновныхнаправленийизученияГМсталадиагностикаегоначальнойнаименееинформативнойпятнистойстадии.Всоответствиисэтимпредпринималисьпопыткивыделитьдифференциально-диагностическиекритериииразработатьалгоритмдиагностики[179,171,151,183].Полученныерезультатыпозволилилучшеописать иточнееориентироватьсявгистологическихособенностяхстадийГМ,ноневсегдапомогалиобнаружитьначальныепризнаки болезни[205].
СовременныегистологическиекритерииразличныхстадийГМперечисленывтаблице1.1[4, 151, 159,179,184].
Таблица1.1–ГистологическиехарактеристикистадийГМ
Стадия |
Гистопатология |
Пятнистая стадия |
Эпидермис: Пятнистый лихеноидный или полосовидный инфильтратврасширенныхсосочкахдермы.Наблюдаетсяпсориазиформнаягиперплазияэпидермиса,новбольшинствеслучаев эпидермис не изменен. Малые лимфоцитыпреобладают,количествоатипичныхклетоквинфильтратеневелико.Обычновыявляютэпидермотропизмединичныхлимфоцитов, микроабсцессы Потрие встречаются редко.Важнымидиагностическимипризнакамиявляются:наличиевэпидермиселимфоцитовсядромбольшегодиаметра,чемвдермеиобнаружениелимфоцитов,расположенныхцепочкойвдольбазальногослояэпидермиса.ХарактернодляэтойстадииГМотсутствиеилислабовыраженныйспонгиоз.Дерма:Всосочковойдерменаблюдаетсяфиброзсгрубымипучками коллагена и полосовидным или пятнистыминфильтратомизлимфоцитов. |
Бляшечная стадия |
Эпидермис: Наблюдается скопление лимфоцитов в микроабсцессахПотрие,которыечащевстречаютсявэтойстадии. Дерма:Плотныйполосовидныйинфильтратвверхнейчастидермы.Малыецеребриформныеклетки доминируют. |
Опухолевая стадия |
Плотныйузловойилидиффузныйинфильтратповсейдерме иподкожнойжировойклетчатке.Эпидермотропизмможетбытьпотерян. |
Молекулярно-генетическиеметодыисследования
Использованиемолекулярно-генетическихметодовдлядиагностикигрибовидногомикозаактивноразвивается[86].
Группаисследователейв2003г.изучалаДНКсприменениеммикрочиповивыявлилаоколо27генов(включаяонкогеныигеныапоптоза),отличающиесяупациентовсраннимиипозднимистадиямиГМ отздоровыхлюдей[194].Сходноеисследованиебылопроведенодругойгруппойученых,которыетакжевыделелилитрикластерагенов,изменениявкоторыххарактерныдляГМ.Причем,дваизнихвстречаютсяприраннихстадияхГМ,аодин–припоздних[180].
Обнаружено,чтотакиеонкогены,какp16иp53,неизмененывраннихстадияхГМ,ноихэкспрессияменяетсяприпрогрессированиизаболевания[150].НарушенияэкспрессиигеновJUNBиJUNDупациентовсГМбылиобнаруженывнесколькихисследованиях[139,140,141,149].МутациигенаFASтакжесвязываютсГМ[77].
ХромосомныеабберацииприкрупноклеточнойтрансформацииГМвключаютперестройкухромосом1,2,7,9,17и19.Амплификацияидетвследующихлокусаххромосом:1p36,7,9q34,17q24-qter,19,делеция−вучастках:2q36-qter,9p21и17p.Выявленапрогрессиязаболевания,связаннаяспотерейгетерозиготностивспециальномлокусе10хромосомы[139].ОбнаруженаделециягеновсупрессоровопухолиBCL7A,SMACA,DIABLO,RHOFпосредствомсравнительнойгеномнойгибридизации[64].
Мутации,поражающиеCDKN2A,FAS,иJUNBгены,измененияJanuskinase[JAK]/signaltransducer,активаторатранскрипции(STAT)ирецепторысмерти, былитакжевыявленывгруппепациентовсГМ[77,139, 150,186].
FischerисоавторыпосредствомсравнительнойгеномнойгибридизацииобнаружилиубольныхГМнетолькоучасткихромосомсосниженнымиповышеннымсодержаниемхроматинапосравнениюсоздоровымилицами,нои
нашливзаимосвязьэтихизмененийспродолжительностьюжизнивзависимостиотстепениэтихнарушений[86].
Однимизперспективныхнаправлениймолекулярно-генетическихметодовисследованиялимфомкожи,которыйактивноразвиваетсявпоследниегоды,являетсяопределениеэкспрессиимикро-РНК.Микро-РНКпредставляетсобойнебольшойнекодирующийсяучастокРНК.Еефункциязаключаетсявпосттранскрипционнойрегуляцииэкспрессиигенов[147,157].
Определено,чтоэкспрессиямикро-РНКбудетвозрастатьприувеличениипролиферативнойактивностилимфоцитов[124].Микро-РНКимеетподтипы(микро-РНК-155,микро-РНК-203имикро-РНК205).Исследователипришликвыводу,чтоприлимфопролиферативныхпроцессахидетнарушениеэкспрессииразличныхподтиповмикро-РНК,ипоэтимизменениямможносудитьоразвитиидоброкачественногоилиначавшегосязлокачественногопроцесса[166].
НесмотрянамногочисленныеработыпоизучениюгенетическихособенностейбольныхГМ,тольконекоторые[47,107,201,213]былинаправленынавыявлениеизменений,происходящихнаначальномэтаперазвитияГМ,большинствожеисследователейописываютпрогрессирующиестадиизаболевания,когдадиагностикалимфопролиферативногопроцессанепредставляеттрудностей.
Изучениемолекулярно-генетическихособенностейбольныхГМпозволитглубжепроникнутьвпатогенезэтогозаболеванияивпоследствииразработатьтаргентнуютерапию.Ксожалению,внастоящеевремяисследованиявданнойобластинедостаточны,аединственнымприменимымметодомдлядиагностикиГМявляетсяопределениереаранжировкигенаТ-клеточного рецептора.
ОпределениереаранжировкигенаТ-клеточногорецептора
В1975годубританскийбиологEdwinSouthernизобрелновыйметоддлявыявленияопределеннойпоследовательностиДНКвобразце.МетодСаузернблоттингасочетаетэлектрофорезвагарозномгеледляфракционированияДНКсметодамипереносаразделеннойподлинеДНКнамембранныйфильтрдлягибридизации[39,187].Учитывая,чтопрималигнизациилимфоцитовпроисходитреаранжировкагенаТ-клеточногорецептора(ТКР),ипоявляютсямоноклональныелимфоциты,данныйметодсталииспользоватьдлядиагностикиГМ.ПозжеСаузернблотингбылзамененнаПЦРисследованиегенаТКРкакболееспецифичный.
Дальнейшиеисследованияустановили,чтоспецифичностьПЦР,атакжесаузернблоттингадляидентификацииреаранжировкигенаТ-клеточногорецепторадостигает86-95%,тогдакакчувствительность—52%,иесливбляшечнуюиопухолевуюстадииГМклональностьопределяетсяу90%больных,то впятнистую–толькоу50%[23,45,55,210, 211, 213,216].
МоноклональностьТ-лимфоцитовинфильтратаявляетсястабильнымпризнакомтольковопухолевойстадииГМ[7].
Входеопределенияклональностилимфоцитовубольныххроническимидоброкачественнымизаболеваниямикожи,былавыявленагруппа«клональных»дерматозов,прикоторыхпроисходитвыявлениегенаТКР,чтоможетпривестикошибкамвдиагностике[182].ЛожноположительныерезультатывданномслучаеобусловленыналичиемприхроническихдерматозахпревалирующегоклонаТ-лимфоцитов [111,115,138,161].
Такимобразом,нанастоящеевремяналичиеилиотсутствиеклональностиТ-лимфоцитовнеявляетсяэквивалентомзлокачественностиилидоброкачественностинаблюдаемыхпатологическихизмененийвкоже,таккакэтотпараметрнедостаточнокоррелируетсклиническимипризнаками,новместестемонможетиспользоватьсявкачестведополнительногомаркерапридиагностикеГМ[162].
Иммуногистохимическоеисследование
Принципиммуногистохимического(ИГХ)исследованиябылпредложенболее80летназадJ.R.Marrack(1934)изаключаетсявтом,чтовкачествегистохимическихреагентовиспользуютантитела,ккоторымприсоединяютопределенныйфлуоресцентныймаркер(Рисунок1.1).АвторамиметодапоправусчитаетсягруппаисследователейподруководствомA.H.Coons,котораяв1941годувпервыеспомощьюантител,меченныхизоцианатом,выявилаантигеныпневмококковвинфицированныхтканях[72,73].
Однимизважныхоткрытийдлядальнейшегоширокогоиспользованияиммуногистохимическогоисследованиябыловыявлениев1951годуJ.M.Marshallвозможностилокализоватьinvitroмолекулыадренокортикотропногогормонавгипофизеспомощьюантител, меченныхфлуоресцентнымимаркерами[117].
МетодыиспользованияконъюгированныхферментамиантителбылинезависиморазработаныP.K.Nakane,G.B.Pierce(1966)иS.Avrameas,J.Uriel(1966)[1].Наибольшуюпопулярностьполучилпероксидазно-антипероксидазныйметодL.A.Sternbergerссоавторами(1979)[188].Длявизуализацииэнзиматическихмаркероввконцереакцииантиген-антителопроводятгистохимическуюреакцию,врезультатекоторойферментстановится видимымнасветовомуровне.Дальнейшееусовершенствованиеэтойреакциипривелоктому,чтопродуктыреакциибыливидныинаэлектронно-микроскопическомуровне.Привзаимодействиисосмиемонистановилисьэлектронно-плотными[1].
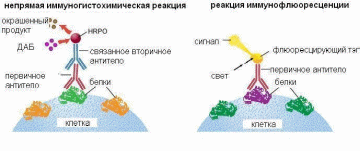
Рисунок1.1Схемапроведениянепрямойиммуногистохимическойреакциииреакциииммунофлюоресценции.
Впоследниегодыприменениеиммуногистохимическихреакцийвморфологииширокоразвивалосьвсвязисразработкойновыхметодовконъюгацииантител,фиксациейтканей,демаскированияантигенов,атакжеиспользованияновыхлампифильтровдляфлуоресцентноймикроскопии[1,16,19,22].
Внастоящеевремянетединогомненияотносительнотого,изкакихТ-лимфоцитовидетразвитиенеопластическихклетокприГМ[36,59].Высказываютсяпредположения,чтофенотиплимфоцитовможетизменятьсявзависимостиотфакторов окружающейсреды[164,165,218,].
Темнеменее,установлено,чтовбольшинствеслучаевклассическийиммунофенотипмалигнизированныхклетокприГМсоответствуетзрелымТ-клеткампамяти:βF1+CD3+CD4+CD5+CD7+CD8-CD45RO+.ВпозднихстадияхГМможетнаблюдатьсяпотеряэкспрессиипан-Т-клеточныхантигеновCD3, CD5иCD7[63].
Исследователипридаютзначениенетолькоиммунофенотипуопухолевыхклеток,ноиихмикроокружению.Считается,чтоклетки,окружающиеопухоль,могутоказыватьвлияниенаразвитиеканцерогенногопроцесса[54,61].
СоотношениеCD4/CD8-лимфоцитов
ОднимизважныхпоказателейдлядиагностикиГМявляетсяопределениесоотношениялимфоцитовсмаркерамиCD4/CD8вкоже.Установлено,чтоупациентовсвоспалительнымизаболеваниямиэтотпоказательбудетгораздониже,чемубольныхраннимистадиямиГМ[159,193].
Дендритныеклетки
Впоследнеевремяпридаютвсебольшеезначениеопределениюподтиповиколичествадендритныхклеток(ДК).Считается,чтоДКвыполняютфункциюрегулированиябалансамеждуиммуннымответомииммунологическойтолерантностью[121,122].Находясьвкоже,ДКпоглощаютчужеродныеантигены(АГ)имигрируютчерезафферентныелимфатическиепутивдренирующиелимфатическиеузлы[177].ВлимфатическихузлахпроисходитпрезентацияАГТ-лимфоцитамприучастииклассических(IиIIклассакомплексагистосовместимости)инеклассических(CD1-семейство)антиген-презентирующихмолекул,следствиемчегоявляетсяпролиферацияидифференцировкаантигенспецифическихТ-иВ-лимфоцитов[46,102, 168,106].
ДКпроисходятизединойстволовойклеткикрови,котораявдальнейшемразвиваетсяподвумпутям:миелоидномуилимфоидному.ПослециркуляциивкровиДКоседаютвпериферическихорганах,втомчислеикоже.МиелоидныйростокдаетначалоклеткамЛангергансаидермальнымДК,алимфоидный–плазмоцитоиднымДК[71,121].
Таблица2.2–МаркерыДКкожи
|
Локализация |
С-типлектина |
TLR |
Маркер |
Клетки |
эпидермис/дерма |
Langerin/ |
TLR1, |
CD11c, |
Лангерганса |
CD207 |
TLR2, |
CD1a, |
|
TLR3, |
E-cadherin |
|||
TLR6 |
||||
Дермальные интерстициальныеДК |
дерма |
CD206, CD209/DC-SIGN |
TLR2, TLR4,TLR5 |
CD1c, CD1a/CD14c,CD11b,CD36, факторXIIIa |
Плазмоцитоидные ДК |
дерма |
CD303/BDCA2 |
TLR1, TLR6,TLR7,TLR9,TLR10 |
CD123, ILT7 |
Укаждоговидаклетокестьхарактерныйнаборповерхностныхмаркеров,определяющийихфенотип.Так,клеткиЛангергансахарактеризуютсяналичиемlangerin/CD207иCD205антигенов,дермальныеДКимеютCD207–CD205+CD209+фенотип,плазмоцитоидныеДК–CD207–CD303+.ДлякаждоготипаДКсвойственноуникальноесочетаниеТолл-подобныхрецепторов(TLR)(таблица2.2)[196].
ВсеподтипыДКвкоженаходятсянаразныхстадияхсозревания.ДляопределениястепенизрелостииспользуютмаркерыCD83иCD208(DC-LAMP).МолекулаCD208являетсялизосом-ассоциированныммембраннымгликопротеином,экспрессирующимсяпридифференцировкеДКвходееесозревания[51,132,169,202].CD83маркируетполностьюзрелыеДК.СуществуетдвеизоформымолекулыCD83:одна–мембрано-связанная,обладающаяиммуностимулирующимисвойствами,другая–растворимая,оказываетпротивоположноедействие,вызываяингибированиеиммунногоответа[154, 155,217].
Обнаруженыизмененияколичестваэтихизоформприразличныхзаболеваниях.ПовышенныезначениярастворимойизоформымолекулыCD83выявленыприхроническойлимфоцитарнойлейкемии,лимфомеизмантийныхклеток,ревматоидномартрите.Некоторыевирусы,например,цитомегаловирусиливируспростогогерпеса,могутблокироватьрецепторыCD83наповерхностиДК,чтоприводиткнарушениюсозреванияэтихклетоки,какследствие,подавлениюиммунногоответаорганизма [163].
Обнаруженыассоциациимеждустепеньюзрелостью,количествомсубпопуляцийДКипрогнозомрядаонкологическихзаболеваний.Установлено,чтоувеличениеколичествазрелыхДКвочагепоражениясмаркеромDC-LAMP+убольныхмеланомойассоциированосотсутствиемметастазоввлимфатическихузлах[83].ПовышеннаяэкспрессиянезрелыхдермальныхDC-SIGN/CD209+-ДКсвязанаснеблагоприятнымпрогнозомприостройлимфобластнойлейкимии.ПрикарциномеклетокпочечногоэпителиявозрастаетколичествоДК[192].При
аденокарциномемолочнойжелезынаблюдаетсяинфильтрациянезрелымиДКсамойопухолиископлениезрелыхДКпоеёпериферии[49].Перечисленныефактысвидетельствуютотом,чтоизучениеподтиповДКиихстепенизрелостизначимодляонкологическихзаболеваний.
ОписановлияниеДКнамикроокружениеприлимфопролиферативныхзаболеванияхкожи.ChuA.исоавторыустановилиповышенноесодержаниеCD1a-позитивныхДКвдермебольныхГМ,чтопозжеподтвердилосьданнымидругихисследователей[97,143,158].MeissnerисоавторыобнаружиликорреляционнуюсвязьмеждуколичествомклетокЛангергансаивыживаемостьюпациентовсГМ,выявивболееблагоприятныйпрогнозприувеличенииколичестваCD1a+-клетоквэпидермисе[144].
ИсследуясодержаниеклетокЛангергансавТ-иВ-клеточныхлимфомахкожи,Der-PetrossianM.исоавторыпришликвыводу,чтоэпидермотропизмопухолевыхлимфоцитовприГМкоррелируетсколичествомклетокЛангергансавинфильтрате[76].Большинствоисследователейненашлиассоциациймеждуколичествомlangerin+-илиCD1a+-клетокивозрастом,полом,ответомнатерапию[97,175,176],новтожевремяобнаруженазависимостьмеждуколичествомдермальныхДК истадиейзаболевания[97].
Былоисследованонетолькоколичество,ноистепень зрелостиДК.Проводяэкспериментinvitro,BergerCLисоавторыустановили,чтоопухолевыелимфоциты,извлеченныеизочаговТ-клеточнойлимфомыкожи,могутрастивкультуредо3-хмесяцевтольковприсутствииснезрелымиДК[54].SchlapbachC.исоавторамибылаобнаруженазначительнаяинфильтрацияпораженнойкожибольныхГМнезрелымиCD209+-ДК[175].
Роль Т-регуляторныхклеток
ОтличительнымпризнакомТ-клеточныхлимфомкожиявляетсяразвитиевыраженногоиммунодефицита,вследствиечегопациентывпозднихстадиях
чащеумираютотинфекционныхзаболеваний,чемотраспространенияопухолевыхклеток.ReinholdU.исоавторамибылоустановлено,чтолимфоциты,изолированныеизкожи,проявляютиммуносупрессивныесвойства,оказываяингибирующеевоздействиенапротивоопухолевыйиммунитет.Авторывысказалипредположение,чтоэтовлияниевызывают Т-регуляторныеклетки(Т-рег)[200].
Т-регклеткиявляютсяспециализированнойсубпопуляциейТ-лимфоцитов,котораяобладаетиммуносупрессивнымисвойствами.Ониподдерживаютгомеостазиммуннойсистемы,подавляяизбыточнуюактивностьэффекторныхТ-клетоквреакцияхсчужероднымиантигенами.СнижениефункцииТ-регсопровождаетсяразвитиемаутоиммунныхзаболеваний,аизбыточнаяактивностьчастонаблюдаетсяпризлокачественныхновообразованиях[125].ДляопределенияТ-регклетоквтканяхприпроведениииммуногистохимическогоисследованияиспользуютмаркерыFOXP3(forkhead boxprotein3) иCD25.
ИзучаясодержаниеТ-регклетоквкожеупациентовсГМ,FriedиCerroniобнаружили,чтоонисоставляютот10%до25%отвсехлимфоидныхклеток.Причем,среднеезначениевпятнисто-бляшечныхстадияхГМсоставило13%,авопухолевую–10.7%.Выявленотакже,чтоучастипациентоввпятнисто-бляшечнойстадиивэпидермиселимфоцитыпредставленытолькоТ-регуляторнымиклетками[67].
БольшоезначениеТ-регклетоквпатогенезеГМподтверждаютисследованияGjerdumисоавторов,которыеустановили,чтоповышенноеколичествоFoxp3+-Т-регклетоксоотноситсясувеличениемвыживаемоститакихпациентов[98].ТакжевисследованииFriedиCerroniпредставленпациент,укоторогонайденыассоциацииповышенногосодержанияFoxp3+-Т-регсдлительнымблагоприятнымтечениемзаболевания[67].
Роль маркеров пролиферации
Выявлениемаркеровпролиферацииклетоккожипредставляетнаучныйинтерес,свидетельствомчемуявляютсяобнаруженныекорреляциимеждууровнемихэкспрессииистадией,прогнозомонкологическогозаболевания[79,88,91,96,117,126].
Циклделенияилипролиферацииклетокразделяютнадвеосновныеточки(checkpoints)SиMидвеподготовительныеточки–G1иG2(Рисунок1.5).Нарушенияводнойилинесколькихфазах,контролирующихклеточныйцикл,лежитвоснове формированиязлокачественныхопухолейиихпрогрессирования.
ПриГМ,несмотрянаегомедленноеразвитие,такжепроисходитнарушениенормальногоцикладеленияклеток,следствиемчегоявляетсяклональнаяпролиферацияТ-лимфоцитов[110, 112, 195].
SточкаопределяетсякакмоментрепликацииДНК.ПолностьюдублированныехромосомыразделяютсявядрахкаждойиздвухдочернихклетоквовремямитозавточкеM.ВовремяG1иG2фазпроисходитсинтезклеточныхбелков,необходимыхдляосуществлениясоответствующейфазыклеточногоделения[1].
Дляустановленияуровняпролиферативнойактивностиклетокорганизмаиспользуютрядмаркеров–участниковклеточногоцикла.НаиболеечастоопределяемымиизнихявляютсяпротеинKi-67,циклинD1ибелокMCM[MiniChromosomeMaintenanceprotein)[90, 101,109, 127,135].
МолекулаKi-67являетсяуниверсальныммаркером,чтообусловленоееприсутствиемвклеткетолькововремяпроцессаделенияиразрушениемвтечение1,5–2часовпослеокончаниямитоза.ДетекциюKi-67используютдляустановлениядиагнозаиоценкипрогноза рядаонкологическихзаболеваний[1].
Прилимфопролиферативныхзаболеванияхкоживысокоезначениеиндексапролиферативнойактивностиопухолевыхклетоккоррелируетсплохимпрогнозомубольныхспервично-кожнойдиффузнойкрупноклеточнойВ-
клеточнойлимфомой[108].Обнаружено,чтоуровеньэкспрессииКi-67увеличиваетсяприпрогрессированииГМ[79].ВисследованииGambichlerT.исоавт.показано,чтоэкспрессиямаркераКi-67вкожедостоверноотличаетсяупациентовсГМIIBстадииибольныхБП,ноупациентовсГМI-IIAстадиейиБПневыявленостатистическизначимыхразличийэтогопоказателя[91].
Определениедругихиммуногистохимическихмаркеров
ДлядиагностикираннегоГМметодомИГХисследованияврекомендацияхподиагностикераннихформГМ(Таблица2.4)предложеновкачестведиагностическогокритерияснижениеэкспрессиимаркеровCD2,CD3,CD5,CD7[159].Врядеслучаевобъективнаяоценкаданныхпоказателейзатруднена[193].
Бляшечныйпарапсориазиегоотношениекгрибовидномумикозу
Теснуюсвязьс ГМимеетспектрзаболеваний,определяемыхвотечественнойлитературетермином«парапсориаз»[26,11,37].Впервыеэтотерминбылиспользованв1902годуфранцузскимдерматологомЛ.Брокомдляхарактеристикирядазаболеванийсосходнойклиническойкартиной[60].Онвключалвсебя:
питириазислихеноидес«pityriasislichenoides»,
бляшечныйпарапсориаз «plaqueparapsoriasis»,
лихеноидныйпарапсориаз «parapsoriasislichenoides».
Посовременнымпредставлениямвпонятие«парапсориаз»входитдвазаболевания:крупнобляшечныйимелкобляшечныйпарапсориаз,отличающиесяклиническойкартиной,течениемипрогнозом[82,181].Остальныеформызаболеваниябылиобъединенывдругиегруппы(например,бывший“parapsoriasislichenoides”),илисталиобособленнойновойнозологией(например,pityriasislichenoidesetvarioliformisacutaetchronica)[27,38, 62, 63, 87, 113,174].
Крупнобляшечныйпарапсориазхарактеризуетсяпятнистымиэлементамибольше6смвдиаметре,локализующимисянаягодицах,нижнейчаституловища,наверхнихучасткахбедер,внутреннейповерхностиверхнихконечностейинаучастках,недоступныхдлясолнечныхлучейсчастымиявлениямиатрофииипойкилодермии[197,148].КрупнобляшечныйпарапсориазбольшинствомотечественныхизарубежныхученыхпризнаетсяначальнойстадиейГМ[38,116,120,129,152,174,70]ивыделенВсемирнойорганизациейздравоохранениякак
«предзлокачественныйвоспалительныйдерматозстенденциейразвитияГМв50%случаев»[131].
Мелкобляшечныйпарапсориазпредставляетсобойвоспалительноезаболеваниекожи,проявляющеесяхорошоочерченнымирозеолезно-эритематознымипятнами,размерами1-6см.Высыпаниячащебываютбезсубъективныхощущений,имеютсклонностькраспространениюирегрессу[28,29,30,31,50].
Нетединогомненияотносительнодоброкачественностимелкобляшечногопарапсориаза.ВтовремякакоднагруппатакихавторитетныхученыхкакBurg,
Degosидр.считаютегодоброкачественнымдерматозом[62,75,146,170,198],другаягруппа,стакимиизвестнымиисследователямикакSanchez,Ackerman,придерживаетсямненияовозможноймалигнизацииэтогозаболевания[171].
Имеетсянесколькопубликаций,демонстрирующихразвитиеГМизмелкобляшечногопарапсориаза[50,198],нокрупномасштабныхисследований,подтверждающихфактпереходамелкобляшечногопарапсориазавГМ,нет.
Дляпроведениядифференциальнойдиагностикимелкобляшечного,крупнобляшечногопарапсориазаиГМиспользуетсяклинический,гистологический,ИГХимолекулярно-генетическийметоды[100,165,133,123,178,189].Былипредложеныкритерии,позволяющиепровестидифференциальнуюдиагностикумелкобляшечногопарапсориазаотГМ(Таблица2.3)[62,34].
Таблица2.3–Дифференциально-диагностическиепризнакимелкобляшечногопарапсориазаигрибовидногомикоза
|
Мелкобляшечныйпарапсориаз |
Грибовидныймикоз |
Клиническаякартина |
<6смвдиаметре,нетпрогрессии |
>6смвдиаметре,естьпрогрессия |
Внекожноераспространение |
Нет |
Часто |
Стадированиепроцесса |
Необязательно |
Необходимо |
КлональнаяреарранжировкагенаТ-клеточногорецептора |
Редко |
Почтивсегдавпрогрессирующихстадиях |
Сочетаниесдругимилимфомами |
Неописано |
Описанонесколькослучаев |
Возможнаятрансформациявболеезлокачественную лимфому |
Никогда |
Частонапозднихстадиях |
Лечение |
Наружное |
Наружноеи/илисистемное |
Учитываяотсутствиечеткихклиническихигистологическихданных,способныхдифференцироватьмелкобляшечныйикрупнобляшечныйпарапсориазы,рядисследователейпредпринялипопыткипримененияИГХисследованиядлядифференциальнойдиагностикиэтихзаболеваний.
ГруппаученыхизИталииисследовалараспределенияCD1a+-дендритныхклетокубольныхГМ,мелкобляшечнымпарапсориазом,лимфоматоиднымпапулезомиВ-клеточнойлимфомойкожи.БылавыявленазначительнаяэкспрессиямолекулCD1aиCD3нетольковкожеубольныхГМилимфоматоиднымпапулезом,ноиупациентовсмелкобляшечнымпарапсориазом.Втожевремя,экспрессияданногомаркераубольныхВ-клеточнойлимфомойбыланиже[158].
Zaybekисоавторыопределялисодержаниевкожебольныхмелкобляшечнымпарапсориазом:HLAClassII,CD1a,CD4,CD8,CD44,CD45иCD68маркеров.ВыявленозначительноепреобладаниеCD1a+-клетоквэпидермисеидермебольныхмелкобляшечнымпарапсориазом.Такжеопределено,чтоколичествопозитивныхCD4,CD8иCD45клетоквкожебольныхмелкобляшечнымпарапсориазомзначительновыше,чем уздоровыхлиц[215].
Очевидно,чтопациентысмелкобляшечнымикрупнобляшечнымпарапсориазомнуждаютсявдальнейшемиммуногистохимическомисследованиидляболееглубокогоизученияпатогенезаэтихзаболеваний.
