
3 курс / Общая хирургия и оперативная хирургия / Справочник_хирурга_Раны_и_раневая_инфекция_Абаев_Ю_К
.pdfEst modus in rebus (мера должна быть во всем).
Гораций
Глава X
МЕТОДЫ КОНТРОЛЯ РАНЕВОГО ЗАЖИВЛЕНИЯ
Для объективной оценки процесса раневого заживления используются различные методы контроля — клинические, лабораторные и инструмен тальные. Применение дополнительных методов контроля позволяет объек тивизировать клиническую оценку заживления раны, избрать рациональный метод лечения и, в конечном счете, способствовать ускорению процесса за живления раны и выздоровлению пациента.
КЛИНИЧЕСКИЕ МЕТОДЫ
Клинические симптомы воспаления, характеризующие очаг инфекции мягких тканей, хорошо известны со времен А. Цельса и К. Галена.
Температура тела. Температура тела является одним из существенных крите риев оценки раневого процесса. Последовательное ее снижение свидетельствует о нормальном течении заживления. Напротив, сохранение на высоком уровне, стой кий субфебрилитет или повышение температуры говорят о развитии местных или общих осложнений.
Боль. Боль — один из наиболее «ощутимых» симптомов воспаления, особенно выраженный при прогрессировании воспалительного процесса. Механизм развития болевого синдрома обусловлен раздражением окончаний чувствительных нервных волокон и связан с их «прямым» повреждением в случае травмы или воздействием на них воспалительного экссудата, содержащего биогенные амины. Источником боли, кроме того, является повышенное внутритканевое давление, усиливающийся ацидоз и локальная гиперкалиемия.
Характер боли отчасти зависит от вида возбудителя, который нередко опреде ляет местные особенности воспалительного процесса. Так, для анаэробной инфек ции характерна внезапно появляющаяся острая «распирающая» боль, быстро рас пространяющаяся по ходу отечных тканей. Постоянная пульсирующая боль сопро вождает развитие флегмон мягких тканей. Болевые ощущения в зоне очага воспа-
Глава X. Методы контроля раневого заживления |
1 4 1 |
ления могут постепенно стихать по мере формирования абсцесса с хорошо выра женной пиогенной капсулой. В этих случаях даже пальпация области поражения не вызывает выраженных болевых ощущений.
Изменение окраски кожи. Изменение цвета кожи в зоне воспаления появля ется обычно в виде очаговой гиперемии, возникающей вследствие локальных гемодинамических нарушений. Если инфекция мягких тканей вызвана гемолитичес ким стрептококком, то окраска чаще принимает цианотичный оттенок с наличием кровоизлияний. В случае развития газовой инфекции окраска кожи может быть не изменена (субфасциальные формы) или она приобретает синюшный или жел товато-коричневый оттенок (эпифасцнальная форма) с крепитацией газа при пальпации.
В отдельных случаях при осмотре можно обнаружить, что от очага гиперемии кожи в зоне очага инфекции краснота расширяется по ходу лимфатических сосу дов; «шнуры» такой гиперемии болезненны при пальпации. Также пальпируются увеличенные, болезненные регионарные лимфоузлы. Лимфангоит и регионарный лимфаденит являются проявлением острого, нередко гнойного воспалительного процесса. При анаэробной инфекции региональный лимфаденит может не наблю даться — из-за скорости распространения воспалительного процесса лимфоузлы не успевают отреагировать.
Отек мягких тканей. Отек тканей является важнейшим признаком воспале ния. По скорости и площади его распространения можно судить не только о форме очага инфекции, виде и вирулентности возбудителя, но и прогнозировать течение воспалительного процесса в процессе лечения.
Так, развитие анаэробной инфекции часто сопровождается быстро нарастающим отеком тканей. Распространение отека преимущественно происходит в проксималь ном направлении от раны. Наличие отека мягких тканей без четких границ являет ся характерным признаком флегмоны, в то время как наличие его контура свиде тельствует об абсцессе.
После адекватно проведенной хирургической обработки очага инфекции к 2-3 сут лечения перифокальный отек мягких тканей должен практически исчезнуть. Если в эти сроки отек тканей сохраняется, можно предположить наличие гнойного затека или неадекватно проводимого местного лечения.
Очаговый некроз. Наличие нежизнеспособных тканей в ране является неотъем лемым признаком гнойно-некротической фазы течения воспалительного процесса. Характер некротических тканей в ране во многом зависит от микрофлоры, каждый вид которой вызывает специфические ферментативные повреждения.
Так, некротические ткани в очаге воспаления стафилококковой инфекции име ют зеленоватый или желтоватый оттенок, относительно прочно фиксированы, одна ко легко удаляются скальпелем. При наличии протея или кишечной палочки некро тические ткани грязно-серого цвета, рыхло фиксированы. Если же в ране присут ствует палочка сине-зеленого гноя, то зона некроза прочно фиксирована, тусклого цвета и с трудом удаляется скальпелем.
1 4 2 |
Инфекция и рана |
Некротические изменения в ране, вызванные анаэробной инфекцией, многооб разны, поэтому их группируют в следующие формы:
•клостридиальный мионекроз — характеризуется поражением мышц с мини мальными изменениями поверхностных тканей. Мышцы напоминают вид «ва реных», без четкой линии отграничения поражения. Одновременно развива ется анаэробный фасциит, при котором фасции становятся серовато-белого цвета и теряют характерный блеск;
•клостридиальный целлюлит — проявляется ранним изменением цвета кожи («белая рожа») с последующим появлением на ней сине-багровых пятен. Под кожная клетчатка тусклая, серо-желтого цвета, не отечна, не кровоточит;
•смешанная форма некроза — характеризуется одновременным поражением всех тканей в очаге воспаления.
'•• раны, при наличии неспорообразующей анаэробной микрофлоры, отличают ся обилием некротических тканей серого или серовато-желтого цвета, неред ко с гнойным отделяемым и неприятным запахом.
Характер отделяемого. Отделяемое из раны является продуктом жизнедея тельности микроорганизмов и местных защитных реакций и позволяет косвенно судить о виде микрофлоры — возбудителе инфекции. Для стафилококковой инфек ции характерно отделяемое зеленовато-желтого цвета, густой консистенции. В ра нах, где источником нагноения является кишечная палочка, гнойное отделяемое в большом количестве, коричневато-серого цвета без запаха. Неприятный запах, ко торый нередко определяют как «колибациллярный», характеризует всегда присут ствие анаэробной микрофлоры.
Гнойное отделяемое при протейной инфекции своими характеристиками напо минает кишечную палочку — жидкое, серовато-коричневого цвета, но отличается примесью пузырьков газа с неприятным запахом, т.к. протей является факультатив ным анаэробом.
Раны, инфицированные палочкой сине-зеленого гноя, имеют скудное серозное отделяемое со специфическим запахом и окраской повязки с зеленоватым оттен ком. Однако в случаях, когда штаммы возбудителя потеряли способность вырабаты вать пигмент, малое количество отделяемого в ране делают последнюю «сухой» с наличием прочно фиксированных некротических тканей.
Грануляции. Появление в гнойной ране островков грануляционной ткани явля ется основным признаком перехода раневого процесса в фазу регенерации. Про цесс гранулирования раны является клиническим тестом контроля ее заживления. Грануляционная ткань ярко-розового цвета, сочная, легко кровоточит. При малей шем ухудшении биосинтеза в ране изменяется вид грануляций — они становятся тусклыми, мелкими, покрываются слизистым налетом. В таких случаях необходимо установить причину «болезни» грануляций. Это может быть суперинфекция, недо статок нутриентов (белки, витамины, микроэлементы и т.д.) и др.
Чрезмерно быстрый рост грануляционной ткани может привести к образованию гипертрофического рубца. В тех случаях, когда имеется изолированный избыточ-

Глава X. Методы контроля раневого заживления |
1 43 |
ный рост грануляций в отдельных участках раны, следует думать о наличии ино родного тела в этом месте (лигатура, фрагмент дренажа и т.д.).
Эпителизация раны. Процесс покрытия раневой поверхности эпителием раз вивается параллельно с ростом грануляционной ткани. Эпителизация осуществля ется за счет пролиферации краевого эпителия, из оставшихся островков эпителия и придатков кожи. Всякое замедление роста грануляций ведет к задержке процесса эпителизации. Для объективного контроля скорости эпителизации раны предложе ны специальные методики.
Планиметрия
Планиметрические методы исследования скорости эпителизации раны основа ны на изменении ее площади в единицу времени. В клинической практике в этих целях широкое распространение получил тест Л.Н. Поповой (1942). На рану поме щается стерильная пластинка целлофана и на нее наносится контур раны. Рисунок переносится на миллиметровую бумагу и подсчитывается площадь раны.
Измерение повторяется через несколько суток и вычисляется процент уменьше ния площади раневой поверхности за сутки по отношению к предыдущему резуль
тату по формуле |
, где S — величина площади раны при предшеству |
ющем измерении; Sn -- величина площади раны в настоящий момент; t — число суток между измерениями. При нормальном течении заживления суточное умень
шение площади раны составляет 4%.
Существует весовой метод определения площади раны" по В. Hejda (1963) и ряд его модификаций. Возможно определение площади ран при помощи курвиметра (В.Ф. Хотинян, 1983).
ЛАБОРАТОРНЫЕ МЕТОДЫ
Лабораторные методы контроля включают исследование общего анализа крови с подсчетом лейкоцитарного индекса интоксикации по Кальф-Калифу, биохимичес кое, бактериологическое и цитологическое исследования.
Общий анализ крови
О наличии или угрозе осложнений объективно свидетельствуют изменения в общем анализе крови — повышение СОЭ, лейкоцитоз, сдвиг формулы влево, лимфопения, в тяжелых случаях — анемия. При нормальном течении процесса раневого заживления эти показатели должны нормализоваться к 6-7 суткам после операции.
Определенное диагностическое значение имеет показатель Кальф-Калифа — эмпирически выведенная формула лейкоцитарного индекса интоксикации (ЛИИ).
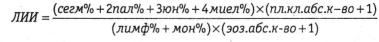
1 4 4 |
Инфекция и рана |
|
t |
где миел — миелоциты; юн — юные; пал — палочкоядерные; сегм — сегментоядерные; пл.кл. — плазматические клетки; лимф — лимфоциты; мон — моноци ты; эоз — эозинофилы.
При гладком течении послеоперационного периода ЛИИ равен 0,6+0,09; если он превышает 1,4, то, как правило, это свидетельствует о развитии осложнений (С. Верник, 1972).
Биохимическое исследование
Биохимическое исследование раневого экссудата обычно включает в себя рНметрию и определение общего белка гнойного отделяемого. У большинства больных после вскрытия гнойного очага в ране определяется ацидоз — рН = 5,5-6,5. В ходе заживления рН постепенно сменяется компенсированным ацидозом или алкалозом. В 30% случаев реакция отделяемого бывает нейтральной или щелочной. Самостоя тельного значения определение рН, как правило, не имеет, что обусловлено местным применением лекарственных средств, изменяющих кислотность раневой среды.
Биохимическое исследование биоптатов раны позволяет определить в ее тка нях ряд компонентов, количественное изменение которых в динамике дает возмож ность судить о характере раневого процесса. В гомогенате изъятой ткани определя ют: общий белок, содержание ДНК и РНК, растворимые и нерастворимые фракции коллагена и гексозаминов, а также неколлагеновые белки.
Количественное определение общего белка проводят по методу Лоури (1965). Содержание ДНК и РНК определяют методом Шмидта и Тангаузера в модификации Н.Г. Трудолюбовой (1977). Определяют как общее содержание РНК, так и ее количе ство в отдельной клетке. Вычисляют показатель «отношение РНК/ДНК», отражаю щий биосинтетическую активность клеток.
Определение содержания коллагеновых белков проводят по оксипролину мето дом Штегемана в модификации Л.И. Слуцкого (1969). Гексозамины определяют по ме тоду Эксли в модификации Л.И. Слуцкого (1969). Содержание неколлагеновых белков вычисляют по разности между содержанием общего белка и коллагеновых белков.
Определение содержания белка в раневом отделяемом имеет диагностическую и прогностическую ценность при анализе заживления ран. При неосложненном процессе отмечается постепенное снижение количества белка в раневом отделяе мом — от 12-24 до 3-6 г/л. Повышение этого показателя, как правило, является признаком гнойного осложнения.
Данные определения белка в раневом отделяемом приобретают прогностичес кое значение при сопоставлении его с уровнем белка плазмы. М.Ф. Мазурик (1984) предложил прогностический коэффициент (ПК) направленности течения раневого процесса:

Глава X. Методы контроля раневого заживления |
1 4 5 |
где ОБП — общий белок плазмы; ОБРО — общий белок раневого отделяемого.
При благоприятном течении раневого процесс ПК составляет 1,2-1,3. Снижение этого показателя свидетельствует о развитии локальных гнойных осложнений.
Для исследования показателей местного гемостаза используют методику (В.П. Ски петров, 1969), основанную на действии тканевых экстрактов на процесс гемокоагуляции донорской плазмы. Данные активности тканевого гемостаза грануляций от крытых ран (уровень активности фибринолиза, активность XIII фактора, уровень свободного гепарина и концентрация продуктов деградации фибриногена) исполь зуют для суммарной оценки характера процессов репарации и протеолиза на ткане вом уровне.
Материалом исследования является грануляционная ткань открытых ран. После обработкираны изотоническим раствором хлорида натрия иссекаются кусочки гра нуляционной ткани 0,15-0,25 см3 и готовят экстракты из расчета 100 мг ткани на 1 мл забуференного изотонического раствора натрия хлорида (рН 7,4). Биоптаты гомогенизируются. Полученный гомогенат центрифугируется 1500 об/мин в'течение 5 мин. Образующаяся надосадочная жидкость используется для исследований.
Фибринолитическую активность определяют по методу Ковальского, Невяровского и Капец; свободный гепарин и тромбиновое время по Ш. Сирман; тромботест — по методу Фуента Ита; активность XIII фактора — по способу В.П. Балуда; определение продуктов деградации фибриногена (ПДФ) — по способу Невяровского иГуревича.
Особое внимание уделяется исследованию активности фибринолиза (XIII фак тор) и уровню продуктов деградации фибриногена — факторам, наиболее ответ ственным за полноценную репарацию в ране. В фазе воспаления и при замедлен ном заживлении активность XIII фактора находится на низком уровне (20-45 с). Такой же уровень активности отмечается при развитии в ране гнойных осложне ний. При нормальном течении раневого процесса в фазе репарации этот показатель возрастает более чем в два раза (70 с).
Фибринолитическая активность грануляционной ткани также зависит от харак тера раневого процесса. При нормальном течении заживления в тканях раны обна руживается высокое содержание ингибитора плазминогена и соответственно низ кая фибринолитическая активность (до 200 мин). При вялом течении раневого процесса, развитии гнойных осложнений возрастают активность плазминогена и фибринолитическая активность плазмы. В соответствии с этим изменяется и со держание в ткани ПДФ. В первой фазе раневого заживления он достигает 1 г/л, во второй — обычно бывает ниже 0,2 г/л. При развитии гнойных осложнений уровень ПДФ обычно составляет 0,6-0,8 г/л.
Методами гистохимического анализа в раневых биоптатах изучаются фермен ты: кислая и щелочная фосфатаза по методу Гомори, сукцинатдегидрогеназа по ме-
1 4 6 |
Инфекция и рана |
тоду Пахласа, АТФ-аза по методу Такуечи, лактатдегидрогеназа. Липиды окрашива ются суданом-Ш, кислые мукополисахариды — альциановым и толуидиновым си ним. Гистохимические критерии функциональной активности фибробластов позво ляют более точно оценить процесс регенерации в ранах. Фибробласты в хорошо регенерирующих ранах отличаются высокой функциональной активностью (нали чие в цитоплазме РНК, высокая активность фосфатазы).
В раннем периоде развития раневого процесса в цитоплазме фибробластов не содержаться липиды, быстро происходит нарастание содержания РНК, увеличива ется активность лактатдегидрогеназы, щелочной фосфатазы, глюкозо-б-дегидро- геназы, в межуточной ткани быстро нарастает количество гликозогликанов (гиалуроновой кислоты, хондроитин-сульфатов А и С) с максимумом накопления на 7-10 сут.
Бактериологическое исследование
Бактериологическое исследование включает в себя качественное и количе ственное изучение раневой микрофлоры в динамике, а также определение чувстви тельности раневой микрофлоры к антибактериальным препаратам (антибиотики, антисептики). Исследование позволяет также судить об эффективности антибакте риального лечения.
В практической работе для предварительной идентификации возбудителя ши роко используется сравнительно простой метод бактериоскопии мазков-отпечатков раны, окрашенных по Романовскому и Гимзе. Метод позволяет легко дифференци ровать палочки от кокков, обнаружить стрептококки и провести идентификацию вульгарных кокков от патогенных стафилококков. При помощи окраски мазков-от печатков по Граму можно дифференцировать грамположительную и грамотрицательную флору.
Принцип метода основан на том, что у микроорганизмов, красящихся грамположительно, генцианвиолет в присутствии йода образует в оболочке стойкое соеди нение фиолетового цвета, не разрушающееся спиртом в течение 30 с. Другие клет ки этим свойством не обладают и спирт обесцвечивает их, а при докрашивании фук сином они приобретают красный цвет (грамотрицательные). К сожалению, при бактериоскопическом исследовании обнаруживаются микроорганизмы, гнездящиеся на поверхности раны, тогда как микрофлора, находящаяся в глубине тканей, не идентифицируется.
Бактериоскопия — простой и быстрый практически прикроватный способ этио логической диагностики. Мазок, окрашенный по Граму в модификации KopeloffBeerman, позволяет в совокупности, с учетом особенностей клинического течения инфекции поставить этиологический диагноз на уровне, достаточном для назначе ния правильной химиотерапии. Важно подчеркнуть значение модификации. Она позволяет получить более представительные данные и меньшее количество «грамвариабельных» результатов. Для окраски по Граму в модификации Kopeloff-
Глава X. Методы контроля раневого заживления |
1 4"7 |
Beerman необходимо пять реактивов: раствор кристалл-виолета, раствор бикарбо ната натрия, раствор йода, смывная жидкость и раствор сафранина.
Рабочий раствор кристалл-виолета готовится из маточного, представляющего смесь 5 г кристалл-виолета и 100 мл 96%-ного этанола. Для приготовления рабо чего раствора 20 мл маточного раствора смешивают с 80 мл дистиллированной воды. Раствор бикарбоната натрия состоит из 5 г соли, 10 мл мертиолята натрия и 90 мл дистиллированной воды. Для приготовления раствора йода смешивают 2 г кристаллического йода и 10 мл I N раствора едкого натра с дистиллированной водой до 100 мл. Смывная жидкость состоит из равных частей ацетона и 96%-ного этанола.
Для приготовления раствора сафранина 2,5 г красителя растворяют в 100 мл 96%-ного этанола. Затем 10 мл полученного раствора (маточного) смешивают с 80 мл дистиллированной воды. Фиксированный мазок окрашивают смесью равных частей (на стекле) растворов кристалл-виолета и гидрокарбоната натрия в тече ние 2 мин. Затем обрабатывают раствором йода также 2 мин. После этого обесцве чивают смывной жидкостью и промывают водой. Далее — двухминутная окраска сафранином и сушка.
К настоящему времени установилось, что оценка микроскопической картины эк ссудата — дело бактериолога. Действительно, в специализированной лаборатории можно было бы сделать более глубокие выводы, но потеря времени, которая неми нуема при отсылке образца в работу на территорию другого подразделения, может обесценить результат. Поэтому в сложившихся сейчас в медицине условиях, тем бо лее, если речь идет о медицине военного времени, бактериоскопию раневых экссу датов необходимо делать самому хирургу. При этом, конечно, надо стремиться дос тигать как можно более детальной дифференциации обнаруживаемых микроорга низмов, что требует не только специальных знаний, но и опыта.
Для исследования качественного состава микробных возбудителей производят посев раневого отделяемого на кровяной агар, среды Чистовича, Сабуро, Эндо и мясопептонный агар. Посевы инкубируют в термостате при температуре 37°С в течение 20 ч, а посевы на средах Чистовича и Сабуро — 48 ч. При получении монокультуры на указанных средах изучают под микроскопом ее морфологию, тинкториальные свой ства возбудителя, его биохимическую характеристику. При выявлении в суточной культуре микробных ассоциаций производят дальнейшую идентификацию всех вы росших колоний, выявляют преобладающую микрофлору и определяют ее свойства.
В последние годы нередко отмечается несоответствие клинических проявлений раневой инфекции данным стандартного бактериологического исследования ран. Микрофлора, высеваемая с поверхности ран, отличается видовым составом от вегетирующих в глубине тканей микроорганизмов, которые и определяют клинические проявления процесса. Идентификация «глубинной» микрофлоры проводится парал лельно с ее количественным определением в биоптате края раны.
Для определения чувствительности микрофлоры к антибактериальным препа ратам материал из раны забирают стерильным тампоном и помещают в стерильную
1 4 S |
Инфекция и рана |
пробирку. Посев производят на сахарный бульон, а также на кровяной агар или среду Эндо. Материал помещают в термостат при температуре 37°С на 24 ч. После этого полученную суточную бульонную культуру в виде монокультуры или мик робных ассоциаций разводят по двухмиллиардному стандарту и засевают в чашки Петри с сахарным кровяным агаром.
Чашки подсушивают в течение 20-25 мин, после чего на поверхность засеянно го агара накладывают «стандартные» диски, пропитанные известными антибакте риальными препаратами. Диски для исследования активности новых препаратов го товят самостоятельно: их вырезают из фильтровальной бумаги диаметром, равным стандартному диску. После пропитывания диском новым антимикробным препара том их накладывают на поверхность засеянного агара в чашках Петри.
Чашки помещают в термостат и через сутки учитывают результаты по зонам задержки роста микробных колоний вокруг дисков, выраженной в миллиметрах. Микробные штаммы считаются устойчивыми к исследуемому препарату, если зона задержки их роста составляет менее 15 мм, чувствительными — при зоне задержки от 15 до 25 мм и высокочувствительными, если зона задержки превышает 25 мм.
Особенностью гнойной раны является то, что вегетирующие в ней возбудители довольно часто выделяются в виде микробных ассоциаций. Поэтому на практике целесообразно проводить определение чувствительности к антибиотикам сразу всей микробной ассоциации и лишь при необходимости выделять отдельные куль туры для определения индивидуальной чувствительности. Для оценки антибиотикорезистентности всей ассоциации по общепринятым методикам затрачивается 48 ч, а при разделении ассоциации на отдельные культуры — 72-96 ч.
Ускоренные методы определения чувствительности микрофлоры к антибиоти кам позволяют сократить сроки, в течение которых клиницисты проводят антимик робную терапию «вслепую», назначая антибиотики широкого спектра действия.
Данные бактериологических исследований являются важнейшим параметром эпидемиологического надзора для построения рационального лечения пациентов с гнойно-воспалительными заболеваниями. Методом выбора для проведения монито ринга лекарственной устойчивости является метод разведений антибиотиков и ан тисептиков в плотной питательной среде, который, по мнению Комитета экспертов по антибиотикам ВОЗ, оказался наиболее стандартным, высокочувствительным и воспроизводимым. Кроме того, к преимуществам этого метода относится также воз можность использования неограниченного круга антимикробных препаратов, эко номия средств и труда при исследовании на одной чашке со средой 25-50 культур бактерий, что обеспечивается различными устройствами по одновременному посе ву групп культур микроорганизмов на питательные среды.
Данные мониторинга, полученные этим методом, позволяют выбирать препара ты с целью проведения эмпирической терапии до получения антибиотикограмм возбудителей, а в случаях эффективной терапии исключить необходимость бакте риологического исследования, стоимость которого возрастает. Использование диф ференцирующей концентрации биологической устойчивости к антисептикам и де-

Главах. Методы контроля раневого заживления |
1 4 9 |
зинфектантам позволяет разделить выборку штаммов на чувствительные и устой чивые и до появления клинически устойчивых вариантов или появления их в боль шим количестве корректировать масштабы применения каждого препарата.
Ограниченно для целей мониторинга может быть использован метод разведе ний препаратов в жидкой питательной среде (громоздкость постановки исследо ваний в пробирках, отсутствие возможности выбора препаратов при использова нии планшет, кювет в автоматизированных системах и приборах, например АТВ Expression, M3-2000 и др.). Неприемлемым для проведения слежения за лекарствен ной устойчивостью возбудителей является также диско-диффузионный метод, на результаты которого оказывают выраженное влияние условия культивирования, толщина слоя агара, посевная доза микроорганизмов и другие факторы. Поэтому результаты, полученные этим методом, могут быть использованы только для выбора препаратов с целью лечения конкретного больного.
Метод количественного определения микрофлоры
Материал из ран больных забирается желатиновыми тампонами, определяется навеска материала, приготавливаются разведения его 1:1000 и 1:10000 и высевает ся каждое разведение на три лунки желточно-солевого агара в чашки Петри для выделения стафилококков и среду Левина — для выделения грамотрицательных бактерий. После инкубации чашек в термостате в течение 24-48 ч подсчитывается число колоний в секторах и их среднее число. Количество микроорганизмов в 1 г материала рассчитывается по формуле
где п — среднее число колоний на секторе; 50 — показатель перерасчета с учетом посевной дозы; к — степень разведения материала.
Бактериологическое исследование анаэробной микрофлоры требует специаль ного оснащения. Важно подчеркнуть, что в исследуемом материале больных с гной но-некротическими процессами анаэробные бактерии, как правило, обнаруживают ся в ассоциации с аэробными микроорганизмами. Поэтому на практике исследуе мый материал должен подвергаться одновременному изучению, как на аэробную, так и на анаэробную микрофлору. Обнаружение анаэробных возбудителей пред ставляет значительные трудности: важную роль играет правильный забор материа ла и его транспортировка в лабораторию.
В специализированных учреждениях этиологические выводы могут быть под креплены газохроматографическим экспресс-анализом раневых экссудатов.
Газовая (газожидкостная) хроматография представляет собой высокочув ствительный метод, суть которого состоит в физико-химическом разделении смесей, сложного состава на отдельные компоненты или в выделении определенных ве ществ из каких-либо проб. Физической сутью хроматографии первоначально была
