
- •II. Оглавление
- •2 Этиология и патогенез
- •3 Эпидемиология
- •4 Кодирование по мкб-10
- •5 Классификация и клиническая картина
- •Виды младенческих гемангиом
- •Стадии развития младенческой гемангиомы
- •Виды мг, требующие особого внимания: phaces-синдром
- •Lumbar-синдром
- •Множественные мг кожных покровов
- •Гемангиомы печени
- •VI. Диагностика
- •1. Жалобы и анамнеза
- •2. Инструментальная диагностика
- •3. Иные диагностические исследования Тириотропный гормон (ттг).
- •Биопсия.
- •4. Дифференциальная диагностика
- •Врожденная гемангиома
- •Капошиформная гемангиоэндотелиома (кгэ)
- •Тафт-ангиома
- •Пиогенная гранулема
- •Лимфатическая мальформация.
- •Артериовенозная мальформация
- •Изъязвления
- •Кровотечения.
- •Косметические дефекты
- •VII. Лечение
- •1 Системная терапия
- •Способы дозирования препаратов
- •Побочные действия -адреноблокаторов
- •Абсолютные противопоказания:
- •Относительные противопоказания или группы риска по осложнениям на системную терапию -адреноблокаторами.
- •Обследование перед началом терапии -адреноблокаторами
- •Пропранолол:
- •Мониторинг
- •Правила кормления ребенка во время терапии
- •Особенность терапии для групп риска
- •Особенность терапии у больных с сегментарными мг лица
- •Наблюдение во время лечения пропранололом
- •Сроки отмены -адренолокаторов
- •Показания к назначению глюкокортикоидов в терапии иг.
- •Схемы назначения.
- •Сиролимус
- •2. Местное лечение Местное применение -адреноблокаторов
- •Лечение язв
- •3 Хирургическое лечение Местные инъекции кортикостероидов
- •Лазерное лечение
- •Криотерапия
- •Эндоваскулярная окклюзия.
- •Оперативное лечение
- •XV. Приложение г1. Шкала оценки уровней достоверности доказательств (удд) для методов диагностики (диагностических вмешательств)
Криотерапия
Криотерапия имеет строго ограниченные показания к применению. Ее использование оправдано при небольших поверхностных МГ, расположенных в функционально и косметически не значимых места. При этом криовоздействие должно обеспечивать деструкцию всего клеточного компонента МГ.
Эндоваскулярная окклюзия.
В редких случаях, при МГ большого размера, в случаях плохого ответа на системную терапию возможно применение эндовасклярной окклюзии сосудов МГ (рис. 42).


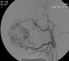
Рис. 42. а – МГ лица в стадии регрессии. Грубый косметический дефект на лице и плохой ответ на системную терапию послужили показаниями для эндоваскулярной окклюзии МГ. б – Ангиография до эндоваскулярной окклюзии. в – Ангиография после эндоваскулярной окклюзии.
Оперативное лечение
Оперативное лечение МГ не утратило своей актуальности, хотя с появлением современных медикаментозных возможностей, отошло на второй план.
Оперативное лечение оправдано в строго определенных случаях в зависимости от стадии развития МГ (УДД-3, УУР-B)
Использование оперативного лечения крайне нежелательно в стадии пролиферации за исключением экстренных ситуаций и осложнений, например кровотечение из МГ либо изъязвление с развитием воспаления.
Также иссечение МГ в стадии пролиферации возможно в редких случаях, когда размеры и локализация позволяют выполнить радикальное удаление без оставления косметического дефекта. Например: МГ «на ножке».
Наибольшее применение хирургический метод находит в лечении МГ в стадии инволюции, поскольку даже после успешного и раннего начала медикаментозной терапии часто остается значительный косметический дефект, вызванный наличием рубцовой-измененной кожи, растянутой объемным образованием, а также остаточного фибро-жирового компонента, как результата регресса МГ. В подобных ситуациях выполняется иссечение патологических тканей с пластикой дефекта различными видами лоскутов в зависимости от локализации и объема поражения.
4 Иное лечение
Близкофокусная рентгенотерапия (Буки-терапия).
В настоящее время близкофокусная рентгенотерапия не рекомендуется для лечения МГ ввиду наличия серьезный отдаленный побочных эффектов.
VIII. Организация оказания медицинской помощи
IX. Дополнительная информация, влияющая на исход заболевания
МГ не является противопоказанием для плановой иммунизации [37,38].
X. Критерии оценки качества медицинской помощи
Приказ Минздрава России от 10.05.2017 N 203н "Об утверждении критериев оценки качества медицинской помощи".
XI. Список литературы
Haggstrom AN, Drolet BA, Baselga E, et al. Prospective study of infantile hemangiomas: clinical characteristics predicting complications and treatment. Pediatrics. 2006; 118 (3): 882–887.
Colonna V, Resta L, Napoli A, Bonifazi E Placental hypoxia and neonatal haemangioma: clinical and histological observations. Br J Dermatol. 2009; 162(1):208–9
Drolet BA, Frieden IJ Characteristics of infantile hemangiomas as clues to pathogenesis: does hypoxia connect the dots? Arch Dermatol. 2010; 146(11):1295–1299
Mihm MC Jr, Nelson JS Hypothesis: the metastatic niche theory can elucidate infantile hemangioma development. J Cutan Pathol. 2010; 37:83–87
Barnes CM, Christison-Lagay EA, Folkman J The placenta theory and the origin of infantile hemangioma. Lymphat Res Biol. 2007; 5(4):245–255
Greenberger S, Bischoff J Pathogenesis of infantile haemangioma. Br J Dermatol. 2013; 169(1):12–19
Greenberger S, Yuan S, Walsh LA, Boscolo E, Kang KT, Matthews B, Mulliken JB, Bischoff J Rapamycin suppresses selfrenewal and vasculogenic potential of stem cells isolated from infantile hemangioma. J Invest Dermatol. 2011; 131(12):2467–2476
Mulliken JB, Zetter BR, Folkman J In vitro characteristics of endothelium from hemangiomas and vascular malformations. Surgery. 1982; 92(2):348–353
https://www.issva.org
Bessis D, Bigorre M, Labreze C. Reticular infantile hemangiomas with minimal or arrested growth associated with lipoatrophy. J Am Acad Dermatol. 2015;72(5):828-833
Tollefson M.M., Frieden I.J., et al. Early Growth of Infantile Hemangiomas: What Parents’ Photographs Tell Us. Pediatrics 2012; 130(2); 314-20.
Chang L.C., Haggstrom A.N., et al. Growth Characteristics of Infantile Hemangiomas: Implications for Management. Pediatrics 2008; 122(2); 360-367.
Mulliken JB, Enjolras O. Congenital hemangiomas and infantile hemangioma: missing links. J Am Acad Dermatol. 2004; 50(6): 875-82.
Haggstrom, A.N., Lammer E.J., et al. Patterns of Infantile Hemangiomas: New Clues to Hemangioma Pathogenesis and Embryonic Facial Development. Pediatrics 2006; 117(3), 698–703.
Nabatian A.S., Milgraum S.S., Hess C.P., et al. PHACE without face? Infantile hemangiomas of the upper body region with minimal or absent facial hemangiomas and associated structural malformations. Pediatric dermatology. 2011; 28(3): 235-241.
Christison-Lagay E.R., Burrows P.E., Alomari A., et al. Hepatic hemangiomas: subtype classification and development of a clinical practice algorithm and registry. J. Pediatr. Surg. 2007; 42(1): 62-7.
Iacobas I., Phung T.L., et al. Guidance Document for Hepatic Hemangioma (Infantile and Congenital) Evaluation and Monitoring. J. Pediatr. Surg. 2018; 203: 294-300.
Chinnadurai S, Snyder K, Sathe N, et al. Diagnosis and Management of Infantile Hemangioma. Rockville, MD: Agency for Healthcare Research and Quality; 2016,
Menapace D, Mitkov M, Towbin R, Hogeling M. The changing face of complicated infantile hemangioma treatment. Pediatr Radiol. 2016;46(11):1494-1506
Krowchuk DP, Frieden IJ, Mancini AJ, Darrow DH, Blei F, Greene AK, et al. Clinical Practice Guideline for the Management of Infantile Hemangiomas. Pediatrics. 2019;143(1): 2018-3475.
Rialon KL, Murillo R, Fevurly RD, et al. Risk factors for mortality in patients with multifocal and diffuse hepatic hemangiomas. J Pediatr Surg. 2015;50(5):837-841
Mamlouk MD, Hess CP. Arterial spin-labeled perfusion for vascular anomalies in the pediatric head and neck. Clin Imaging. 2016; 40(5):1040-1046
Huang S.A., Tu H.M., Harney J.W., et al. Severe hypothyroidism caused by type 3 iodothyronine deiodinase in infantile hemangiomas. N. Engl. J Med 2000; 343(3): 185-9.
Jockin YM, Friedlander SF. Periocular infantile hemangioma. Int Ophthalmol Clin. 2010; 50(4):15-25
Schwartz SR, Blei F, Ceisler E, Steele M, Furlan L, Kodsi S. Risk factors for amblyopia in children with capillary hemangiomas of the eyelids and orbit. JAAPOS. 2006;10(3):262-268
Chamlin SL, Haggstrom AN, Drolet BA, et al. Multicenter prospective study of ulcerated hemangiomas [published correction appears in J Pediatr. 2008;152(4):597]. J Pediatr. 2007;151 (6):684-689
Connelly EA, Viera M, Price C, Waner M. Segmental hemangioma of infancy complicated by life-threatening arterial bleed. Pediatr Dermatol. 2009;26(4):469-472
Garzon MC, Epstein LG, Heyer GL, et al. PHACE syndrome: consensus-derived diagnosis and care recommendations. J Pediatr. 2016;178:24-33
Hoeger PH, Harper JI, et al. Treatment of infantile haemangiomas: recommendations of a European expert group. The European Journal of Pediatrics. 2015; 174 (7): 855-65.
Vleuten C., Schultze Kool L., Verhoeven B., et al. Consensusdocument voor de behandeling van infantiele hemangiomen. 2017 hevas.eu › HEVAS_richtlijnen_2017_WEB.
Chinnadurai S, Snyder K, Sathe N, et al. Diagnosis and Management of Infantile Hemangioma. Agency for Healthcare Research and Quality (US); 2016 Jan. Report No.: 16-EHC002-EF.
Leaute-Labreze C, Dumas de la Roque E, Hubiche T, Boralevi F, Thambo JB, Tai'eb A. Propranolol for severe hemangiomas of infancy. N Engl J Med. 2008;358(24):2649-2651
Leaute-Labreze C, Boccara O, Degrugillier-Chopinet C, et al. Safety of oral propranolol for the treatment of infantile hemangioma: a systematic review. Pediatrics. 2016;138(4):e20160353
Drolet BA, Frommelt PC, Chamlin SL, et al. Initiation and use of propranolol for infantile hemangioma: report of a consensus conference. Pediatrics. 2013;131(1):128-140
Baselga Torres, Bernabéu Wittel, et al. Spanish consensus on infantile haemangioma. An. Pediat.r (Barc). 2016; 85(5): 256-265
Bayart C.B., Tamburro J.E., et al. Atenolol Versus Propranolol for Treatment of Infantile Hemangiomas During the Proliferative Phase: A Retrospective Noninferiority Study. Pediatr Dermatol. 2017; 34(4): 413-421.
Smithson SL, Rademaker M, et al. Consensus statement for the treatment of infantile haemangiomas with propranolol. Australasian Journal of Dermatology. 2017; 58(2): 155-159.
Solman L, Glover M, et al. Oral propranolol in the treatment of proliferating infantile haemangiomas: British Society for Paediatric Dermatology consensus guidelines. British Journal of Dermatology 2018; 179(3): 582-589
Leaute-Labreze C., Hoeger P., Mazereeuw-Hautier J. et al. A randomized, controlled trial of oral propranolol in infantile hemangioma. N. Engl. J. Med. 2015; 372:735–46.
Wedgeworth E., Glover M., Irvine A.D., et al. Propranolol in the treatment of infantile haemangiomas: lessons from the European Propranolol In the Treatment of Complicated Haemangiomas (PITCH) Taskforce survey. British Journal of Dermatology 2016; 174(3): 594-601.
Breur JM, de Graaf M, Breugem CC, Pasmans SG. Hypoglycemia as a result of propranolol during treatment of infantile hemangioma: a case report. Pediatr Dermatol. 2011;28(2):169-171
Prey S, Voisard JJ, Delarue A, et al. Safety of propranolol therapy for severe infantile hemangioma. JAMA. 2016;315(4):413-415
Raphael MF, Breugem CC, Vlasveld FA, et al. Is cardiovascular evaluation necessary prior to and during beta-blocker therapy for infantile hemangiomas?: a cohort study. J Am Acad Dermatol. 2015;72(3):465-472
Shah SD, Baselga E, McCuaig C, et al. Rebound growth of infantile hemangiomas after propranolol therapy. Pediatrics. 2016; 137(4):e20151754
Chang L., Gu Y., Yu Z., et al. When to stop propranolol for infantile hemangioma. Scientific Reports 2017; 22(7): 43292.
Greene AK, Couto RA. Oral prednisolone for infantile hemangioma: efficacy and safety using a standardized treatment protocol. Plast Reconstr Surg. 2011;128(3):743-752
Chinnadurai S, Fonnesbeck C, Snyder KM, et al. Pharmacologic interventions for infantile hemangioma: a meta-analysis. Pediatrics. 2016;137(2):e20153896
Буторина А.В. Лечение сосудистых новообразований у детей: метод, рек. М., 2000. 42с.
Bartoshesky L.E. Corticosteroid treatment of cutaneous hemangiomas: how effective a report on 24 children. Clin. Pediatr. 1978; 17: 629-638.
Nguyen J.F., Fay A. Pharmacologic therapy for periocular infantile hemangiomas: a review of the literature. Semin. Ophthalmol. 2009; 24(3): 178-184.
George M.E., Sharma V., et al Adverse Effects of Systemic Glucocorticosteroid Therapy in Infants With Hemangiomas. Arch. Dermatol. 2004; 140(8): 963-969.
Cogen M.S. Eyelid depigmentation following corticosteroid injection for infantile ocular adnexal hemangioma. J. Pediatr. Ophthalmol. Strabismus. 1989; 26 (1): 35-38.
Gawrych E. Intralesional corticosteroid therapy in infantile hemangiomas. Ann. Acad. Med. Stetin. 2009; 55(1): 15-21.
Pope E. Oral Versus High-Dose Pulse Corticosteroids for Problematic Infantile Hemangiomas: A Randomized, Controlled Trial. Pediatrics. 2007; 119(6): 1239-1247.
Gnarra M., Solman L., Harper J.I., Syed S.B. Propranolol and prednisolone combination for the treatment of segmental haemangioma in PHACES syndrome. Br J Dermatol. 2015; 173(1): 242-6.
Breur J.M., de Graaf M., Breugem C.C., Pasmans S.G. Hypoglycemia as a result of propranolol during treatment of infantile hemangioma: a case report. Pediatr Dermatol. 2011; 28(2): 169–171.
Greenberger S., Yuan S., Walsh L.A., et al. Rapamycin suppresses self-renewal and vsculogenic potential of stem cells isolated from infantile hemangioma. J. Invest. Dermatol. 2011; 131(12): 2467–2476.
Kaylani S., Theos A.J., Pressey J.G. Treatment of infantile hemangiomas with sirolimus in a patient with PHACE syndrome. Pediatr. Dermatol. 2013; 30(6): 194–7.
Hutchins K.K., Ross R.D., Kobayashi D. et al. Treatment of Refractory Infantile Hemangiomas and Pulmonary Hypertension With Sirolimus in a Pediatric Patient. Journal of Pediatric Hematology Oncology. 2017; 39(7): 391–393.
Puttgen K, Lucky A, Adams D, et al; Hemangioma Investigator Group. Topical timolol maleate treatment of infantile hemangiomas. Pediatrics. 2016; 138(3):e20160355
Chinnadurai S, Snyder K, Sathe N, et al. Diagnosis and Management of Infantile Hemangioma. Rockville, MD: Agency for Healthcare Research and Quality; 2016
Ng M, Knuth C, Weisbrod C, Murthy A. Propranolol therapy for problematic infantile hemangioma. Ann Plast Surg. 2016;76(3):306-310
Frommelt P., Juern A., Siegel D., et al. Adverse Events in Young and Preterm Infants Receiving Topical Timolol for Infantile Hemangioma. Pediatric dermatology. 2016; 33(4): 405-414.
Puttgen K., Lucky A., Adams D., et al. Topical Timolol Maleate Treatment of Infantile Hemangiomas. Pediatrics. 2016; 138(3).
https://www.kinderformularium.nl/
Chowdri NA, Darzi MA, Fazili Z, Iqbal S. Intralesional corticosteroid therapy for childhood cutaneous hemangiomas. Ann Plast Surg. 1994;33(1):46-51
Chen MT, Yeong EK, Horng SY. Intralesional corticosteroid therapy in proliferating head and neck hemangiomas: a review of 155 cases. J Pediatr Surg. 2000; 35(3):420-423
Buckmiller LM, Francis CL, Glade RS. Intralesional steroid injection for proliferative parotid hemangiomas. Int J Pediatr Otorhinolaryngol. 2008; 72(1):81-87
Prasetyono TO, Djoenaedi I. Efficacy of intralesional steroid injection in head and neck hemangioma: a systematic review. Ann Plast Surg. 2011;66(1):98-106
Mulliken JB. Vascular malformation. In: Thorne CH, Beasley RW, Aston SJ, et al. eds. Grabb and Smith’s Plastic Surgery. 6th ed. Philadelphia, PA: Lippincott, Williams and Wilkins; 2007:191–200
Prasetyono, T. O. H., Djoenaedi, I. Efficacy of Intralesional Steroid Injection in Head and Neck Hemangioma. Annals of Plastic Surgery,2011; 66(1), 98–106.
Sloan GM, Reinisch JF, Nichter LS, Saber WL, Lew K, Morwood DT. Intralesional corticosteroid therapy for infantile hemangiomas. Plast Reconstr Surg. 1989;83(3):459-467
Chowdri NA, Darzi MA, Fazili Z, Iqbal S. Intralesional corticosteroid therapy for childhood cutaneous hemangiomas. Ann Plast Surg. 1994;33(1):46-51
Chen MT, Yeong EK, Horng SY. Intralesional corticosteroid therapy in proliferating head and neck hemangiomas: a review of 155 cases. J Pediatr Surg. 2000; 35(3):420-423
Goyal, R., Watts, P., Lane, C. M., Beck, L., Gregory, J. W. Adrenal suppression and failure to thrive after steroid injections for periocular hemangioma. Ophthalmology, 2004; 111(2), 389–395
Egbert JE, Schwartz GS, Walsh AW. Diagnosis and treatment of an ophthalmic artery occlusion during an intralesional injection of corticosteroid into an eyelid capillary hemangioma. Am J Ophthalmol. 1996;121(6): 638-642
Egbert JE, Paul S, Engel WK, Summers CG. High injection pressure during intralesional injection of corticosteroids into capillary hemangiomas. Arch Ophthalmol. 2001;119(5):677-683
Baselga E, Roe E, Coulie J, et al. Risk factors for degree and type of sequelae after involution of untreated hemangiomas of infancy. JAMA Dermatol. 2016; 152(11): 1239-1243
Boos MD, Castelo-Soccio L. Experience with topical timolol maleate for the treatment of ulcerated infantile hemangiomas (IH). J Am Acad Dermatol. 2016; 74(3):567-570
Tay Y.K., Tan S.K. Treatment of infantile hemangiomas with the 595-nm pulsed dye laser using different pulse widths in an Asian population. Lasers Surg Med 2012; 44(2): 93-96.
Kessels J.P., Hamers E.T., Ostertag J.U. Superficial hemangioma: pulsed dye laser versus wait- and-see. Dermatol. Surg. 2013; 39(3 Pt 1): 414-421.
Civas E., Koc E., Aksoy B., Aksoy H.M. Clinical experience in the treatment of different vascular lesions using a neodymium-doped yttrium aluminum garnet laser. Dermatol Surg 2009; 35(12): 1933-1941.
Hartmann F., Lockmann A. Nd:YAG and pulsed dye laser therapy in infantile haemangiomas: a retrospective analysis of 271 treated haemangiomas in 149 children. Journal of the European Academy of Dermatology and Venereology. 2017; 31(8): 1372–1379
XII. Приложение А1. Состав Рабочей группы
Абушкин И.А., профессор
Гарбузов Р.В., д.м.н.
Голенищев А.И.
Денис А.Г.
Донюш Е.К.
Клецкая И.С.
Купатадзе Д.Д, профессор
Мыльников А.А., к.м.н.
Нарбутов А.Г., к.м.н.
Нурмеев И.Н., профессор
Петрушин А.В., к.м.н.
Поляев Ю.А., профессор
Романов Д.В., к.м.н.
Сафин Д.А.
Хагуров Р.А., к.м.н.
XIII. Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций
Детские хирурги
Педиатры
Онкологи
Дерматологи
Кардиологи
Врачи лучевой диагностики
Порядок обновления клинических рекомендаций
По мере возникновения новых знаний о сути болезни в рекомендации будут внесены соответствующие изменения и дополнения.
XIV. Приложение Б. Алгоритм действия врача
XIV. Приложение В. Информация для пациента
Что такое пропранолол и как он работает?
Пропранолол относится к группе препаратов, известных как бета-блокаторы, которые используются для лечения высокого кровяного давления и учащенного сердцебиения. Они работают, замедляя сердце и сужая кровеносные сосуды. Последний полезен при гемангиомах, так как он уменьшает кровоток через них, выцветает и смягчает их. Кроме того, пропранолол влияет на клетки, вызывающие рост гемангиомы, поэтому размер гемангиомы начинает уменьшаться.
Что такое младенческая гемангиома?
Инфантильные гемангиомы состоят из небольших незрелых кровеносных сосудов и обычно появляются в первые несколько дней или недель жизни в виде одной или нескольких приподнятых красных областей на поверхности кожи или в виде голубоватых отеков, возникающих глубже в коже. Они встречаются до 10% детей и чаще встречаются у женщин, недоношенных детей и многоплодных (близнецов).
Гемангиомы быстро растут в первые 3 месяца жизни и обычно прекращают расти в возрасте от 6 до 12 месяцев. Они медленно сжимаются в течение нескольких лет.
Большинство гемангиом не вызывают проблем и не требуют лечения; однако их нужно лечить, если они развиваются в месте, которое мешает жизненно важной функции, такой как дыхание, кормление или зрение. Иногда гемангиомы, особенно в области подгузника, могут изъязвляться и кровоточить, что может быть очень болезненным и потребовать лечения.
Лечение стероидами через рот использовалось в качестве первой линии лечения в прошлом, однако с 2008 года было установлено, что пропранолол является гораздо более безопасным и более эффективным средством лечения гемангиом, и в настоящее время стероиды очень редко требуются.
Вылечит ли пропранолол состояние кожи моего ребенка?
Пропранолол помогает уменьшить рост, размер и покраснение гемангиом быстрее, чем это происходит без лечения, и может предотвратить обезображивание в долгосрочной перспективе, особенно там, где гемангиомы возникают на лице. Необработанные гемангиомы также сокращаются и исчезают сами по себе в течение нескольких лет и могут оставить обезображивание позади.
Как часто и когда мой ребенок должен принимать пропранолол?
Пропранолол обычно начинают, как только гемангиома вызывает или, как считается, может вызвать проблему. Это дано 2 или 3 раза в день, пока гемангиома, как думают, больше не будет вмешиваться в жизненно важную функцию и не покажет дальнейший рост, когда лечение остановлено. Обычно это около одного года, но иногда лечение может быть продлено.
Какую дозу должен принять мой ребенок?
Доза вашего ребенка рассчитывается в зависимости от его веса и может быть увеличена в зависимости от реакции на лечение. Это означает, что ваш доктор будет корректировать дозу по мере роста вашего ребенка. Пропранолол для детей обычно поставляется в виде 5 мг / 5 мл жидкости (то есть 1 мл жидкости содержит 1 мг пропранолола).
Пропранолол также доступен с другими сильными сторонами, поэтому вы должны всегда проверять его с вашим фармацевтом, прежде чем использовать лекарство. В идеале следует избегать любой другой силы, чтобы свести к минимуму риск неправильной дозы для вашего ребенка.
Если у вас есть какие-либо вопросы о дозе пропранолола для вашего ребенка, обратитесь к медсестре, врачу или фармацевту.
Как долго моему ребенку нужно принимать пропранолол, прежде чем я увижу эффект?
Раннее воздействие на гемангиомы часто можно увидеть в течение нескольких дней, но лечение обычно должно продолжаться до достижения возраста не менее 12-15 месяцев, чтобы гарантировать, что гемангиома не будет расти снова. Пропранолол может быть отменен без необходимости постепенного снижения дозы.
Каковы побочные эффекты пропранолола?
Большинство детей не испытывают никаких побочных эффектов пропранолола в дозах, используемых для лечения гемангиом. Однако пропранолол редко может быть связан со следующими побочными эффектами:
¥ хрип и кашель (бронхоспазм).
¥ нарушение сна.
¥ более холодные руки и ноги, в результате чего они приобретают легкий синий цвет (периферическая вазоконстрикция).
¥ слабость и усталость, проявляющиеся как гибкость и отсутствие интереса к окружению. жидкий стул (диарея) и рвота
¥ медленный сердечный ритм (брадикардия).
¥ пониженное артериальное давление (гипотония). низкий уровень сахара в крови (гипогликемия).
¥ Если у вас есть какие-либо опасения по поводу этих побочных эффектов, пожалуйста, обсудите их с вашим врачом, медсестрой или фармацевтом.
Что я должен сделать, чтобы избежать низкого уровня сахара в крови у моего ребенка?
Низкий уровень сахара в крови чаще встречается, когда ребенок не ест нормальное количество пищи или долгое время не питался. Дайте пропранолол с молоком или кормом, чтобы избежать снижения уровня сахара в вашем ребенке. Избегайте длительных периодов без кормления. Если ваш ребенок временно плохо питается из-за болезни или рвоты, дозу пропранолола следует удерживать.
Как будет контролироваться мой ребенок на предмет побочных эффектов лечения пропранололом?
Большинство детей не требуют какого-либо контроля при запуске пропранолола. Пациенты младше 4 недель, недоношенные дети, а также те, кто испытывает трудности с кормлением или другие дополнительные расстройства, нуждаются в измерении частоты сердечных сокращений и артериального давления в течение 2 часов в больнице после первой дозы, и если доза увеличивается вдвое или втрое. Вполне вероятно, что требования к оценке и мониторингу изменятся с ростом опыта использования пропранолола при гемангиомах.
Может ли моему ребеноку делать прививки во время приема пропранолола?
Да, все прививки могут проходить как обычно.
Влияет ли пропранолол на будущую фертильность или будущую беременность у детей женского пола?
Нет.
Может ли мой ребенок принимать другие лекарства одновременно с пропранололом?
Некоторые лекарства могут взаимодействовать с пропранололом, поэтому важно проконсультироваться с врачом, прежде чем давать другие лекарства.
Если у вашего ребенка появляется одышка, может потребоваться отказ от пропранолола до тех пор, пока одышка не прекратится.
Если считается, что свистящее дыхание требует лечения ингаляторами или небулайзерами, рассмотрите возможность использования ипратропия бромида, а не сальбутамола. Пропранолол может оказывать противоположное действие на сальбутамол.
Гели для прорезывания зубов, содержащие лидокаин, не следует давать детям, принимающим пропранолол. Некоторые аптеки продают зубные порошки, которые не содержат лидокаина и безопасны.
