
- •Контрольная работа №8. Обмен и функции аминокислот.
- •1. Био. Роль белков. Био. Ценность белков. Заменимые и незаменимые аминокислоты.
- •11) Экспрессия ген. Информации.
- •2. Нормы белка в питании. Азотистый баланс, его виды, значение.
- •3. Переваривание белков и всасывание аминокислот в желудочно-кишечном тракте.
- •5. Окислительное дезаминирование аминокислот.
- •6.Трансаминирование аминокислот (а.Браунштейн, и.Крицман). Диагностическое значение определения активности трансаминаз. Связь трансаминирования с дезаминированием (непрямое дезаминирование).
- •7. Декарбоксилирование аминокислот. Образование биогенных аминов: гистамина, серотонина, гамма-аминомасляной кислоты (гамк), биологическая роль и их инактивация.
- •8. Образование аммиака и судьба аммиака в организме. Гипераммониемия. (*Токсическое действие аммиака).
- •1) Синтез аминокислот из соответствующих кетокислот:
- •3) Синтез пуриновых и пиримидиновых нуклеотидов.
- •4) Синтез мочевины – основной путь обезвреживания аммиака.
- •9. Биосинтез мочевины. Клиническое значение определения мочевины.
- •10. Синтез креатина, креатин – фосфата, биологическая роль. Клиническое значение определения креатинина.
- •11* Особенности обмена аминок-т (глицин, метионин, глутаминовая и аспарагиновая кислоты, триптофан, фенилаланин).
- •12* Патология азотистого обмена: белковая недостаточность (Квашиоркор).
- •13. Механизм возникновения наследственных нарушений обмена аминокислот (фенилпировиноградная олигофрения, алкаптонурия, альбинизм).
- •14. Переваривание и всасывание нуклеопротеинов.
- •15. Распад пуриновых нуклеотидов.
- •16. Заболевания, связанные с нарушением обмена нуклеотидов: подагра, синдром Леша – Нихена.
- •Ситуационные задачи по теме: «обмен и функции аминокислот».
10. Синтез креатина, креатин – фосфата, биологическая роль. Клиническое значение определения креатинина.
К онечным
продуктом распада аминокислот в
организме, наряду с мочевиной, является
креатинин,
который
образуется в мышечной ткани из
креатинфосфата. Креатин и креатинфосфат
– важнейшие азотистые вещества мышц,
участвующие в химических процессах,
связанных с ресинтезом АТФ, являющегося
участником мышечного сокращения. Это
небелковые азотистые вещества мышц.
Креатин синтезируется в почках и печени
из трех аминокислот, затем поступает в
мышечную ткань.
онечным
продуктом распада аминокислот в
организме, наряду с мочевиной, является
креатинин,
который
образуется в мышечной ткани из
креатинфосфата. Креатин и креатинфосфат
– важнейшие азотистые вещества мышц,
участвующие в химических процессах,
связанных с ресинтезом АТФ, являющегося
участником мышечного сокращения. Это
небелковые азотистые вещества мышц.
Креатин синтезируется в почках и печени
из трех аминокислот, затем поступает в
мышечную ткань.
Креатинфосфати явл. «депо» макроэргических связей. Креатинфосфат обеспечивает ресинтез АТФ в первые секунды работы (5-10 сек), когда ни анаэробный гликолиз, ни аэробное окисление глюкозы и ВЖК ещё не активировано, и кровоснабжение мышцы не увеличено. В клетках нерв. ткани креатинфосфат поддерживает жизнеспособность клеток при отсутствии О2.
Креатинин удаляется в составе мочи. В норме мочевины за сутки у взрослого выделяется около 25- 30г, креатинина – 1,5-2,4 г., солей аммония – 0,5-1,2 г.
Физиолог. креатинурия: 1) У новорождённых (синтез креатина превышает объём мышечной массы). 2) У стариков (т.к. атрофия мышц и неполное использование образующегося креатина). Патологическая креатиниурия: мыш. дистрофия, миопатии, СД, голодание, авитаминозы С и Е. |
Патолог. креатининурия (уменьшение выделения креатинина): заболевания почек и печени. Патологи. креатининурия (увел-е выделения креатинина): опухоли, ожоги, гипотиреоз, акромегалия.
|
11* Особенности обмена аминок-т (глицин, метионин, глутаминовая и аспарагиновая кислоты, триптофан, фенилаланин).
1 )
ГЛИЦИН
– участвует в реакциях обмена. Ее
основной источник – серин.
)
ГЛИЦИН
– участвует в реакциях обмена. Ее
основной источник – серин.
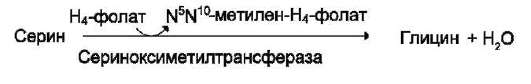
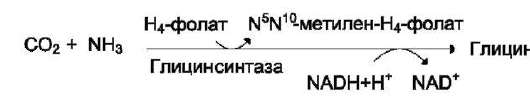
Участвует:
- В синтезе порфиринов, входящих в состав гемоглобина.
- В синтезе пуринов.
- В синтезе глутатиона.
- В синтезе креатина, холина, парных желчных кислот.
- В обезвреживании токсических соединений, путем связывания с бензойной и фенилуксусной кислотами, образуя гиппуровую кислоту, которая выводится с мочой.
2) МЕТИОНИН – является донором метильных групп (-СН3) для образования: адреналина, холина, креатина, карнитина и участвует в синтезе цистеина. Участвует в обезвреживании токсичных метаболитов и лекарственных веществ.
Активная форма метионина – S-аденозилметионин (SAM). (SAГ – аденозигомоцистеин).

3) АСПАРАГИНОВАЯ К-ТА участвует в синтезе мочевины, обезвреживании аммиака с образованием аспарагина, в образовании пуринов и пиримидинов, в синтезе АМФ, УМФ.

4) ГЛУТАМИНА К-ТА принимает участие в синтезе глютатиона, в образовании α-кетоглутаровой к-ты, в обезвреживании аммиака с образованием глутамина, при ее декарбоксилир. образуется ГАМК.

5) ТРИПТОФАН – в организме превращается в биохимически активные соединения: никотиновую кислоту (витамин РР), серотонин.
С еротонин
– для образования мелатонина. При
избыточном накоплении наблюдается
карционоидный
синдром.
еротонин
– для образования мелатонина. При
избыточном накоплении наблюдается
карционоидный
синдром.
6 ) ФЕНИЛАЛАНИН.
Значению обмена фенилаланина в детском
организме придается большое значение.
Это связано с тем, что выпадение активности
определенных ферментов (мутация гена,
ответственного за синтез ферментов,
принимающих участие в превращении этой
аминокислоты) приводит к накоплению
необычных продуктов реакции, например,
фенилпировиноградной, гомогентизиновой
кислот, являющихся токсическими
веществами, влияющими на функции
головного мозга ребенка. Кроме того,
избыток фенилаланина и дефицит тирозина
сказывается на процессах биосинтеза
специфических белков головного мозга.
) ФЕНИЛАЛАНИН.
Значению обмена фенилаланина в детском
организме придается большое значение.
Это связано с тем, что выпадение активности
определенных ферментов (мутация гена,
ответственного за синтез ферментов,
принимающих участие в превращении этой
аминокислоты) приводит к накоплению
необычных продуктов реакции, например,
фенилпировиноградной, гомогентизиновой
кислот, являющихся токсическими
веществами, влияющими на функции
головного мозга ребенка. Кроме того,
избыток фенилаланина и дефицит тирозина
сказывается на процессах биосинтеза
специфических белков головного мозга.
Основное количество фенилаланина расходуется по 2 путям:
включается в белки;
превращается в тирозин.
Превращение фенилаланина в тирозин необходимо для удаления его избытка, т.к. высокие концентрации фенилаланина токсичны для клеток.
