
- •Контрольная работа №8. Обмен и функции аминокислот.
- •1. Био. Роль белков. Био. Ценность белков. Заменимые и незаменимые аминокислоты.
- •11) Экспрессия ген. Информации.
- •2. Нормы белка в питании. Азотистый баланс, его виды, значение.
- •3. Переваривание белков и всасывание аминокислот в желудочно-кишечном тракте.
- •5. Окислительное дезаминирование аминокислот.
- •6.Трансаминирование аминокислот (а.Браунштейн, и.Крицман). Диагностическое значение определения активности трансаминаз. Связь трансаминирования с дезаминированием (непрямое дезаминирование).
- •7. Декарбоксилирование аминокислот. Образование биогенных аминов: гистамина, серотонина, гамма-аминомасляной кислоты (гамк), биологическая роль и их инактивация.
- •8. Образование аммиака и судьба аммиака в организме. Гипераммониемия. (*Токсическое действие аммиака).
- •1) Синтез аминокислот из соответствующих кетокислот:
- •3) Синтез пуриновых и пиримидиновых нуклеотидов.
- •4) Синтез мочевины – основной путь обезвреживания аммиака.
- •9. Биосинтез мочевины. Клиническое значение определения мочевины.
- •10. Синтез креатина, креатин – фосфата, биологическая роль. Клиническое значение определения креатинина.
- •11* Особенности обмена аминок-т (глицин, метионин, глутаминовая и аспарагиновая кислоты, триптофан, фенилаланин).
- •12* Патология азотистого обмена: белковая недостаточность (Квашиоркор).
- •13. Механизм возникновения наследственных нарушений обмена аминокислот (фенилпировиноградная олигофрения, алкаптонурия, альбинизм).
- •14. Переваривание и всасывание нуклеопротеинов.
- •15. Распад пуриновых нуклеотидов.
- •16. Заболевания, связанные с нарушением обмена нуклеотидов: подагра, синдром Леша – Нихена.
- •Ситуационные задачи по теме: «обмен и функции аминокислот».
1) Синтез аминокислот из соответствующих кетокислот:
АТФ
С Н3-С-СООН
+ NН3
СН3-СН-СООН
Н3-С-СООН
+ NН3
СН3-СН-СООН
О NН2
ПВК аланин
2) Синтез аммонийных солей в почках. В почках глутамин под влиянием глутаминазы расщепляется с образованием аммиака, идущего на нейтрализацию кислых соединений с образованием аммонийных солее(0,5 г/сут).
NH3 нейтрализует кислые продукты обмена, которые в виде аммон. солей экскретируются с мочой. Этот процесс является одним из механизмов регуляции кислотно-щелочного равновесия в организме и сохранения важнейших катионов (Na+, K+) для поддержания осмотического давления.
3) Синтез пуриновых и пиримидиновых нуклеотидов.
4) Синтез мочевины – основной путь обезвреживания аммиака.
5) Обезвреживание NH3 – синтез глутамата и глутамина, аспарагина, карбамоилфосфата.
Синтез глутамата (восстановит. аминирование): α-кетоглутарат + NH3 =(ГДГ)= глутамат.
Синтез глутамина. Явл. главным способом связывания NH3, активно происходит в нерв. и мыш. тканях, в почках, сетчатке глаза, печени. Реакция в митохондриях.
Г лутамат
+ NH3
=(глутаминсинтетаза вверху, АТФ
АДФ внизу)= глутамин.
лутамат
+ NH3
=(глутаминсинтетаза вверху, АТФ
АДФ внизу)= глутамин.
Глутамин – основной донор азота, который используется для синтеза:
- пурин. и пирим. колец;
- аспарагина;
-аминосахаров.
ТОКСИЕЧЕСМКОЕ ДЕЙСТВИЕ АММИАКА:
1) Связывание NH3 с α-кетоглутарат приводит в уменьшению его кон-и, снижению скорости ЦТК и ЦПЭ (гипоэнергетическое состояние);
2) Продукт связывания NH3 с глутаматом – глутамин – явл. осмотически активным вещ-вом. Это приводит к задержке воды в клетках и их набуханию, что вызывает отёк тканей. В нервной ткани это может вызвать отёк мозга, кому и смерть.
3) Использование глутамата для нейтрализации NH3 вызывает снижение синтеза ГАМК, основного тормохного медиатора ЦНС (судороги).
4) Ионы аммония NH4+ вызывают алкалоз. При этом увел. сродство Hb к О2, Hb не отдаёт О2 в капиллярах, в результате возникает гипоксия клеток.
ГИПЕРАММОНИЕМИЯ - повышение содержания аммиака в крови до 60мкмоль/л (норма-11,0-32,0мкмоль/л) оказывает токсическое действие на организм.Причины:
1) Врожденная форма - генетический дефект фермент орнитинового цикла в печени (дефект любого из 5-ти ферментов синтеза мочи, поэтому 5 типов).
С имптомы:
рвота, беспокойство, судороги, дых.
алкалоз, печён. недостаточность, легочные
и внутричер. кровоизлияния.
имптомы:
рвота, беспокойство, судороги, дых.
алкалоз, печён. недостаточность, легочные
и внутричер. кровоизлияния.
2) Приобретённая форма - вторичное поражение печени в результате цирроза, гепатита и др.
Симптомы: тошнота, рвота, судороги, нечленоразд. речь, тремор, нарушение координации движений.
Для диагностики производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, активность ферментов печени.
9. Биосинтез мочевины. Клиническое значение определения мочевины.
Еще в прошлом веке русские ученые М.В. Ненцкий и С.С. Салазкин показали, что в печени происходит образование мочевины из углекислого газа и аммиака.
К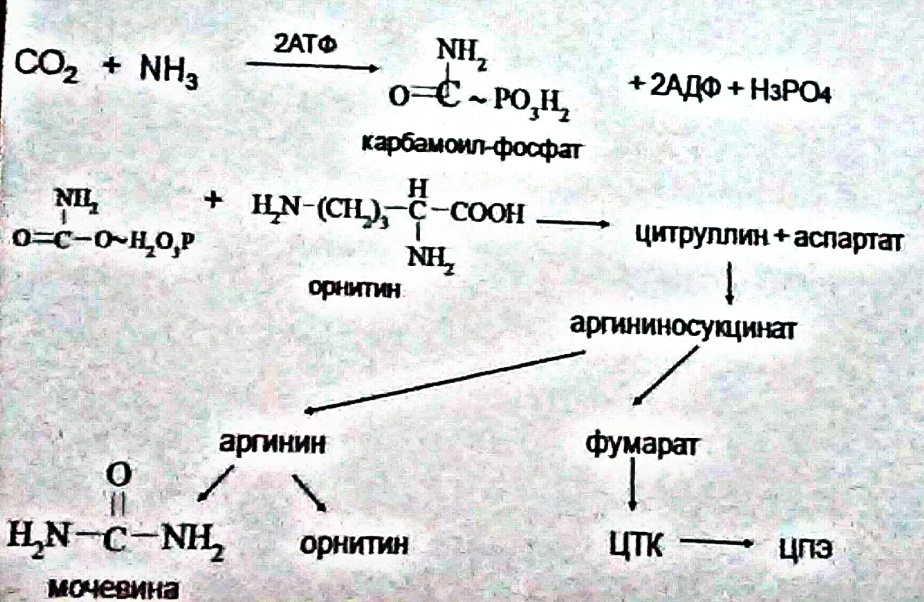 ребс
и Гензеляйт установили, что синтез
мочевины
- цикл. процесс, в котором ключевым
соединением, замыкающим цикл, является
орнитин. Кохен и Ратнер выяснили, что
начальной реакцией этого цикла является
синтез карбамоилфосфата.
ребс
и Гензеляйт установили, что синтез
мочевины
- цикл. процесс, в котором ключевым
соединением, замыкающим цикл, является
орнитин. Кохен и Ратнер выяснили, что
начальной реакцией этого цикла является
синтез карбамоилфосфата.
В печени аммиак связывается с СО2 с образованием карбамоилфосфата под действием карбамоилфосфатсинтетазы. Затем под действием орнитин-карбамоилтрансферазы карбамоильная группа карбамоилфосфата переносится на орнитин и образуется цитруллин. В следующей реакции аргининосукцинатсинтетаза связывает его с аспартатом и образуется аргининоянтарная кислота. Аспартат – источник второго атома азота мочевины. Далее происходит расщепление аргининоянтарной кислоты на аргинин и фумарат (идет в ЦТК). Аргинин гидролизуется под действием аргиназы на орнитин и мочевину. Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается.
Первые две реакции происходят в митохондриях гепатоцитов. Затем цитруллин транспортируется в цитозоль, где и осуществляются дальнейшие превращения.
Орнитиновый цикл в печени выполняет 2 функции:
1) Превращение азота аминокислот в мочевину, которая экскретируется и предотвращает накопление токсичных продуктов - аммиака;
2) Синтез аргинина и пополнение его в организме.
Отмечается, что у детей первых месяцев жизни функция печени развита недостаточно, что проявляется в том, что у ребенка количество аммиака по сравнению с взрослым человеком увеличено в 2-2,5 раза. У новорожденных – 20-30% общего азота падает на азот мочевины.
Мочевина – безвредное для организма соединение. Главным местом ее образования в организме является печень, где есть ферменты мочевинообразования. В головном мозге имеются все ферменты синтеза мочевины, кроме карбамоилфосфатазы, поэтому в нем мочевина не образуется. Мочевина – основной конечный продукт азотистого обмена, в составе которого из организма выделяется до 90% всего выводимого азота. В норме экскрекция мочевины – 25-30 г/сут. При повышении количества потребляемых с пищей белков увеличивается выделение мочевины.
