
- •Газы крови влияют на pH
- •Углекислый газ
- •Кислород
- •Оксигемоглобин
- •Насыщение гемоглобина кислородом
- •Иллюстрация понятий оксигемоглобина (HbO2) и насыщения гемоглобина (HbO2sat) Парциальное давление кислорода (pO2)
- •Кривая диссоциации гемоглобина в норме и при изменении pH и концентрации 2,3-дифосфоглицерата
- •Как удаляются ионы водорода?
- •Источники и пути удаления ионов водорода
- •Быстрая компенсация сдвигов рН Буферные системы
- •Фосфатная буферная система
- •Удаление щелочных эквивалентов фосфатным буфером
- •Бикарбонатная буферная система
- •Белковая буферная система
- •Изменение заряда буферных групп белка при различных рН Гемоглобиновая буферная система
- •Длительная стабилизация сдвигов рН
- •Удаление кислоты через легкие
- •Удаление кислоты через почки
- •Реабсорбция бикарбонат-ионов
- •Реабсорбция бикарбонат-ионов
- •Ацидогенез
- •Реакции ацидогенеза
- •Аммониегенез
- •Реакции аммониегенеза
- •Показатели кислотно-основного состояния
- •Изменение кос - частая ситуация
- •Причины нарушений кислотно-основного состояния
- •Диагностика нарушений кос
- •Использование показателя рСо2 для диагностики нарушений кислотно-основного состояния
Аммониегенез
Глутамин и глутаминовая кислота, попадая в клетки канальцев, быстро дезаминируются глутаминазой и глутаматдегидрогеназой с образованием аммиака. Являясь гидрофобным соединением, аммиак диффундирует в просвет канальца и связывает экскретируемые ионы Н+ с образованием иона NH4+ , который удаляется с мочой.
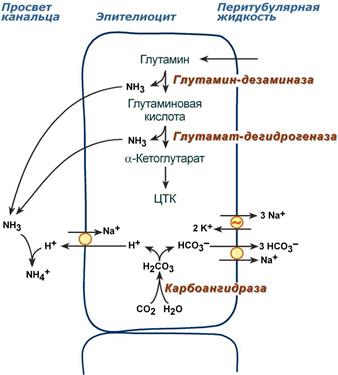
Реакции аммониегенеза
Аммониегенез происходит на протяжении всего почечного канальца, но более активно идет в дистальных отделах – дистальных канальцах и собирательных трубочках коркового и мозгового слоев. В этих сегментах секреция ионов Н+ происходит активно с участием Н+‑АТФазы, локализованной на апикальной мембране эпителиоцита.
Некоторые ткани влияют на рН пассивно
Влияние костной ткани
Это пассивная и наиболее медленно реагирующая система. Механизм ее участия в регуляции рН крови состоит в возможности отдавать в плазму крови ионы Са2+ и Na+ в обмен на ионы Н+. Происходит растворение гидроксиапатитных кальциевых солей костного матрикса, освобождение ионов Са2+ и HPO42–. В дальнейшем ионы HPO42– попадут в мочу и свяжутся с Н+ с образованием дигидрофосфата (ацидогенез), который и уходит с мочой.
8Н+ + Ca10(PO4)6(OH)2 → 2H2O + 10Ca2+ + 6HPO42–
Параллельно при снижении рН (закисление) происходит поступление ионов H+ внутрь остеоцитов, а ионов K+ – наружу.
Участие костной ткани в стабилизации КОС приводит к ее деминерализации и развитию остеопороза.
Роль печени
Существенную, но пассивную роль в регуляции кислотно-основного состояния крови берет на себя печень:
процесс глюконеогенеза обеспечивает превращение аминокислот, кетокислот и молочной кислоты в нейтральную глюкозу,
осуществляет метаболизм аммиака (сильное основание) и его удаление в виде в мочевины,
синтезирует белки крови (в первую очередь альбумин), которые создают белковую буферную систему,
удаление кислых и щелочных веществ с желчью.
Печеночная недостаточность приводит к развитию метаболического ацидоза.
Роль желудочно-кишечного тракта
Органы ЖКТ влияют на состояние КОС, так как в соответствующих клетках происходит синтез HCl и НСО3–.
В обкладочных клетках желудка при секреции HCl одновременно генерируется НСО3–, выводимый в кровь и сдвигающий pH в щелочную сторону. Поэтому при рвоте, когда происходит потеря HCl и избыточный переход НСО3– в кровь, развивается алкалоз.
Образование панкреатического и кишечного соков сопровождается секрецией НСО3– при одновременном выходе ионов H+ в кровоток. При диарее ионы НСО3– пищеварительных соков не успевают реабсорбироваться обратно и теряются, ионы H+ в крови оказываются в избытке, развивается ацидоз.
Анионы крови связывают протоны
Буферные основания
Общим показателем, характеризующим КОС, является концентрация буферных, включающая сумму всех оснований крови, хотя большую часть этих оснований представляют анионы бикарбоната и белковые анионы.
Более узким показателем является концентрация бикарбонат-ионов. При дыхательных нарушениях количество бикарбонатов мало изменяется, т.к. угольная кислота, образуемая из CO2, очень плохо диссоциирует и изменение ее концентрации не влияет на содержание иона HCO3‑. Но, например, при накоплении в крови метаболических кислот (молочной кислоты) ион HCO3‑ будет активно расходоваться на их буферизацию, показатель снизится.
На практике главным и наиболее информативным показателем служит избыток буферных оснований (base excess, BE). Изменение величины BE отражает степень использования буферных оснований для удержания гомеостаза при смещении уровня ионов H+. При алкалозе использование буферных оснований не требуется, показатель возрастает. При закислении среды основания расходуются и показатель BE снижается, т.е. возникает дефицит оснований.
Остаточные анионы
Если посчитать сумму всех ионных зарядов в плазме крови, будет обнаружено, что количество положительных зарядов равно количеству отрицательных зарядов, т.е. присутствует электронейтральность.
Катионы (мэкв/л) |
Анионы (мэкв/л) |
||
Na+ |
140 |
Cl– |
100 |
Mg2+ |
1,5 |
Белки |
13 |
K+ |
4,5 |
HCO3– |
24 |
Ca2+ |
5,0 |
PO43– |
2 |
|
|
Остаточные анионы |
12 |
Всего |
151 |
Всего |
151 |

|
Остаточные анионы отражают накопление каких-либо кислот в плазме крови.
Остаточные анионы представлены анионами органических (молочная, щавелевая, мочевая и др.) и неорганических (серная и др.) кислот. Они возрастают при кетоацидозе (анионы ацетоуксусной и b‑гидроксимасляной кислот), лактоацидозе (лактат-анионы), отравлении этанолом (анионы ацетоуксусной и b‑гидроксимасляной кислот, ацетат-анионы, лактат-анионы). Особое значение показатель приобретает при интоксикациях салицилатами, метанолом, этиленгликолем, концентрация кислых метаболитов которых вносит существенный вклад в его величину.
