
- •Газы крови влияют на pH
- •Углекислый газ
- •Кислород
- •Оксигемоглобин
- •Насыщение гемоглобина кислородом
- •Иллюстрация понятий оксигемоглобина (HbO2) и насыщения гемоглобина (HbO2sat) Парциальное давление кислорода (pO2)
- •Кривая диссоциации гемоглобина в норме и при изменении pH и концентрации 2,3-дифосфоглицерата
- •Как удаляются ионы водорода?
- •Источники и пути удаления ионов водорода
- •Быстрая компенсация сдвигов рН Буферные системы
- •Фосфатная буферная система
- •Удаление щелочных эквивалентов фосфатным буфером
- •Бикарбонатная буферная система
- •Белковая буферная система
- •Изменение заряда буферных групп белка при различных рН Гемоглобиновая буферная система
- •Длительная стабилизация сдвигов рН
- •Удаление кислоты через легкие
- •Удаление кислоты через почки
- •Реабсорбция бикарбонат-ионов
- •Реабсорбция бикарбонат-ионов
- •Ацидогенез
- •Реакции ацидогенеза
- •Аммониегенез
- •Реакции аммониегенеза
- •Показатели кислотно-основного состояния
- •Изменение кос - частая ситуация
- •Причины нарушений кислотно-основного состояния
- •Диагностика нарушений кос
- •Использование показателя рСо2 для диагностики нарушений кислотно-основного состояния
Как удаляются ионы водорода?
Метаболическая активность организма сопровождается непрерывным потреблением кислорода, поступлением в среду ионов водорода и углекислого газа. Все это может повлиять на активность гормональных сигналов, ферментативных и транспортных систем клетки.
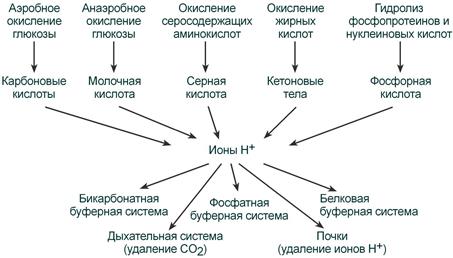
Источники и пути удаления ионов водорода
Для сохранения кислотно-основного гомеостаза в организме необходимо наличие двух крупных систем компенсации сдвигов КОС:
1. Система химических реакций:
действие вне- и внутриклеточных буферных систем (бикарбонатная, фосфатная, белковая, гемоглобиновая),
интенсивность внутриклеточного образования ионов Н+ и НСО3–.
2. Система физиологических механизмов:
легочная вентиляция и удаление СО2.
почечная экскреция ионов Н+, реабсорбция и синтез НСО3–,
пассивное, т.е. нерегулируемое, влияние оказывают печень и костная ткань.
Быстрая компенсация сдвигов рН Буферные системы
Буферные системы – это соединения, противодействующие резким изменениям концентрации ионов Н+. Любая буферная система - это кислотно-основная пара: слабое основание (анион, А–) и слабая кислота (Н-Анион, H-А). Они минимизируют сдвиги количества ионов Н+ в растворе за счет их связывания с анионом и включения в плохо диссоциирующее соединение – в слабую кислоту. Поэтому общее количество ионов Н+ изменяется не так заметно, как это могло бы быть.
Существует три буферные системы жидкостей организма – бикарбонатная, фосфатная, белковая (включая гемоглобиновую).Они вступают в действие моментально и через несколько минут их эффект достигает максимума возможного.
Фосфатная буферная система
Фосфатная буферная система составляет около 2% от всей буферной емкости крови и до 50% буферной емкости мочи. Она образована гидрофосфатом (HPO42–) и дигидрофосфатом (H2PO4–). Дигидрофосфат слабо диссоциирует и ведет себя как слабая кислота, гидрофосфат обладает щелочными свойствами. В норме отношение HРO42– к H2РO4– равно 4 : 1.
При взаимодействии кислот (ионов Н+) с двузамещенным фосфатом (HPO42‑) образуется дигидрофосфат (H2PO4–):
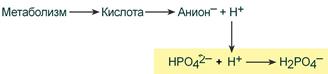
Удаление ионов H+ фосфатным буфером
В результате концентрация ионов Н+ понижается.
При поступлении в кровь оснований (избыток ОН–‑групп) они нейтрализуются поступающими в плазму от H2PO4– ионами Н+:
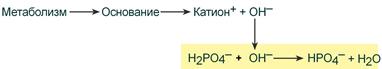
Удаление щелочных эквивалентов фосфатным буфером
Роль фосфатного буфера особенно высока во внутриклеточном пространстве и в просвете почечных канальцев. Кислотно-основная реакция мочи зависит только от содержания дигидрофосфата (H2PO4–), т.к. бикарбонат натрия в почечных канальцах реабсорбируется.
Бикарбонатная буферная система
Эта система самая мощная, на ее долю приходится 65% всей буферной мощности крови. Она состоит из бикарбонат-иона (НСО3–) и угольной кислоты (Н2СО3). В норме отношение HCO3– к H2CO3 равно 20 : 1.
При поступлении в кровь ионов H+ (т.е. кислоты) ионы бикарбоната натрия взаимодействуют с ней и образуется угольная кислота:
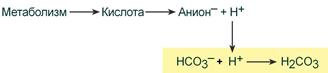
При работе бикарбонатной системы концентрация водородных ионов понижается, т.к. угольная кислота является очень слабой кислотой и плохо диссоциирует. При этом в крови не происходит параллельного значимого увеличения концентрации НСО3–.
Если в кровь поступают вещества с щелочными свойствами, то они реагируют с угольной кислотой и образуют ионы бикарбоната:

Работа бикарбонатного буфера неразрывно связана с дыхательной системой (с вентиляцией легких). В легочных артериолах при снижении плазменной концентрации СО2 и благодаря присутствию в эритроцитах фермента карбоангидразы угольная кислота быстро расщепляется с образованием CO2, удаляемого с выдыхаемым воздухом:
Н2СО3→ Н2О + СО2↑
Кроме эритроцитов, значительная активность карбоангидразы отмечена в эпителии почечных канальцев, клетках слизистой оболочки желудка, коре надпочечников и клетках печени, в незначительных количествах – в центральной нервной системе, поджелудочной железе и других органах.
