- •Газы крови влияют на pH
- •Углекислый газ
- •Кислород
- •Оксигемоглобин
- •Насыщение гемоглобина кислородом
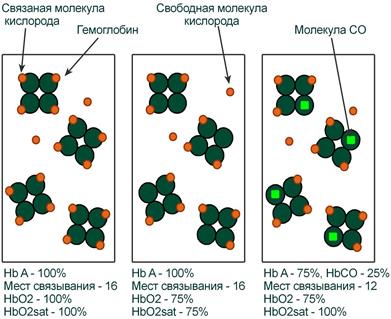
- •Иллюстрация понятий оксигемоглобина (HbO2) и насыщения гемоглобина (HbO2sat) Парциальное давление кислорода (pO2)
- •Кривая диссоциации гемоглобина в норме и при изменении pH и концентрации 2,3-дифосфоглицерата
- •Как удаляются ионы водорода?
- •Источники и пути удаления ионов водорода
- •Быстрая компенсация сдвигов рН Буферные системы
- •Фосфатная буферная система
- •Удаление щелочных эквивалентов фосфатным буфером
- •Бикарбонатная буферная система
- •Белковая буферная система
- •Изменение заряда буферных групп белка при различных рН Гемоглобиновая буферная система
- •Длительная стабилизация сдвигов рН
- •Удаление кислоты через легкие
- •Удаление кислоты через почки
- •Реабсорбция бикарбонат-ионов
- •Реабсорбция бикарбонат-ионов
- •Ацидогенез
- •Реакции ацидогенеза
- •Аммониегенез
- •Реакции аммониегенеза
- •Показатели кислотно-основного состояния
- •Изменение кос - частая ситуация
- •Причины нарушений кислотно-основного состояния
- •Диагностика нарушений кос
- •Использование показателя рСо2 для диагностики нарушений кислотно-основного состояния
Величина рН формирует активность клеток
Кислотно-основное равновесие представляет собой активность физиологических и физико-химических процессов, составляющих функционально единую систему стабилизации концентрации ионов Н+.
Основной количественной характеристикой кислотности водных растворов. является водородный показатель (рН) – отрицательный десятичный логарифм концентрации водородных ионов в растворе, т.е. зависимость pH и [H+] не линейная!
pH=-lg [H+]).
Установленный диапазон концентраций ионов Н+, совместимый с жизнью 16-160 нмоль/л, что соответствует рН 6,8-7,8. В среднем в плазме крови концентрация ионов водорода [Н+] = 40 нмоль/л, нормальный диапазон рН 7,35-7,45.
Сдвиги концентрации ионов Н+ приводят к изменению активности внутриклеточных ферментов даже в пределах физиологических значений. Например, ферменты глюконеогенеза более активны при закислении цитоплазмы гепатоцитов кетоновыми телами или молочной кислотой, что имеет значение при голодании и физической нагрузке.
Закисление саркоплазмы в мышечной клетке при работе подавляет активность фермента 3-й реакции гликолиза фосфофруктокиназы и останавливает сокращение мышцы. Интересной оборотной стороной данного эффекта служит повышенная устойчивость плода и новорожденных к острой гипоксии благодаря наличию особой фосфофруктокиназы, нечувствительной к закислению среды, что позволяет продолжать окисление глюкозы и получать энергию при накоплении лактата.
Роль систем гомеостаза организма – обеспечить неизменность концентрации ионов водорода в клетке и вне ее при жизнедеятельности, что необходимо для:
сохранения активности ферментативных и транспортных белков,
неспецифической защиты кожного эпителия;
отрицательного заряда наружной поверхности мембраны эритроцитов, при снижении величины заряда мембран эритроциты начинают агрегировать, образуя "монетные столбики", что повышает вязкость крови,
растворимости неорганических и органических молекул (кальция и магния, щавелевой и мочевой кислот),
формирования электро-химического градиента мембраны митохондрий на должном уровне и активности катаболических процессов.
Водородный показатель является главным при оценке кислотно-основного состояния и его значение определяет диагноз ацидоза (снижение pH) или алкалоза (повышение pH).
Источники атомов водорода в организме
1. В реакциях аэробного метаболизма глюкозы, аминокислот и жирных кислот постоянно образуются молекулы CO2. При участии фермента карбоангидразы он реагирует с водой и образует угольную кислоту, слабо диссоциирующую на ион Н+ и бикарбонат-ион НСО3 .
СО2 + Н2О → Н2СО3 → НСО3¯ + Н+
Данный способ продукции протонов характерен почти для всех клеток и протекает при аэробном метаболизме, когда активно идут реакции окислительного декарбоксилирования пирувата и цикла трикарбоновых кислот.
2. Еще одним источником кислотных эквивалентов является анаэробный метаболизм глюкозы, при котором появляется молочная кислота.
Глюкоза → Молочная кислота → Лактат¯ + Н+
Особенно ярко это проявляется при интенсивной мышечной работе. В клинической практике с накоплением молочной кислоты сталкиваются при недостаточном поступлении кислорода в клетки – при любых анемиях, шоке, тромбозах, сердечной и дыхательной недостаточности, повышении вязкости крови, обезвоживании. Также играет роль дефицит железа и меди в составе ферментов дыхательной цепи.
3. Метаболизм серусодержащих аминокислот и других соединений приводит к появлению серной кислоты:
Метионин →Н2SО4 → SО42- + 2Н+
Цистеин → Н2SО4 → SО42- + 2Н+
4. В определенных условиях (голодание, сахарный диабет 1 типа) в кровь поступают кетоновые тела (ацетоуксусная и β-гидроксимасляная кислоты):
Жирные кислоты → Ацетил-SКоА → Ацетоуксусная кислота → Ацетоацетат¯ + Н+
Жирные кислоты → Ацетил-SКоА → Гидроксимасляная кислота → Гидроксибутират¯ + Н+
5. При отравлениях органическими соединениями источником ионов Н+ могут служить щавелевая и муравьная кислоты при метаболизме, соответственно, этиленгликоля и метанола.
Газы крови влияют на pH
Несмотря на то, что исследование кислотно-основного состояния, строго говоря, подразумевает исследование только величины pH (концентрации ионов H+), в реальности в него также включается исследование физиологически важных газов, присутствующих в крови – O2 и CO2. Анализ газов показывает эффективность газообмена по величинам парциальных давлений – pO2 и pCO2.
Через альвеолярную мембрану молекулы любых газов перемещаются диффузно по градиенту концентрации. Молекулы O2 атмосферного воздуха поступают из альвеол в кровь, а молекулы CO2 из крови в альвеолы до тех пор, пока их парциальные давления не выровняются.
Величина парциального давления – это процентная доля газа в общем объеме.
Углекислый газ
Концентрация СО2 в альвеолярном воздухе столь низка, а в крови столь высока, что диффузия этого газа в альвеолы чрезвычайно эффективна и скорость его удаления зависит только от альвеолярной вентиляции – общего объема воздуха, транспортируемого в минуту между альвеолами и атмосферой ("скорости выдувания").
Следовательно,
при усиленной вентиляции легких углекислый газ быстро выводится, и показатель pCO2 в крови снижается. Это означает потерю организмом угольной кислоты (ионов H+), что является причиной защелачивания крови – алкалоза, называемого дыхательным или респираторным.
при недостаточной альвеолярной вентиляции величина рСО2 повышается, что свидетельствует о недостаточном его удалении и накоплении H2CO3. Иными словами, повышение в крови показателя рСО2 является причиной дыхательного ацидоза.
Увеличенное pCO2 (гиперкапния) всегда свидетельствует о снижении альвеолярной вентиляции.
Кислород
Вопросы, связанные с оксигенацией крови и транспортом кислорода более сложны. Связано это с тем, что в виде свободных (растворенных) молекул O2 находится лишь небольшая доля общего кислорода крови. Основная часть кислорода связана с гемоглобином (оксигемоглобин) и истинное содержание кислорода зависит от двух дополнительных параметров – концентрации Hb и насыщения (сатурации) гемоглобина кислородом.
Оксигемоглобин
Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину).
Насыщение гемоглобина кислородом
Насыщение гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2.
Отличия между двумя показателями HbО2 и HbOSAT заключаются в том, что у пациентов возможно наличие в крови такой формы гемоглобина, которая не способна акцептировать О2 (Hb‑CO, metHb, сульфоHb). Но так как большинство больных не имеют в крови повышенного содержания этих форм гемоглобина, значения HbО2 и SО2 обычно очень близки.
Например, если при отравлении нитритами количество metHb составляет 15%, тогда величина HbО2 никогда не сможет превысить 85%, но насыщение (HbOsat) может быть различно – от максимума (HbOsat=95-98%) при полном насыщении до низких величин при отсутствии кислорода.
Показатель насыщения кислородом показывает процент доступных мест связывания на гемоглобине.