
Ядерные свойства
Изотопы
Массовое число Период полураспада Тип распада
224 0,6 с α
225 2,0 с α
226 1,8 с α
227 38,3 мин. α
228 22 час. α (2%)
229 1,4 дня α (0,25%),
230 17 дней β− (10%), α (0,003%),
231 32480±260 лет α
232 1,31 дня β−
233 27,4 дня β−
234 (UX2) 1,18 мин. β−
234 (UZ) 6,7 час. β−
235 23,7 мин. β−
236 12,5 мин. β−
237 10,5 мин. β−
В
настоящее время известно 14 изотопов
протактиния. Из них только
и
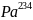 встречаются в природе, остальные получены
искусствен- ным путем.
встречаются в природе, остальные получены
искусствен- ным путем.
Протактиний-231 – единственный природный изотоп доступный в весовых количествах. Он образуется в результате распада :
→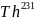 →
→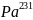 →
→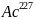
Протактиний -233 – наиболее важный искусственный изотоп, получающийся при облучении тория нейтронами по схеме:
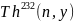
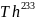 →
→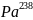 →
→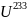
Протактиний-234
- второй природный изотоп элемента,
полученный из
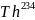 -короткоживущего
β-излучателя, образующегося при распаде
долгоживущего изотопа урана -
-короткоживущего
β-излучателя, образующегося при распаде
долгоживущего изотопа урана -
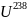 . Протактиний-234 существует в двух
изомерных формах UX2
и UZ.
. Протактиний-234 существует в двух
изомерных формах UX2
и UZ.
Методы и техника получения
Из
природных источников — остатков от
переработки урановой смолки — можно
получить только
.
Кроме того,
можно получить облучением
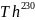 медленными нейтронами:
медленными нейтронами:
(n, γ) → .
или
при облучении
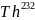 быстрыми нейтронами по реакции
быстрыми нейтронами по реакции
(n,
2n)
→
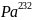 .
.
Изотоп
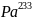 также получают из тория:
также получают из тория:
(n, γ) → .
Металлический протактиний получают при восстановлении PaF4 парами бария или кальция при 1400-1500 С.
Изотоп выделяют из уранового сырья с применением осадительных, экстракционных и ионообменных методов.
Экстракция
ЭКСТРАКЦИЯ (позднелат. extractio - извлечение, от extraho - вытягиваю, извлекаю), перевод одного или несколько компонентов раствора из одной органической фазы в контактирующую и не смешивающуюся с ней другую водную фазу.
Экстракция – процесс извлечения вещества (соединения металла) из водного раствора в жидкую органическую фазу, не смешивающуюся с водой.
Экстракция может быть разовой (однократной или многократной) или непрерывной. Простейший способ экстракции из раствора — однократная или многократная промывка экстрагентом в делительной воронке.
Сущность экстракции:
водный раствор, содержащий экстрагируемое вещество обрабатывается избирательным органическим растворителем (экстрагентом). Вещество распределяется между водным раствором и растворителем в количествах, зависящих от его коэффициента распределения между двумя жидкими фазами и количественного соотношения этих фаз. Переход вещества из водной в органическую фазу совершается до тех пор, пока не будет достигнута в системе равновесие, которая определяется коэффициентом распределения.
Существует два механизма экстракции:
физическая - распределяемое вещество не взаимодействует на с органической, ни с водной фазами ( экстракция проводится нейтральными реагентами )
химическая (анионо- и катионообменная экстракция) при которой распределяемое вещество претерпевает химические превращения как в водной так и в органической фазах .
Закон распределения. Закон Генри – Нернста.
Закон распределения, в одинаковых степенях, справедлив для физического и химического механизмов экстракции. Процесс экстракции подчиняется закону распределения, который гласит, что для данной температуры отношения концентрации вещества между двумя несмешивающимися жидкостями, является величиной постоянной при различных концентрациях вещества в условиях равновесия.
Определения:
Экстрагент – органическое вещество, образующее с извлекаемым элементом, соединения способные растворяться в органической фазе (кислоты, спирты, эфиры, кетоны)
Разбавитель – органическое жидкое вещество, не смешивающее с водой, служащий растворителем экстрагента (керосин и т.д.). Благодаря разбавителю можно использовать экстрагенты или улучить физические характеристики жидких экстрагентов.
Высаливатель – неорганическое вещество (электролит) улучающий показатель экстракции.
Экстракт – органическая фаза после экстракции.
Рафинат – объединённая водная фаза.
Реэкстракт – водная фаза после экстракции, то есть извлечение металла из экстракта в водный раствор
Стадии:
привидение в контакт и диспергирование фаз.
разделение фаз на экстракт и рафинат.
выделение целевых компонентов из экстракта и регенерация экстрагента, для чего на ряду с дистилляцией применяют реэкстракцию, обрабатывают экстракт водным раствором вещества, обеспечивает полный перевод целевых компонентов в раствор или осадок и их концентрирование.
промывка экстрагента для уменьшения содержания и удаления механического, захваченного исходного раствора.
Свойства экстрагента:
- несмшиваемость;
- хорошая экстрагируемая способность и селективность;
- малая растворимость в воде, кислотах, щелочах;
- регенирация, устойчивость в водных растворах;
-отличная плотность;
-низкая вязкость, трудновоспламеняемость, нетоксичные.
В водных растворах ионы гидротируются и прочно удерживаются в водной фазе. Их извлечение происходит, если процесс сопровождается низкой энергий Гибсса. Это условие может быть выполнено при использовании в качестве экстрагентов органические соединения при взаимодействии которые с извлекаемым ионом будет компенсироваться энергия. Отвечающие этому условию органические вещества можно подразделить на две группы:
нейтральные экстрагенты, которые способны к образованию координационных связей с извлекаемым ионом, более прочным, чем связи молекулы воды ( Есольв.
 Егидр.)
Егидр.)ионообменные органические кислоты и их соли, органические основания, способны при контакте с водным раствором к обмену неорганического катиона или аниона на одноименный ион, находящейся в растворе
Эктсракционные процессы по типу применяемых экстрагентов делятся на:
экстракция нейтральными экстрагентами;
анионообменная экстракция;
катионообменная экстракция.
Для того чтобы нитратные соединения актинидов переходили в органическую фазу, необходимо наличие химической связи между экстрагентом и нитратами извлекаемым элементом и образуют растворимые в органической фазе координационные соединения.
Экстрагенты проявляют склонность к комплексообразованию, и чем выше их полярность, тем выше экстракционная способность, но при этом они больше растворимы в воде.
Склонность ТБФ к сольватации – результат его высокой донорной способности, связан с наличием фосфорной группы Р=О, в состав которой входит основной атом О.
Сольватация солей ТБФ осуществляется путем присоединения молекул ТБФ к катиону соли.
Основние константы и коэффициенты экстракции
Коэффициент распределения (D) – отношения концентрации элемента в органической и в водной фазе в условиях равновесия
D=
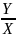 (1)
(1)
Классификация коэффициентов подразделяется по:
- концентрация извлекаемого элемента;
- по количеству извлекаемого элемента;
- по доле извлекаемого элемента.
Коэффициент экстракции (µ) – отношения количества перешедшего в органическую фазу к равновесному количеству этого вещества в водном растворе.
µ
=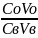 =
D·n
(2)
=
D·n
(2)
Для
успешного выделения вещества необходимо,
что бы µ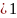
Степень извлечения (Е)- доля вещества перешедшего в органическую фазу.
Е
=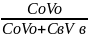 (3)
(3)
n- отношения объёмов в органической и в водной фазах.
n
=
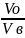 (4)
(4)
Кажущая константа (К)-
