
- •Роль высокоэнергетических фосфатов как “энергетической валюты” клетки
- •Понятие об энергетическом заряде клетки
- •Механизмы образования атф в клетке
- •Имеется два пути синтеза атф в клетке: 1) окислительное фосфорилирование и 2) субстратное фосфорилирование.
- •Цепь переноса электронов (цпэ) или дыхательная цепь
- •Хемиосмотическая гипотеза сопряжения окисления и фосфорилирования
- •Коэффициент фосфорилирования
- •Дыхательный контроль
- •Разобщение окисления и фосфорилирования
- •Ингибиторы тканевого дыхания
- •Энергетический обмен и теплопродукция
- •Фазы освобождения энергии из питательных веществ
- •Общие пути катаболизма
- •Окислительное декарбоксилирование пирувата
- •Реакции окислительного декарбоксилирования пирувата
- •Регуляция окислительного декарбоксилирования
- •Цикл лимонной кислоты
- •Реакции цикла лимонной кислоты
11
Образование
ацетил-КоА из пирувата - ключевой
необратимый этап метаболизма, поэтому
ПДК имеет сложную систему регуляции и
реализуется через киназу и фосфатазу
(субъединицы ПДК). В результате
фосфорилирования под действием киназы
ПДК переходит в неактивную форму, при
дефосфорилировании фосфатазой - в
активную форму. Активность киназы и
фосфатазы регулируется многими
аллостерическими эффекторами. Киназа
ПДК аллостерически активируется АТФ,
следовательно, при накоплении АТФ
прекращается
дальнейшее превращение пирувата в
ацетил-КоА. Киназа ПДК аллостерически
ингибируется пируватом, АДФ, Са²+
.
Две
последние реакции необходимы для
регенерации активных форм коферментов,
участвующих в окислительном
декарбоксилировании пирувата.
Образовавшийся в пятой реакции НАДННГ
поступает в дыхательную цепь.
Суммарное
уравнение окислительного декарбоксилирования
пирувата:Реакции окислительного декарбоксилирования пирувата
Регуляция окислительного декарбоксилирования
Цикл лимонной кислоты
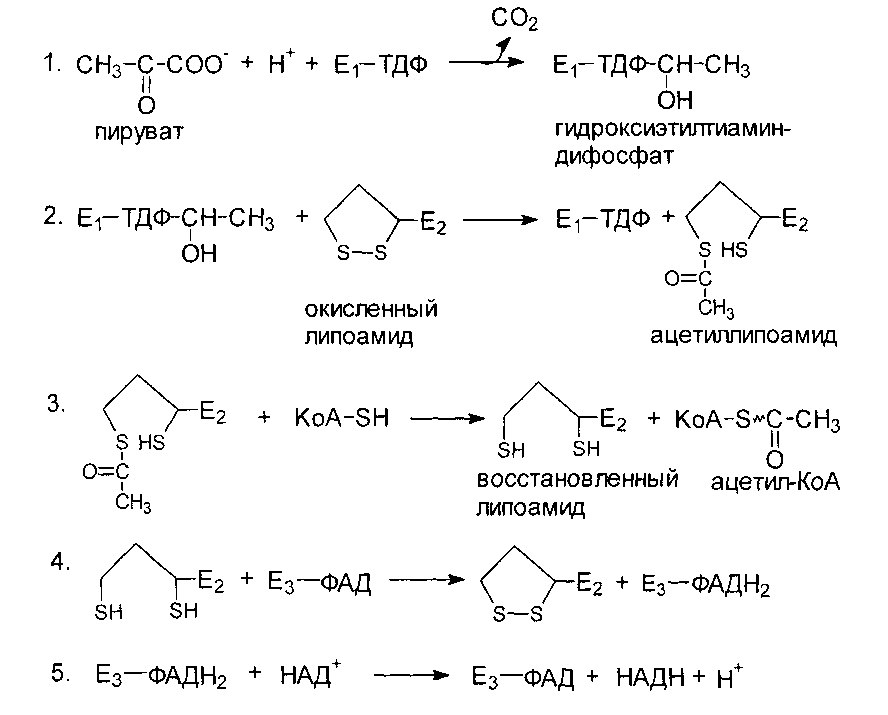
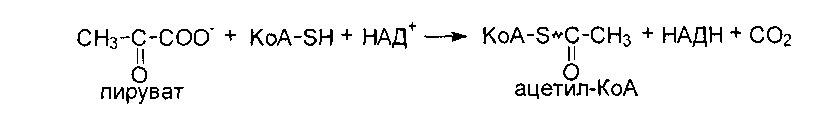
Реакции
ЦЛК протекают в матриксе митохондрий.
Е1
- цитратсинтаза, является регуляторным
ферментом. Цитратсинтазная реакция
лимитирует скорость всего процесса.
Превращение
цитрата в изоцитрат катализирует
аконитатгидратаза (Е2),
содержащая ионы Fe2+.
Эта реакция осуществляется в две стадии:
сначала происходит дегидратация с
образованием цис-аконитата, а затем
гидратация с образованием изоцитрата.
Реакция
ингибируется фторацетатом, в результате
накапливается цитрат.
Реакции цикла лимонной кислоты
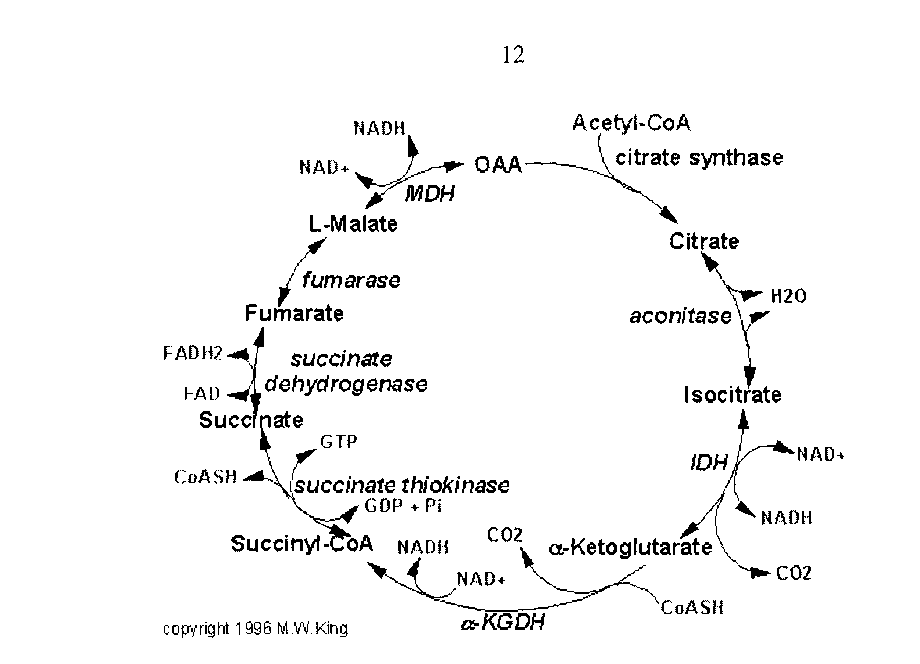
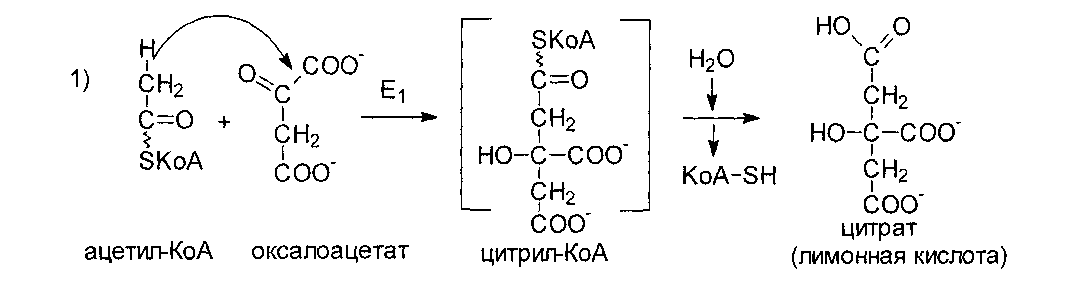

13
Далее
изоцитратдегидрогеназа (Е3)
катализирует дегидрирование с
образованием оксалосукцината, а затем
следует декарбоксилирование под
действием того же фермента.
2-Оксоглутарат
подвергается окислительному
декарбоксилированию, сходному с
окислительным декарбоксилированием
пирувата.
Эта
реакция катализируется 2-оксоглутаратным
комплексом (ЕД который
состоит
из 3-х ферментов: 2-оксоглутаратдегидрогеназы,
дигидролипоилсукцинилтрансферазы
и дигидролипоилдегидрогеназы и пяти
коферментов: тиаминдифосфата, липамида,
НАД+,
ФАД, KoA-SH.
Таким образом, 2-ксоглутаратдегидрогеназный
комплекс по строению аналогичен
пируватдегидрогеназному комплексу.
Однако, первый фермент данного комплекса
не имеет такой сложной регуляции как
пируватдегидрогеназа. В результате
окислительного декарбоксилирования
2-оксоглутарата образуется сукцинил-КоА,
содержащий макроэргическую связь.
Реакция ингибируется арсенатом, что
приводит к накоплению 2-оксоглутарата.
Под
действием фермента сукцинил-КоА-синтетатазы
энергия макроэргической связи
сукцинил-КоА запасается в форме
макроэргической связи в молекуле ГТФ
(субстратное фосфорилирование).
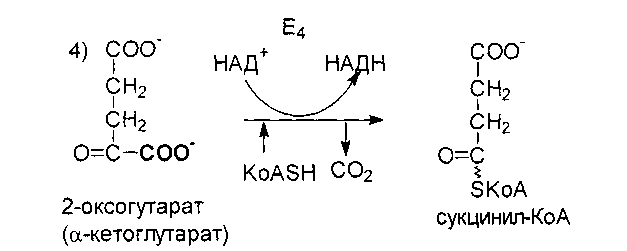
2-Оксоглутарат
подвергается окислительному
декарбоксилированию, сходному с
окислительным декарбоксилированием
пирувата.
Эта
реакция катализируется 2-оксоглутаратным
комплексом (Е4)
который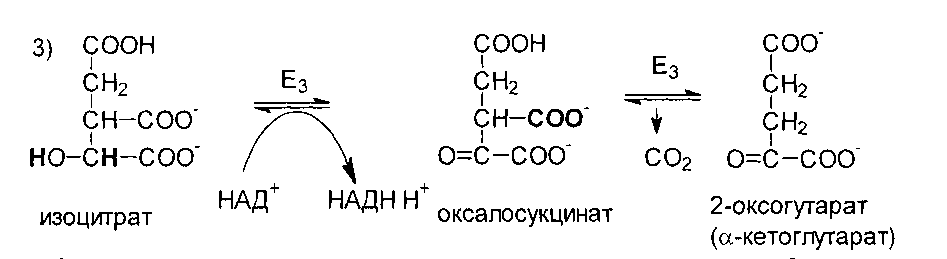

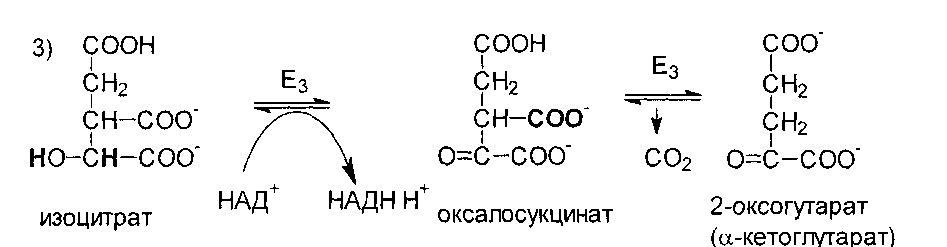
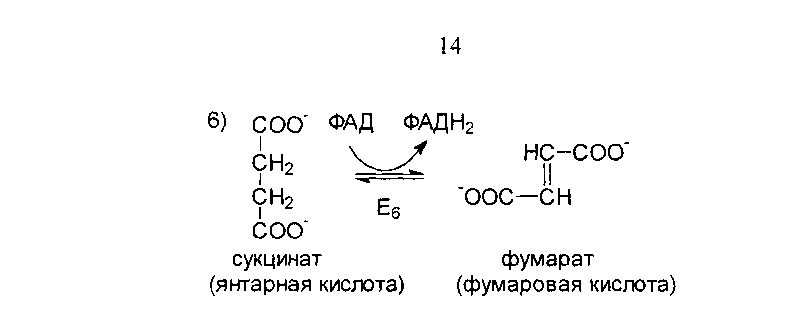
Далее
сукцинат под действием сукцинатдегидрогеназы
(Е6)
превращается в фумарат. Это единственная
реакция ЦЛК, в ходе которой осуществляется
прямой перенос атомов водорода с
субстрата на флавопротеин ЦПЭ без
участия НАД+.
Коферментов данного фермента является
ФАД.
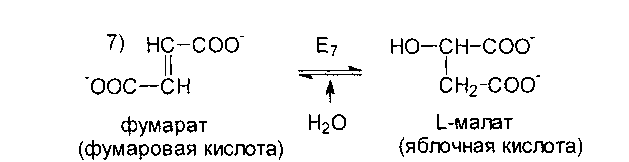
Затем
к фумарату присоединяется молекула
Н2О
под действием фумаратгидратазы (Е7)
с образованием малата.
Малатдегидрогеназа
(E8)
катализирует превращение малата в
оксалоацетат, реакция идет с участием
НАД+.
Хотя реакция обратима, реально она
протекает в направлении образования
оксалоацетата, поскольку он вместе с
НАДН-Н+
постоянно потребляется в других
реакциях.
Регуляция
ЦЛК
Осуществляется
на уровне цитратсинтазной реакции.
Скорость реакции возрастает при
повышении концентрации оксалоацетата
и снижается при повышении концентраций
АТФ, сукцинил-КоА длинноцепочечных
жирных кислот.
Значение
ЦЛК
Амфиболическая
функция: а) катаболическая - в ЦЛК
происходит утилизация ацетильных
групп; б) анаболическая - метаболиты
ЦЛК служат предшественниками при
синтезе ряда веществ в организме:
аминокислот, жирных кислот, глюкозы и
других соединений. Например, из
сукцинил-КоА образуются порфирины
(предшественник гема), из 2-оксоглутарата
в результате реакции переаминирования
с аминокислотой образуется глутамат.
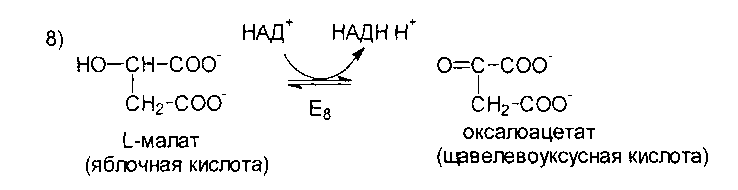
15
Водороддонорная
функция: в ЦЛК образуется 3 молекулы
НАДН-Н+ и 1 молекула ФАДН2.
Энергетическая
функция: с восстановленных коферментов
водород передается в ЦПЭ, где в результате
окислительного фосфорилирования
образуется АТФ. При этом на каждую
молекулу НАДНН+ в митохондриях
образуется 3 молекулы АТФ, на каждую
молекулу ФАДН2 - 2 молекулы АТФ.
Т.о. при окислении одного ацетильного
остатка путем окислительного
фосфорилирования образуется 11 мол. (9
+ 2) АТФ. Еще одна молекула (ГТФ) образуется
путем субстратного фосфорилирования
в ходе сукцинил-КоА- синтетазной
реакции. После суммирования получаем
11 + 1 = 12 мол. АТФ (в расчете на один
ацетильный остаток).
