
Тема 2. Расчет тепловых эффектов химических реакций при различных температурах
Задача №6
Вычислите
среднюю теплоемкость
![]() вещества, приведенного в табл. 6, в
интервале температур от 298 до Т
К.
вещества, приведенного в табл. 6, в
интервале температур от 298 до Т
К.
Таблица 6
Вари-ант |
Вещество |
Т, К |
Вари-ант |
Вещество |
Т, К |
1 |
|
500 |
16 |
|
500 |
2 |
|
550 |
17 |
|
550 |
3 |
|
600 |
18 |
|
600 |
4 |
|
650 |
19 |
|
650 |
5 |
|
700 |
20 |
|
700 |
6 |
|
750 |
21 |
|
750 |
7 |
|
800 |
22 |
|
800 |
8 |
|
850 |
23 |
|
850 |
9 |
|
900 |
24 |
|
900 |
10 |
|
950 |
25 |
|
950 |
11 |
|
1000 |
26 |
|
1000 |
12 |
|
1050 |
27 |
|
1050 |
13 |
|
1100 |
28 |
|
1100 |
14 |
|
1150 |
29 |
|
1150 |
15 |
|
1200 |
30 |
|
1200 |
Решение:
Рассмотрим расчет средней теплоемкости аммиака в интервале температур от 298 до 800 К.
Теплоемкость – это отношение количества теплоты, поглощаемой телом при нагревании, к повышению температуры, которым сопровождается нагревание. Для индивидуального вещества различают удельную (одного килограмма) и мольную (одного моля) теплоемкости.
Истинная теплоемкость
![]() ,
(21)
,
(21)
где δQ – бесконечно малое количество теплоты, необходимое для повышения температуры тела на бесконечно малую величину dT .
Средняя теплоемкость – это отношение количества теплоты Q к повышению температуры ∆T = T2 – T1,
![]() .
.
Поскольку теплота не является функцией состояния и зависит от пути процесса, необходимо указывать условия протекания процесса нагревания. В изохорном и изобарном процессах для бесконечно малого изменения δQV = dU и δQp = dH, поэтому
![]() и
и
![]() .
(22)
.
(22)
Связь
между истинными
изохорной (СV)
и изобарной
(Cp)
теплоемкостями
вещества и его средними
изохорной
и изобарной
![]() теплоемкостями
в интервале температур от Т1
до Т2
выражается уравнениями (23) и (24):
теплоемкостями
в интервале температур от Т1
до Т2
выражается уравнениями (23) и (24):
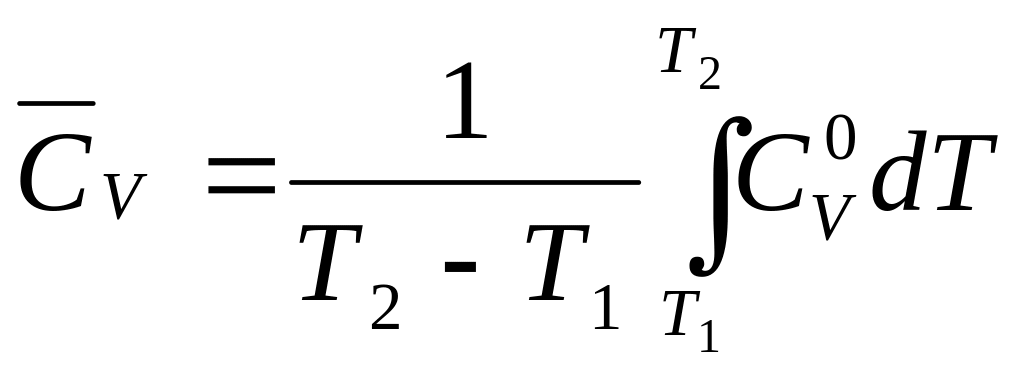 ;
(23)
;
(23)
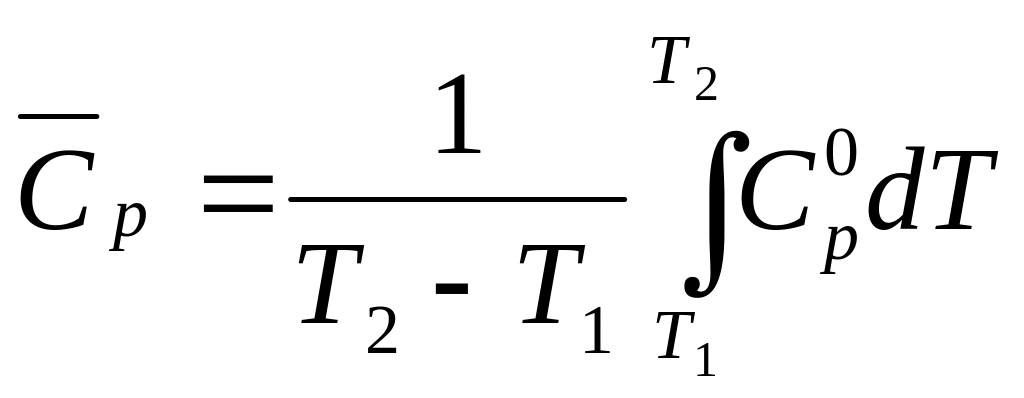 .
(24)
.
(24)
Зависимости истинной теплоемкости от температуры выражаются следующими эмпирическими уравнениями:
![]() ;
(для неорганических веществ) (25)
;
(для неорганических веществ) (25)
![]() .
(для органических веществ) (26)
.
(для органических веществ) (26)
Воспользуемся справочником физико-химических величин. Выпишем коэффициенты (a, b, c) уравнения зависимости изобарной теплоемкости аммиака от температуры:
Таблица 7
-
Вещество
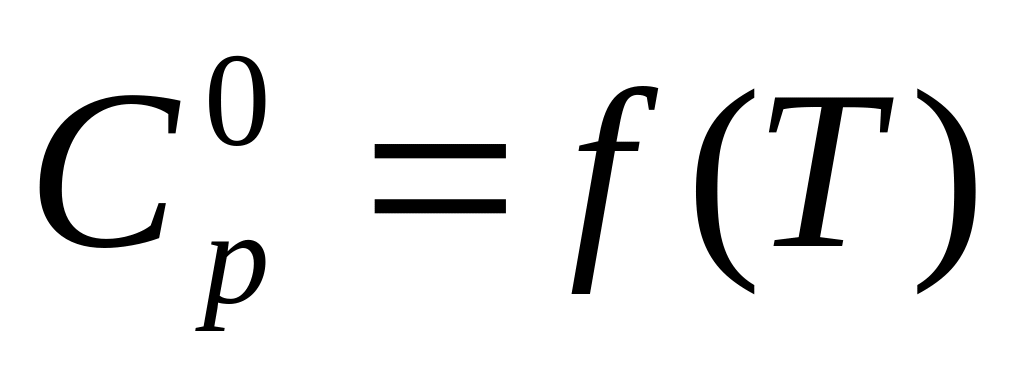
a
b·103
c/·10–5
NH3(Г)
29,8
25,48
–1,67
Запишем уравнение зависимости истинной теплоемкости аммиака от температуры:
![]() .
.
Подставим это уравнение в формулу (24) и вычислим среднюю теплоемкость аммиака:
![]() =
1/(800-298)
=
1/(800-298)![]() =
=
= 0,002 [29,8(800–298) + 25,5·10–3/2 (8002 – 2982) +
+ 1,67·105 (1/800 – 1/298)] = 43,5 Дж/моль·К.
