
Задача №2
Определите тепловой эффект реакции, приведенной в табл. 2, при T = 298 К и р = 1,0133·105 Па:
а) по стандартным теплотам образования исходных и конечных веществ;
б) по стандартным теплотам сгорания исходных и конечных веществ.
Таблица 2
Вариант |
Реакция |
1 |
|
2 |
|
3 |
|
4 |
|
5 |
|
6 |
|
7 |
|
8 |
|
9 |
|
10 |
|
11 |
|
12 |
|
13 |
|
14 |
|
15 |
|
16 |
|
17 |
|
18 |
|
19 |
|
20 |
|
21 |
|
22 |
|
Продолжение таблицы 2 |
|
Вариант |
Реакция |
23 |
|
24 |
|
25 |
|
26 |
|
27 |
|
28 |
|
29 |
|
30 |
|
Решение:
Решение задачи рассмотрим на примере реакции синтеза аммиака:
![]() .
.
а) Согласно следствию из закона Гесса, тепловой эффект реакции при стандартных условиях равен разности сумм стандартных теплот образования продуктов и исходных веществ:
![]() ,
(16)
,
(16)
где
![]() – стехиометрические коэффициенты
веществ в уравнении реакции.
– стехиометрические коэффициенты
веществ в уравнении реакции.
Воспользуемся справочником физико-химических величин (табл.3):
Таблица 3
-
Вещество
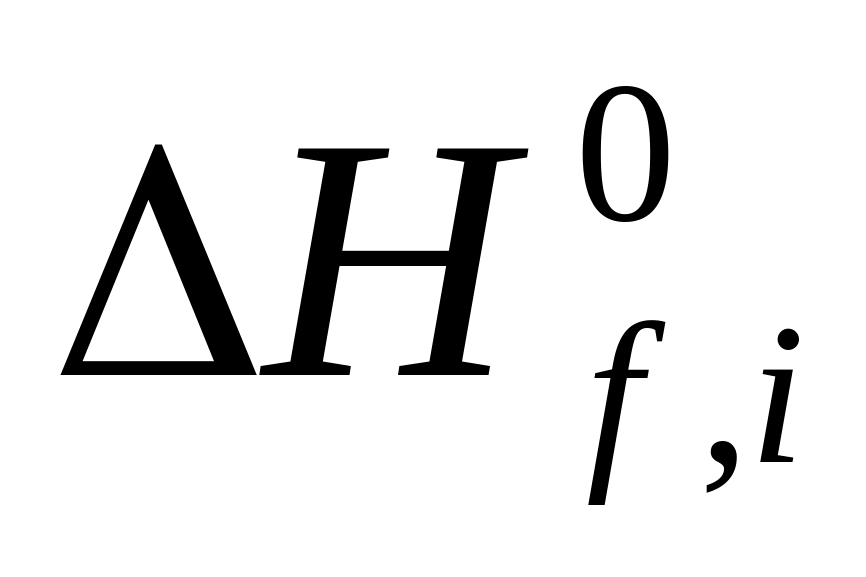 ,
кДж/моль
,
кДж/мольN2
0
H2
0
NH3
–45,94
![]() ,
,
![]() = 2·(–45,94) – (0 + 3·0)
= –91,88 кДж.
= 2·(–45,94) – (0 + 3·0)
= –91,88 кДж.
б) Для реакций, протекающих с участием органических веществ, тепловой эффект реакции при стандартных условиях можно определять и по стандартным теплотам сгорания как разность сумм стандартных теплот сгорания исходных веществ и продуктов реакции:
![]() . (17).
. (17).
в) При отсутствии данных о теплотах образования или сгорания веществ, участвующих в реакции, можно вычислить тепловой эффект реакции, используя для этого методы приближенного расчета тепловых эффектов, например, по энергиям химических связей. В этом методе расчета сначала предполагают разложение исходных простых веществ на атомы, а затем образование из них конечного газообразного соединения. Первый этап связан с затратой энергии на разрыв связей в исходных простых веществах, а второй – с выделением энергии образования новых связей. Поэтому тепловой эффект реакции может быть определен по уравнению
![]() ,
(18)
,
(18)
где n – число связей данного вида; ε – энергия разрыва или образования связей; n* – число атомов твердых элементов; Qвозг – теплота возгонки твердого элемента..
