
- •1. Основные термодинамические параметры и уравнения состояния рабочего тела
- •2. Основные термодинамические функции
- •3. Теплоемкость газов
- •3.1. Основные определения
- •3.2. Истинная и средняя теплоемкости
- •3.3. Зависимость теплоемкости от характера процесса
- •4. Основные законы термодинамики
- •4.1. Первый закон
- •4.2. Второй закон
- •5. Процессы изменения состояния идеальных газов
- •5.1. Изохорный процесс
- •5.2. Изобарный процесс
- •5.3. Изотермический процесс
- •5.4. Адиабатный процесс
- •5.5. Политропный процесс
- •6. Круговые процессы
- •7. Реальные газы
- •7.1. Основные понятия
- •7.2. Водяной пар
- •7.3. Определение параметров воды и водяного пара
- •7.3.1. Параметры кипящей жидкости
- •7.3.2. Параметры сухого насыщенного пара
- •7.3.3. Параметры влажного насыщенного пара
- •7.3.4. Параметры перегретого пара
- •7.4. Общий метод расчета термодинамических процессов паров
- •8. Задания для курсовой работы
- •8.1. Расчет газового цикла
- •8.2. Расчет парового цикла
- •Библиографический список
- •Оглавление
8. Задания для курсовой работы
8.1. Расчет газового цикла
25 вариантов задания приведены в табл. 1 приложения. Условия индивидуального задания берутся в соответствии с вариантом (графа 1).
Газовый цикл задан следующим образом: каждый из 4 процессов описан соответствующим показателем политропы (графы 2, 3, табл. 1 приложения); приведены термодинамические параметры некоторых точек цикла (графы 3–7, табл. 1 приложения); цикл отнесен к 1 кг воздуха.
Требуется произвести расчет газового цикла по законам и аналитическим зависимостям идеального газа.
Для каждого процесса, входящего в цикл, используя данные задания и характеристические уравнения, определить начальные и конечные параметры: давление, удельный объем, температуру, энтальпию, энтропию. Полученные результаты внести в табл. 8.1.1.
Таблица 8.1.1
Точки |
p |
v |
T |
u |
h |
s |
|||||
Па |
кгс/см2 |
м3/кг |
К |
ºС |
кДж/кг |
ккал/кг |
кДж/кг |
ккал/кг |
кДж/кг·К |
ккал/кг·ºС |
|
1 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
Определить характеристики цикла, используя аналитические зависимости соответствующих процессов и данные табл. 8.1.1. Полученные результаты внести в табл. 8.1.2 с учетом знака.
Таблица 8.1.2
Процесс |
∆u |
∆h |
∆s |
q |
l |
|||||
кДж/кг |
ккал/кг |
кДж/кг |
ккал/кг |
кДж/кг·К |
ккал/кг·ºС |
кДж/кг |
ккал/кг |
кДж/кг |
ккал/кг |
|
1–2 |
|
|
|
|
|
|
|
|
|
|
2–3 |
|
|
|
|
|
|
|
|
|
|
3–4 |
|
|
|
|
|
|
|
|
|
|
4–1 |
|
|
|
|
|
|
|
|
|
|
Для цикла в целом определить подведенное тепло, отведенное тепло, работу цикла.
Перенести цикл по результатам расчета в T,s-и p,v-координаты.
Определить термический к.п.д. цикла. Сравнить полученный к.п.д. с термическим к.п.д. цикла Карно, совершенного при тех же крайних температурах.
Пример расчета
Вариант 0.
Цикл задан следующим образом:
p1 = 2 бар = 2 · 105 Па;
p2 = 12 бар = 12 · 105 Па;
v1 = 0,45 м3/кг;
t3 = 300 ºС ;
n1–2 = k,
n2–3 = ∞,
n3–4 = k,
n4–1 = 0.
Решение.
Определим начальные и конечные параметры каждого процесса, входящего в цикл:
1–2 – адиабатный процесс, так как показатель политропы n = k. Для воздуха как двухатомного газа k =1,4.
Запишем зависимость между параметрами газа в процессе: , где
p1 = 2 бар = 2 · 105 Па, p2 = 12 бар = 12 · 105 Па, v1 = 0,45 м3/кг, k =1,4.
Тогда
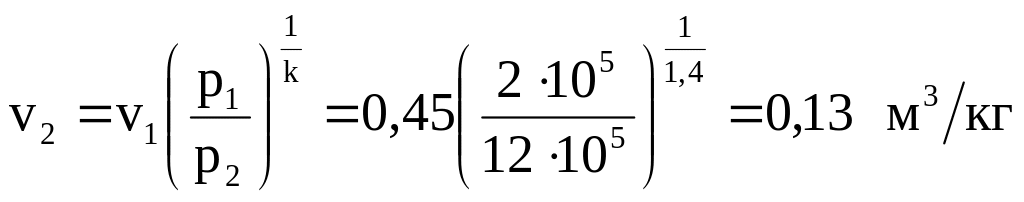 .
.
Запишем уравнение
состояния идеального газа для точки
1:
![]() ,
,
где
R0
– газовая
постоянная, R0
= 287Дж/кг·К, тогда
![]() .
.
Запишем зависимость
меду параметрами р и Т:
![]() ,
тогда
,
тогда
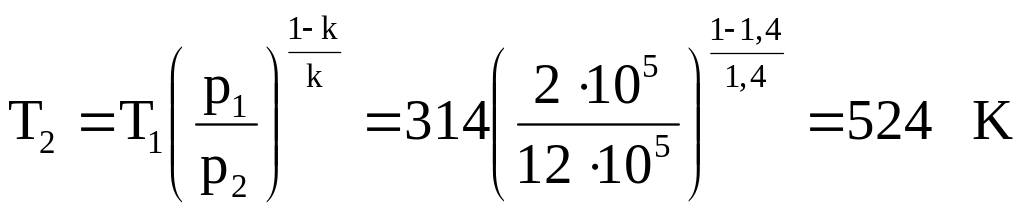
Для
определения термодинамических функций
находим изобарную и изохорную
теплоемкости, используя закон Майера
и выражение для показателя адиабаты:
![]() ;
;
![]() ;
;
![]() .
.
Вычислим внутреннюю энергию в точке 1: u1=cvT1=717,75·314=227 кДж/кг.
Вычислим энтальпию в точке 1: h1=u1+p1v1=227·103 + 2·105·0,45=317 кДж/кг.
Вычислим энтропию
в точке 1:
![]() .
.
2–3 – изохорный процесс, т.к. показатель политропы n = ∞.
Запишем
зависимость между параметрами р и Т:
![]() ,
где
,
где
p1
= 2 бар = 2 ·
105
Па, Т2=524
К, Т3=573
К, тогда
![]() .
.
v3 = v2 = 0,13 м3/кг, т.к. процесс изохорный (v = const).
Вычислим внутреннюю энергию в точке 2: u2=cvT2=717,75·524=379 кДж/кг.
Вычислим энтальпию в точке 2: h2=u2+p2v2=379·103 +12·105·0,13=535 кДж/кг.
Вычислим энтропию
в точке 2:
![]() .
.
3–4 – адиабатный процесс, так как показатель политропы n = k. Для воздуха как двухатомного газа k =1,4.
Запишем зависимость
между параметрами газа в процессе:
,
где р3=13·105
Па, v2
= 0,13 м3/кг,
р4 =
2·105 Па
(так как процесс 4–1 – изобарный, то
р4=р1=2·105
Па), k
= 1,4, тогда:
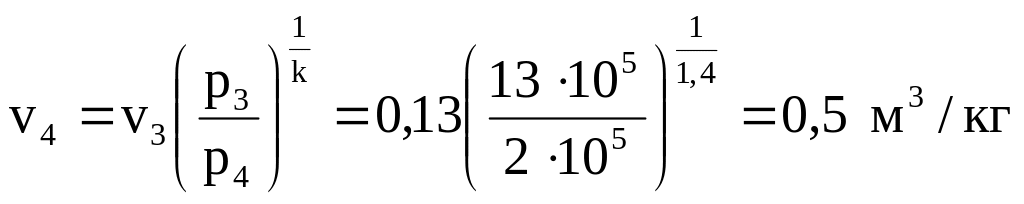 .
.
Вычислим внутреннюю энергию в точке 3: u3=cvT3=717,75·573=411 кДж/кг.
Вычислим энтальпию в точке 3: h3=u3+p3v3=411·103 +13·105·0,13=580 кДж/кг.
Вычислим энтропию
в точке 3:
![]() .
.
4–1 – изобарный процесс, так как показатель политропы n = 0.
Запишем
уравнение состояния идеального газа
для точки 4:![]() ,
,
где
R0
– газовая
постоянная, R0
= 287Дж/кг·К, тогда
![]() .
.
Вычислим внутреннюю энергию в точке 3: u4=cvT4=717,75·350=253 кДж/кг.
Вычислим энтальпию в точке 3: h4=u4+p4v4=253·103 + 2·105·0,5=353 кДж/кг.
Вычислим энтропию
в точке 3:
![]() .
.
Таблица 8.1.1
Точки |
p |
v |
T |
u |
h |
s |
|||||
Па |
кгс/см2 |
м3/кг |
К |
ºС |
кДж/кг |
ккал/кг |
кДж/кг |
ккал/кг |
кДж/кг·К |
ккал/кг·ºС |
|
1 |
2·105 |
2,04 |
0,45 |
314 |
41 |
227 |
54,05 |
317 |
74,48 |
–0,05 |
–0,0119 |
2 |
12·105 |
12,24 |
0,13 |
524 |
251 |
379 |
90,24 |
535 |
127,38 |
–0,05 |
–0,0119 |
3 |
13·105 |
13,26 |
0,13 |
573 |
300 |
411 |
97,86 |
580 |
138,1 |
0,03 |
0,0071 |
4 |
2·105 |
2,04 |
0,5 |
350 |
77 |
253 |
60,24 |
353 |
84,05 |
0,05 |
0,0119 |
Определим характеристики цикла, используя аналитические зависимости соответствующих процессов.
1–2 – адиабатное сжатие.
Вычислим изменение
внутренней энергии:
![]() .
.
Вычислим изменение
энтальпии:
![]() .
.
Вычислим изменение энтропии: ∆s = 0; s = const.
Вычислим теплоту: q1–2 = 0.
Вычислим работу: l = –∆u = –152 кДж/кг.
2–3 – изохорное нагревание.
Вычислим изменение
внутренней энергии:
![]() .
.
Вычислим изменение
энтальпии:
![]() .
.
Вычислим изменение
энтропии:
![]() .
.
Вычислим теплоту:
q1–2
= ∆u
=
![]() .
.
Вычислим работу: l = 0.
3–4 – адиабатное расширение.
Вычислим изменение
внутренней энергии:
![]() .
.
Вычислим изменение
энтальпии:
![]() .
.
Вычислим изменение энтропии: ∆s = 0; s = const.
Вычислим теплоту: q3–4 = 0.
Вычислим работу: l = –∆u = –158 кДж/кг.
4–1 – изобарное сжатие.
Вычислим изменение
внутренней энергии:
![]() .
.
Вычислим изменение
энтальпии:
![]() .
.
Вычислим изменение
энтропии:
![]() .
.
Вычислим теплоту:
q4–1
= сp(T1
– T4)=
![]() .
.
Вычислим работу:
![]() =287,1·(314
– 350) = –10
=287,1·(314
– 350) = –10![]() .
.
Процесс |
∆u |
∆h |
∆s |
q |
l |
|||||
кДж/кг |
ккал/кг |
кДж/кг |
ккал/кг |
кДж/кг·К |
ккал/кг·ºС |
кДж/кг |
ккал/кг |
кДж/кг |
ккал/кг |
|
1–2 |
152 |
36,19 |
213 |
50,71 |
0 |
0 |
0 |
0 |
–152 |
–36,19 |
2–3 |
– 32 |
–7,62 |
45 |
10,71 |
0,08 |
0,019 |
32 |
7,62 |
0 |
0 |
3–4 |
–158 |
–37,62 |
–226 |
–53,81 |
0 |
0 |
0 |
0 |
158 |
37,62 |
4–1 |
26 |
6,19 |
36 |
8,57 |
–0,1 |
–0,024 |
–36,5 |
–8,69 |
–10 |
–2,38 |
Таблица 8.1.2
Для цикла в целом определяем:
подведенное тепло
![]() ;
;
отведенное тепло
![]() ;
;
работу цикла
![]() .
.
Переносим цикл по результатам расчета в T,s- и p,v-координаты.
Определяем термический к.п.д. цикла. Сравниваем полученный к.п.д. с термическим к.п.д. цикла Карно, совершенного при тех же крайних температурах.
Термический к.п.д.
данного цикла
![]() .
.
Термический к.п.д.
цикла Карно
![]() .
.
Термический к.п.д. цикла Карно, совершаемого при тех же крайних температурах, что и данный цикл, на 31% выше. Для получения более высокого к.п.д. цикла необходимо увеличивать разность между крайними температурами.
