
2. Цтк (Цикл Кребса) (Изоцитрат → α-кг; α-кг-сукцинил-КоА; сукцинат → фумарат)
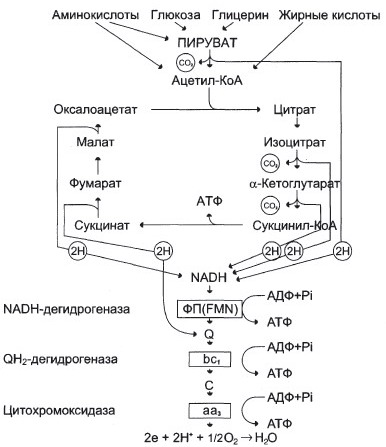
в), г) Витамин B2 – предшественник FAD, который участвует в ЦТК
д), е) Витамин B1 – предшественник FMN, который участвует в ЦПЭ (цепь переноса электронов)
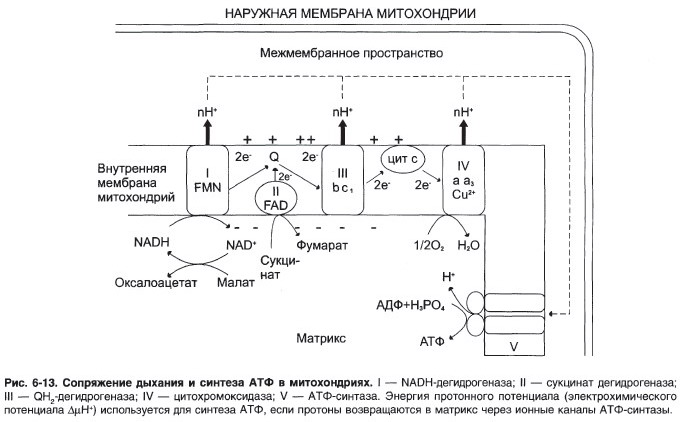
№ 7 В клетках костного мозга протекает следующий метаболический путь:
E1 E2 E3 E4 En
Глицин + Сукцинил-КоА → 5-аминолевулиновая кислота ↔ Р2 ↔ Р3 ↔ P4 ........... ↔ P
При повышении концентрации конечного продукта синтез его прекращается. Объясните, как регулируется скорость процесса, для этого:
а) Назовите, какие ферменты являются регуляторными в данной цепи реакций;
б) Нарисуйте схему строения одного из регуляторных ферментов, перечислите его структурно-функциональные особенности и укажите все лиганды, которые могут взаимодействовать с этим ферментом;
в) Назовите вид регуляции активности фермента данного метаболического пути.
Процесс – синтез гема.
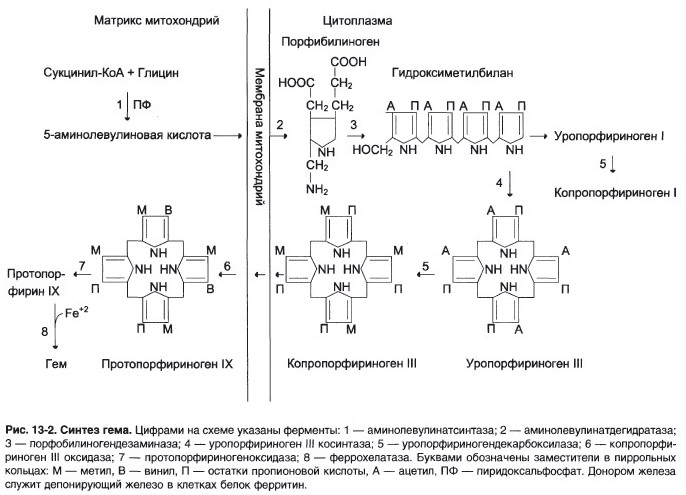
а) Регуляторные ферменты – аминолевулинатсинтаза и аминолевулинатдегидратаза.
б)
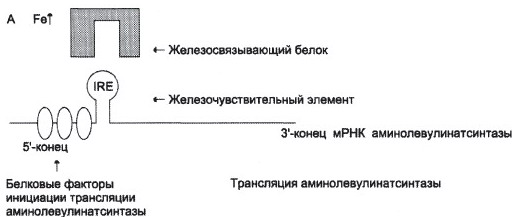
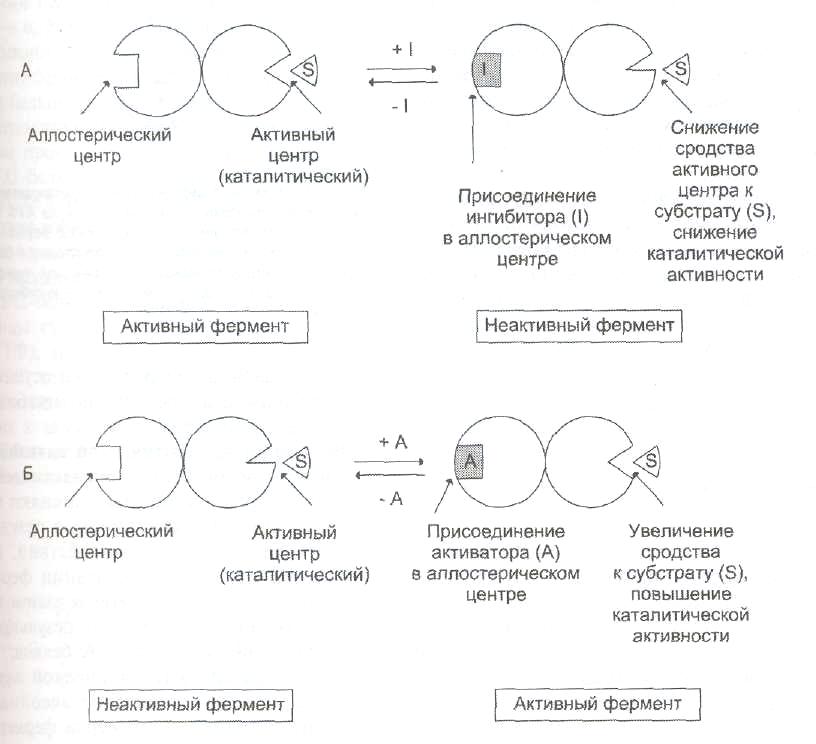
Особенности строения и функционирования аллостерических ферментов:
обычно это олигомерные белки, состоящие из нескольких протомеров или имеющие доменное строение;
они имеют аллостерический центр, пространственно удалённый от каталитического активного центра;
эффекторы присоединяются к ферменту нековалентно в аллостерических (регуляторных) центрах;
аллостерические центры, так же, как и каталитические, могут проявлять различную специфичность по отношению к лигандам: она может быть абсолютной и групповой. Некоторые ферменты имеют несколько аллостерических центров, одни из которых специфичны к активаторам, другие – к ингибиторам.
протомер, на котором находится аллостерический центр, – регуляторный протомер, в отличие от каталитического протомера, содержащего активный центр, в котором проходит химическая реакция; аллостерические ферменты обладают свойством кооперативности: взаимодействие аллостерического эффектора с аллостерическим центром вызывает последовательное кооперативное изменение конформации всех субъединиц, приводящее к изменению конформации активного центра и изменению сродства фермента к субстрату, что снижает или увеличивает каталитическую активность фермента.
регуляция аллостерических ферментов обратима: отсоединение эффектора от регуляторной субъединицы восстанавливает исходную каталитическую активность фермента;
аллостерические ферменты катализируют ключевые реакции данного метаболического пути.
Лаганд здесь – железосвязывающий белок.
в) Аллостерическое ингибирование:
№ 8 Ферменты глюко- и гексокиназа катализируют одинаковую реакцию. Напишите реакцию, протекающую под действием этих ферментов; укажите различие в активности, регуляции и локализации этих ферментов. Объясните биологическое значение наличия в организме двух ферментов катализирующих одинаковую реакцию.
Глюко-
и гексокиназа катализируют реакцию
фосфорилирования глюкозы.
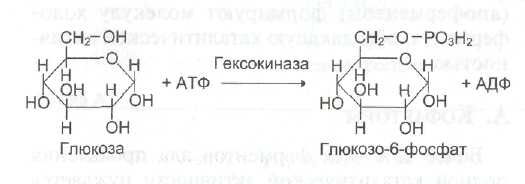
В превращениях в клетках глюкоза и другие моносахариды участвуют только в виде фосфорных эфиров. Фосфорилирование свободных моносахаридов – обязательная реакция на пути их использования, она приводит к образованию более реакционно-способных соединений и поэтому может рассматриваться как реакция активации.
Глюкоза, поступающая в клетки органов и тканей, сразу же подвергается фосфорилированию с использованием АТФ. Эту реакцию во многих тканях катализирует фермент гексокиназа, а в печени и поджелудочной железе – фермент глюкокиназа. Фосфорилирование глюкозы – практически необратимая реакция, так как она протекает с использованием значительного количества энергии. Образование глюкозо-6-фосфата в клетке – своеобразная «ловушка» для глюкозы, так как мембрана клетки непроницаема для фосфорилированной глюкозы (нет соответствующих транспортных белков). Кроме того, фосфорилирование уменьшает концентрацию свободной глюкозы в цитоплазме. В результате создаются благоприятные условия для облегчённой диффузии глюкозы в клетки из крови.
