
1. Цель работы
Изучить процесс кристаллизации на высохших каплях растворов солей и разрезах стальных слитков.
II. Краткие сведения из теории
Металлом называется вещество, обладающее металлическим блеском, высокой электро- и теплопроводностью, сочетанием высокой прочности и пластичности. Все эти свойства обусловлены атомным строением и типом связи между атомами металла. Особенностью строения металлов является то, что, все они построены из таких атомов, у которых внешние электроны слабо связаны с ядром. Энергия, необходимая для удаления электрона с последней оболочки, называется ионизационным потенциалом. Следовательно, металлы это такие элементы, которые обладают низким ионизационным потенциалом.
Теория металлического состояния рассматривает металл, как вещество, состоящее из положительно заряженных ионов, окруженных отрицательно заряженными частицами - электронами и принадлежащими не одному какому-либо атому, а всей совокупности атомов. Свободные электроны как бы создают электронный газ. Беспорядочное движение удерживает ионы в определенном порядке.
Между положительными ионами и свободным электронным газом возникают силы электростатического взаимопритяжения, которые и обусловливают металлический тип связи между атомами.
Все металлы и металлические сплавы являются телами кристаллическими. В кристаллических телах, в отличие от аморфных, атомы располагаются в строгом порядке, который определяет тип кристаллической решетки. Металлический тип связи обусловливает появление сил, удерживающих атомы (ионы) в узлах кристаллической решетки на определенном расстоянии друг от друга.
Свойства (физические, механические, химические и др.) металла зависят от кристаллографического направления. Анизотропия свойств является характерной особенностью любого монокристалла. Реальные же металлы и сплавы состоят не из одного монокристалла, а из большого числа кристаллов, различно ориентированных в пространстве. Такое тело называется поликристаллическим. Гомогенный кристалл поликристаллического тела, окруженный переходными зонами и отделенный ими от других кристаллов, называется зерном, а переходная зона - границей зерна. Множество случайно ориентированных зерен, образующих поликристаллическую структуру, имеют свойства одинаковые во всех направлениях.
Процесс кристаллизации
Каждое вещество может находиться в четырех агрегатных состояниях: твердом, жидком, газообразном и плазменном. В чистых металлах при определенных температурах происходит изменение агрегатного состояния: твердое сменяется жидким при температуре плавления, жидкое - газообразным при температуре кипения, газообразное - плазменным при температура ионизации вещества.
Переход от одного агрегатного состояния в другое называется фазовым превращением.
Переход жидкого металла в твердое состояние происходит при строго определенной температуре кристаллизации.
Первичной кристаллизацией называется процесс перехода из жидкого состояния в твердое с упорядочением атомов в пространстве. Форма, величина, а также направление кристаллов влияют на многие свойства металлов и сплавов. Поэтому изучение кристаллизации является весьма важным при исследовании сплавов.
Вторичной кристаллизацией называется перекристаллизация некоторых металлов и сплавов при нагреве и охлаждении. В основном это связано с явлением полиморфизма, т.е. с изменением у некоторых металлов типа кристаллической решетки в соответствии с температурой.
В природе все самопроизвольно (спонтанно) протекающие процессы, в том числе плавление и кристаллизация, образующие новое агрегатное состояние, обладают более устойчивыми связями и меньшим запасом свободной энергии.
Под свободной энергией F понимают ту часть внутренней энергии, которая может быть превращена в работу. С повышением температуры свободная энергия жидкого и твердого состояний уменьшается (рис.1).

Рис. 1. Схема изменения свободной энергии жидкого и твердого состояний металла в зависимости от температуры.
Однако она меняется различно для жидкого и твердого состояния. При температуре выше ТS, меньшей свободной энергией обладает вещество в жидком состоянии, ниже ТS, в твердом состоянии. Следовательно, вещество при Т > ТS должно находиться в жидком состоянии, а при Т < ТS - в твердом кристаллическом состоянии. Очевидно, что при температуре ТS свободная энергия жидкого и твердого вещества равна, металл одновременно может существовать в двух состояниях. Температура ТS называется равновесной или теоретической температурой кристаллизации. При ТS не может происходить процесс кристаллизации, так как Fж = Fкр. Для начала кристаллизации необходимо, чтобы этот процесс был термодинамически выгоден, т.е. необходимо создать такие условия, при которых свободная энергия твердой фазы будет меньше, чем свободная энергия жидкой фазы.
Как видно из рис. 2, это возможно только при некотором переохлаждении сплава.

Рис.2 Кривые охлаждения чистых металлов: 1 – теоретическая кривая; 2 – фактическая кривая.
Температура, при которой практически начинается кристаллизация, называется фактической температурой кристаллизации. Степенью переохлаждения Т называется разность между равновесной (теоретической) и фактической температурами кристаллизации
ТТs - Tкр,
где Тs - равновесная температура; Tкр - фактическая температура кристаллизации.
Для развития процесса плавления необходима некоторая степень перегрева сплава
Т Tпл - Тs
где Tпл - фактическая температура плавления.
Движущей силой любого превращения является разность свободных энергий
F = F старой фазы - F новой фазы.
Процесс кристаллизации изучается по кривым охлаждения (рис.2). Охлаждение металла в жидком состоянии сопровождается плавным понижением температуры (участок ав). Скорость охлаждения (наклон кривой) зависит от разности температур металла и охлаждающей среды. При достижении температуры кристаллизации на кривой появляется площадка (участок вс), так как отвод тепла компенсируется так называемой скрытой теплотой кристаллизации (эта та теплота, которую поглощала система при нагреве разрушая кристаллическую решетку).
По окончании кристаллизации (точка с), т.е. когда весь жидкий металл перейдет в кристаллическое твердое состояние, при охлаждении затвердевшего металла (участок cd) температура опять начнет снижаться.
Скорость процесса кристаллизации количественно определяют двумя величинами (параметрами кристаллизации): скоростью зарождения центров кристаллизации (ЧЦ в 1 см3 в сек.) и скоростью роста кристаллов (СК в мм/сек; мм/мин). Число центров кристаллизации и скорость их роста зависят от степени переохлаждения (рис.3). С увеличением степени переохлаждения возрастает число центров кристаллизации и увеличивается скорость их роста. При определенной степени переохлаждения наступает максимум. Однако металлы и сплавы, обладающие в жидком состоянии малой склонностью к переохлаждению, невозможно охладить до таких температур, при которых ЧЦ и СК достигли бы максимума перегиба.
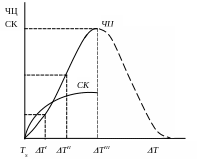
Рис.3. Кривые зависимости числа центров (ЧЦ) и скорости роста кристаллов (СК) от степени переохлаждения системы при кристаллизации.
Размер образующихся кристаллов зависит от соотношения величин ЧЦ и СК в процессе кристаллизации при данной степени переохлаждения. Для степени переохлаждения ΔТ΄ скорости образования центров кристаллизации и их роста малы, поэтому процесс кристаллизации протекает медленно и, в результате образования небольшого количества центров кристаллизации в единице объема, зерна получаются крупные. Для степени переохлаждения ∆Т″, значительно увеличились как скорость зарождения центров кристаллизации, так и скорость их роста, поэтому процесс кристаллизации при ∆Т″ будет протекать значительно быстрее, чем при ΔТ΄. При этом увеличивается число центров кристаллизации в единице объема. Зерна получаются мелкие.
В зависимости от условий кристаллизации могут возникнуть кристаллы различной формы: полиэдрические, пластинчатые, игольчатые, но наиболее распространенным является дендритный (древовидный) кристалл Чернова (рис.4). К дендритной форме кристаллизации наиболее склонны металлы с ГЦК решеткой.




Рис. 4. Дендритная кристаллизация:
а – схема дендрита; б – структура кристаллизации; в – общий вид дендрита.
Процесс кристаллизации реальных сплавов начинается у стенок изложницы, в местах, где жидкий металл охлаждается в первую очередь (т.е. имеет самую высокую степень переохлаждения Т), и последовательно продвигается к центру слитка. В результате кристаллизации слиток состоит из трех основных зон (рис.5).
Первая зона 1 - наружная мелкозернистая корка. Это зона мелких дезориентированных (беспорядочно направленных) кристаллов. Мелкие кристаллы получаются при большой степени переохлаждения, дезориентированные в результате того, что первичные кристаллы (оси первого порядка) растут перпендикулярно неровностям внутренней поверхности стенки изложницы. Растущие кристаллы сталкиваются между собой и образуют зону мелких дезориентированных зерен.
Вторая зона 2 - зона столбчатых кристаллов. После образования корки теплоотвод уменьшается (стенка изложницы прогрелась), уменьшается степень переохлаждения, неровности внутренней стенки изложницы сглаживаются. В результате из небольшого числа центров кристаллизации начинают расти столбчатые кристаллы. Рост этих кристаллов идет в направлении отвода тепла, и поскольку все кристаллы растут одновременно, то получаются вытянутые столбчатые кристаллы, рост которых продолжается до тех пор, пока имеется направленный отвод тепла. В случае сильного перегрева и быстрого охлаждения столбчатые кристаллы могут заполнить весь объем слитка.
1
2 3
.
б)
 ретья
зона 3
- зона крупных равноосных кристаллов.
В центре слитка уже отсутствует
определенная направленность отвода
тепла, температура почти уравновешивается.
Образующиеся зародыши разрастаются
по оси и ветвям в различных направлениях,
встречаясь друг с другом
в результате образуется равноосная
структура.
ретья
зона 3
- зона крупных равноосных кристаллов.
В центре слитка уже отсутствует
определенная направленность отвода
тепла, температура почти уравновешивается.
Образующиеся зародыши разрастаются
по оси и ветвям в различных направлениях,
встречаясь друг с другом
в результате образуется равноосная
структура.
В
Рис.
5.
Строение слитка спокойной стали:
а
– продольное сечение; б
– поперечное сечение;
1
– корковая зона мелких кристаллов,
2
– зона столбчатых кристаллов,
3
– зона крупных равноосных кристаллов,
4 – усадочная раковина, 5 – усадочная
рыхлость
Наблюдение за процессом кристаллизации, металлов и сплавов затруднено в связи с их непрозрачностью и высокой температурой кристаллизации. Поэтому изучение этих процессов осуществляется различными косвенными методами.
В настоящей работе изучаются процессы первичной кристаллизации насыщенных растворов различных солей, вызванные испарением растворителя.
Изучение процесса кристаллизации осуществляется с помощью бинокулярной лупы или биологического микроскопа.
Водные растворы солей приготавливаются насыщенными с тем расчетом, чтобы незначительное испарение воды привело растворы к состоянию перенасыщения.
При кристаллизации жидкого раствора любой соли, так же как и у стального слитка, можно наблюдать три различные зоны кристаллов, отличающиеся своей формой и величиной (рис. 6). Образование трех зон можно объяснить различными условиями, кристаллизации.

Рис.6.
Схема строения засохшей капли раствора:
1
– зона мелких равноосных кристаллов;
2
– зона крупных вытянутых (столбчатых)
кристаллов; 3
– зона крупных равноосных кристаллов
Обычно кристаллизация капли начинается у краев, так как здесь быстрее всего испаряется растворитель и раствор быстро перенасыщается. У краев капли возникает зона весьма мелких кристаллов (зона 1), что указывает на зарождение большого числа центров кристаллизации.
Значительное перенасыщение водного раствора соли можно уподобить значительному переохлаждению кристаллизующегося металла.
К мелкозернистой зоне примыкает зона более крупных столбчатых кристаллов (зона 2), направление роста которых обычно перпендикулярно краю капли.
Большой размер образующихся кристаллов указывает на уменьшение числа центров кристаллизации и увеличение скорости роста кристаллов. Направленный рост, обусловливающий столбчатую форму, вызван тем, что в связи с небольшим пересыщением жидкого раствора в более толстом слое капли центры кристаллизации, не связанные с ранее затвердевшей зоной у краев капли, не образуются, а центры, возникшие на границе мелкозернистой зоны, растут в сторону постепенно пересыщающихся краев, т.е. к центру капли.
Постепенное пересыщение слоев утолщающейся по направлению к центру капли создает условия кристаллизации, подобные направленному отводу тепла в формы или в изложницы для металла.
В центре капли возникает третья зона (зона 3) - состоящая из очень крупных, различно ориентированных равновесных кристаллов. Большой размер кристаллов указывает на малое число образующихся центров кристаллизации в связи с медленным пересыщением этой части капли, малая степень пересыщения, так же как и малая степень переохлаждения в центральной зоне слитка или отливки металла, создаст условие для зарождения наибольшего числа различно ориентированных равновесных кристаллов.
