
- •Раздел 2
- •Глава 11
- •11.1. Общая характеристика
- •11.2. Виды гравиметрических определений
- •11.3. Понятие о механизме образования осадка
- •11.4. Коллоидная стадия образования осадка
- •11.5. Причины загрязнения осадка и способы их устранения
- •11.6. Основные этапы методики гравиметрического определения методом осаждения
- •11.7. Гравиметрия в фармацевтическом анализе
- •Глава 12
- •12.1. Основные понятия титриметрии
- •12.2. Классификация титриметрических методов анализа и способов титрования
- •12.3. Стандартные растворы и стандартные вещества
- •12.4. Расчёты, связанные с приготовлением растворов титрантов и титрованием Расчёты, связанные с приготовлением растворов
- •Расчёты, связанные с титрованием
- •Глава 13
- •13.1. Титранты и стандартные вещества
- •13.2. Обнаружение конечной точки титрования. Кислотно-основные индикаторы
- •Метиловый красный
- •Тимолфталеин (бесцветный синий)
- •Феноловый красный
- •13.3. Кривые титрования
- •0,10 М раствором NaOh
- •Расчёты для построения кривой титрования
- •Расчёты для построения кривой титрования
- •0,10 М Na2co3 0,10 м раствором hCl
- •13.4. Факторы, влияющие на величину скачка титрования
- •13.5. Погрешности титрования
- •13.6. Некоторые случаи практического применения кислотно-основного титрования в водных растворах
- •Глава 14
- •14.1. Ограничения возможностей кислотно-основного основного титрования в водных растворах
- •14.2. Критерии выбора растворителя для кислотно-основного титрования
- •14.3. Применение в фармацевтическом анализе Титрование в кислотных растворителях
- •Глава 15
- •15.1. Общая характеристика
- •15.2. Меркуриметрическое титрование
- •15.3. Комплексонометрическое титрование
- •15.3.1. Понятие о комплексонах
- •15.3.2. Свойства этилендиаминтетрауксусной кислоты и её взаимодействие с катионами металлов
- •15.3.3. Кривые титрования
- •1,010-3 М раствором эдта при рН 9,50 в присутствии 510-2 м nh3
- •15.3.4. Способы обнаружения конечной точки титрования. Металлоиндикаторы
- •Пирокатехиновый фиолетовый – металлоиндикатор из группы сульфофталеиновых красителей. Представляет собой четырёхосновную кислоту. Комплексы с металлами обычно окрашены в синий цвет.
- •15.3.5. Индикаторные погрешности
- •15.3.6. Титранты и стандартные вещества
- •15.3.7. Способы комплексонометрического титрования и его применение
- •Глава 16
- •16.1. Общая характеристика
- •16.2. Аргентометрическое титрование
- •16.2.1. Кривые титрования
- •Расчёты для построения кривой титрования
- •16.2.2. Способы обнаружения конечной точки титрования
- •Метод Мора
- •Метод Фольгарда
- •Особенность определения хлоридов
- •Особенность определения иодидов
- •Метод Фаянса
- •16.2.3. Титранты и стандартные вещества
- •16.2.4. Применение в фармацевтическом анализе
- •16.3. Меркурометрическое титрование
- •Глава 17
- •17.1. Общая характеристика и классификация
- •17.2. Кривые титрования
- •17.3. Способы обнаружения конечной точки титрования. Окислительно-восстановительные индикаторы
- •Глава 18
- •18.1. Иодометрическое титрование
- •Титранты и стандартные вещества
- •Обнаружение конечной точки титрования
- •18.2. Хлориодометрическое титрование
- •18.3. Иодатометрическое титрование
- •18.4. Броматометрическое титрование
- •18.5. Нитритометрическое титрование
- •18.6. Перманганатометрическое титрование
- •18.8. Дихроматометрическое титрование
- •18.8. Цериметрическое титрование
15.3. Комплексонометрическое титрование
15.3.1. Понятие о комплексонах
Комплексонометрическим титрованием называется титриметрический метод анализа, основанный на образовании хелатов при взаимодействии катионов металлов с комплексонами.
Комплексоны – органические соединения, в молекулах которых содержится большое число оснόвных донорных центров и кислотных функциональных групп, расположенных так, что при их взаимодействии с катионами металлов образуются высокоустойчивые внутрикомплексные соединения, содержащие не менее двух циклов.
В качестве оснόвных донорных центров в молекулах комплексонов выступают атомы азота, фосфора или серы; кислотные центры обычно представлены карбоксильными или фосфоновыми группами. Например:
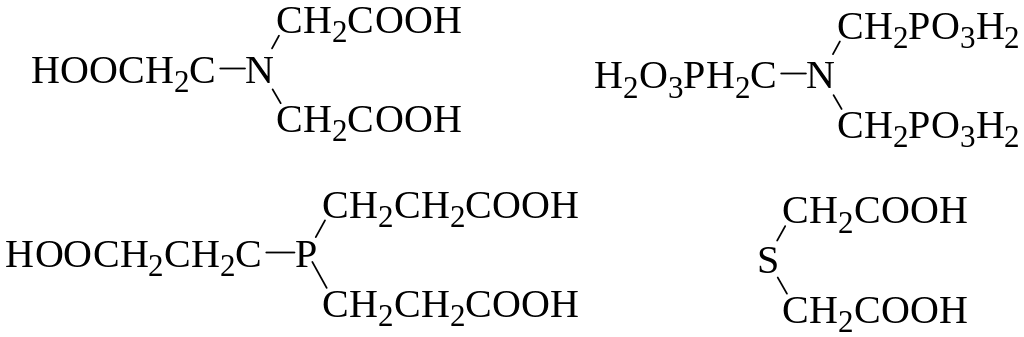
Максимально возможная дентатность у различных комплексонов может изменяться от 3 до 8:
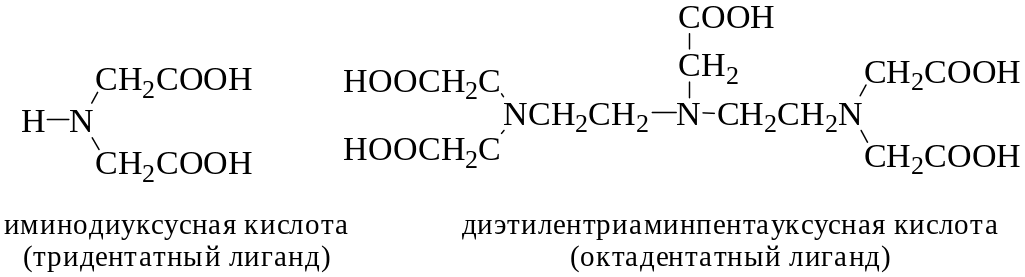
В титриметрии наибольшее значение имеют комплексоны, относящиеся к аминополикарбоновым кислотам: этилендиаминтетрауксусная кислота и её динатриевая соль.
15.3.2. Свойства этилендиаминтетрауксусной кислоты и её взаимодействие с катионами металлов
Этилендиаминтетрауксусная кислота (ЭДТА) представляет собой белое кристаллическое негигроскопичное вещество. Мало растворима в воде и этаноле. Растворимость ЭДТА в воде минимальна при рН 1,6 – 1,8 и увеличивается при уменьшении или увеличении рН.
ЭДТА (H6Y2+) является шестиосновной кислотой: pKa1 0,8; pKa2 1,6; pKa3 = 2,0; pKa4 = 2,67; pKa5 = 6,16; pKa6 = 10,26. Её нейтральная форма (H4Y) имеет цвиттер-ионную структуру.
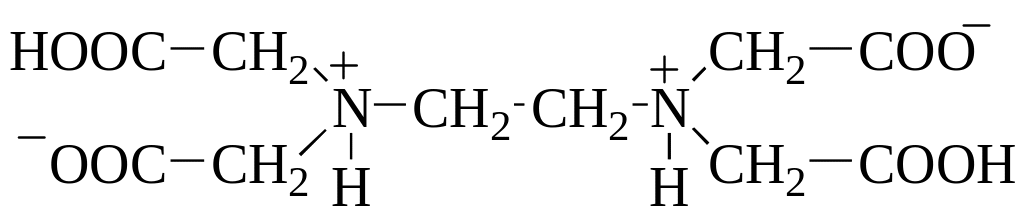
Отщепление первого и второго протонов у H4Y происходит от карбоксильных групп. У дианиона ЭДТА карбоксильные группы депротонированы, а атомы азота, наоборот, остаются протонированными. Третий и четвёртый протоны отщепляются от N-H кислотных центров. Анионы ЭДТА имеют сложное строение, так как протонизированные атомы водорода могут образовывать внутримолекулярные водородные связи –N-H…O, что приводит к формированию циклов.
На рис. 15.1 приведена зависимость состава водных растворов ЭДТА от рН.
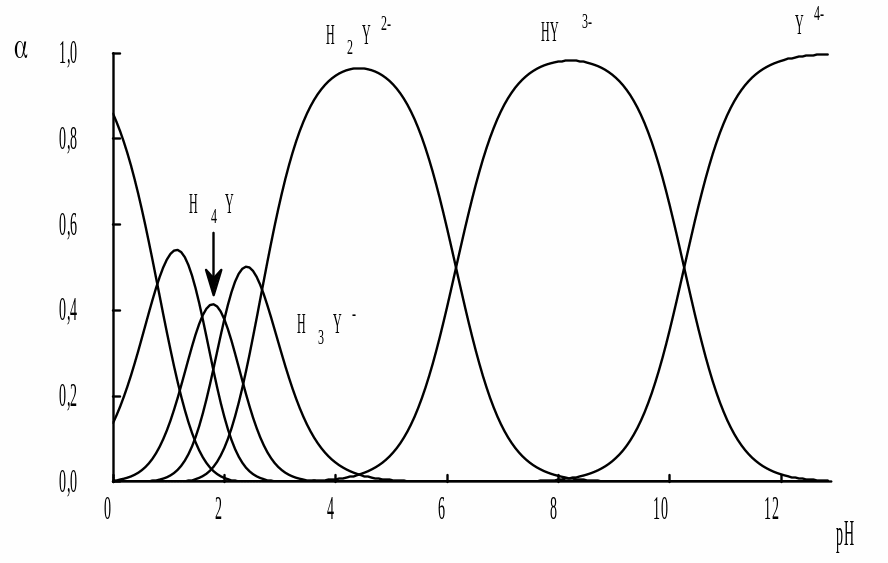
Рис. 15.1. Распределительная диаграмма для ЭДТА
При рН 3-6 в растворе доминирует анион H2Y2-, при рН 6-10 – HY3- а при рН > 10,5 – Y4-. В общем случае значение (Y4-) можно рассчитать:
![]()
По мере увеличения рН формула для расчёта (Y4-) будет упрощаться. Например, при рН > 8 можно принять, что
![]() или
или
![]()
ЭДТА образует комплексы с катионами большинства металлов
Mn+ + HmY(m-4)- [MY](n-4)+ + mH+
При рН 9 это уравнение будет выглядеть как
Mn+ + HY3- [MY](n-4)+ + H+
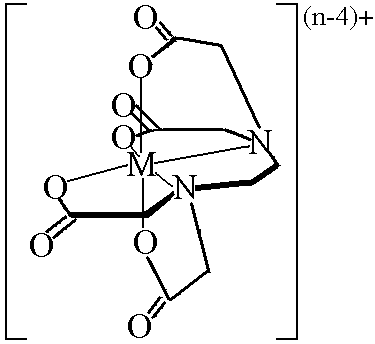
Рис.
15.2. Структура
комплекса металла с ЭДТА
На устойчивость комплексов катионов металлов с ЭДТА влияют вещества, взаимодействующие с катионами металла либо с анионом Y4-.

Практически устойчивость комплексов катионов металлов с ЭДТА удобно описывать с помощью условных констант образования, которые могут быть использованы лишь при тех условиях (рН, концентрация постороннего лиганда), для которых они рассчитаны.
![]()
