
- •Зырянова, л. Н. Круглова
- •Часть 1 омск 2003
- •Часть 1
- •Содержание Введение….................................................................................................................5
- •1.2. Раздел 2. Взаимодействие веществ...................................................................6
- •Введение
- •1.2. Раздел 2. Взаимодействие веществ
- •1.3. Перечень лабораторных работ
- •1.4. Темы семинарских занятий
- •2. Основные теоретические положения и условные обозначения
- •2.1. Основные теоретические положения
- •2.2. Условные обозначения
- •3. Примеры решения задач и
- •0,3 (Моль).
- •1 Моль (64 г) Cu взаимодействует с 2 моль (44,8 л) no2;
- •4. Контрольные задания
- •5. Дополнительные задания
- •6. Программированные задания
- •6.1. Пример оформления программированного задания 1 Программированное задание 1
- •0,30 (Моль);
- •0,1 (Моль).
- •0,1 (Моль).
- •2 (Моль/л).
- •6.2. Программированное задание 1
- •6.3. Программированное задание 2
- •6.4. Свойства неорганических веществ. "Цепочки" превращений
- •7. Задачи повышенной сложности
- •Основные понятия и законы химии
- •Часть 1
- •Лицензия ид № 01094 от 28.02.02.
- •6 44046, Г. Омск, пр. Маркса, 35
- •Особенности взаимодействия кислот с металлами
- •Вещества
- •Простые Сложные
- •Генетическая связь неорганических веществ
- •Периодическая система элементов д. И. Менделеева
Вещества

Простые Сложные



Металлы Неметаллы Оксиды Основания Соли
K ,
Fe, Cu,
,
Fe, Cu,
M
 g,
Al, Zn
g,
Al, Zn
Раствори- Нераство- Средние Кис-
Солеобра- Несолеоб- мые в воде римые в лые
 зующие
разующие (щелочи)
воде Основные
зующие
разующие (щелочи)
воде Основные

Основные Кислотные Кислоты
Амфотерные
Кислород- Бескислородные
Содержащие
Генетическая связь неорганических веществ
М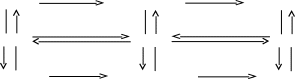 еталл
Оксид металла
Основание
еталл
Оксид металла
Основание
Соль Соль Соль
Неметалл Окисд неметалла Кислота
Н
2
4
 Са
СаО
Са(ОН)2
Са
СаО
Са(ОН)2
Соль Соль Соль
7
6
 Р
Р2О5
Н3РО4
Р
Р2О5
Н3РО4
1. 3Са + 2Р = Са3Р2
2. 2Са + О2 = 2СаО
3. 3СаО + Р2О5 = Са3(РО4)2
4. СаО + Н2О = Са(ОН)2
5. 3Са(ОН)2 + 2Н3РО4 = Са3(РО4)2 + 6Н2О
6. 4Р + 5О2 = 2Р2О5
7. Р2О5 + 3Н2О = 2Н3РО4
Приложение 3
