
Болезни, связанные с нарушением деградации коллагена
увеличенная активность коллагеназы обнаружена в суставах при ревматоидном артрите, в тканях ротовой полости при периодонтите, при ряде кожных заболеваний, язвенных кератитах. Коллагенолитическая активность увеличивается при воспалении, в опухолях, в заживающих ранах.
Недостаточность активности коллагеназы отмечается при циррозе печени, склеродермии, легочном фиброзе и др.
Биохимические маркеры синтеза коллагена
Производные коллагена N и С-пропептиды
Пролил- и лизилгидроксилаза
Фибронектин
Щелочная фосфатаза (костный изофермент)
Биохимические маркеры распада коллагена
Производные коллагена N и С-пропептиды
Гидроксипролин
Пиридинолин
ГАГ
ГГЛ (галактозил-гидроксилизин)
ГГГЛ (глюкозил-ГГЛ)
Коллагеназа, эластаза
Кислая фосфатаза
ЭЛАСТИН – второй главный белок соединительной ткани.
Различия с коллагеном. В свойствах. Эластин в отличие от коллагена не образует при кипячении желатину. В локализации. Коллаген – главный белок белой соединительной ткани, а эластин – жёлтой. Эластин преобладает в эластичных структурах (стенки больших кровеносных сосудов…), а в образовании рубцов, наоборот, участвует коллаген.
Аминокислотный состав тоже отличается от коллагена: хотя много глицина и пролина, отсутствуют гидроксипролин и гидроксилизин. Эластин особенно богат нейтральными алифатическими аминокислотами (вал, лей и иле, ала), а полярных заряженных аминокислот (глу, арг) мало.
Строение. Волокна эластина построены из относительно небольших почти сферических молекул, соединенных в волокнистые тяжи с помощью жестких поперечных сшивок. Всего имеется 2 основных формы поперечных сшивок, обе с участием лизина.
1). Из четырех остатков лизина образуются: десмозин и изодесмозин.
Структура их довольно необычна: четыре остатка лизина, соединяясь боковыми радикалами, образуют замещенное пиридиновое кольцо. Считают, что при образовании десмозина сначала три остатка лизина окисляются лизилоксидазой до ε-альдегидов (аллизин), а затем соединяются с четвертым остатком лизина.
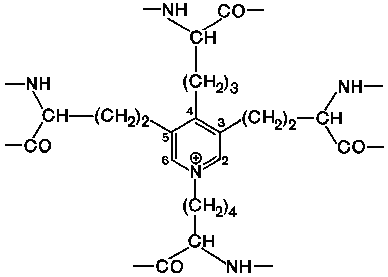
Эти остатки лизина находятся на двух соседних цепях или принадлежат трём или четырём разным цепям. Этим можно объяснить, что эластин в отличие от других фибриллярных белков способен растягиваться в двух направлениях. Поперечные сшивки очень прочные, так что даже кислота не может их гидролизовать.
2). Второй тип поперечных сшивок в эластине образуется лизин-норлейцином
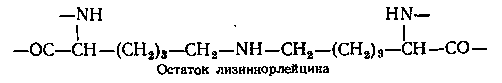
Синтез. Эластин вместе с коллагеном, гликопротеинами и протеогликанами синтезируют фибробласты. Экспрессия гена эластина регулируется витамином С. Непосредственный продукт синтеза – предшественник эластина тропоэластин (в коллагене — проколлаген). Тропоэластин не содержит поперечных связей, он растворим. В последующем тропоэластин превращается в зрелый нерастворимый эластин, содержащий большое количество поперечных связей. Десмозин, изодесмозин и лизиннорлейцин не исчерпывают список соединений, образующих поперечные связи в молекуле эластина.
Катаболизм. В ЖКТ. Нити эластина не перевариваются трипсином или химотрипсином, небольшое действие оказывает пепсин. Поджелудочная железа производит проэластазу, которая под влиянием трипсина превращается в эластазу. Этот фермент гидролизует эластин в мясе, которое потребляется в пищу.
В тканях. Тканевой эластин также может подвергаться деградации эластазой, происходящей из нейтрофилов и макрофагов. Лейкоцитарная эластаза не отличается особой специфичностью и расщепляет также протеогликаны и гликопротеины.
Отличительные признаки коллагена и эластина
Коллаген |
Эластин |
Несколько генетических типов |
Один генетический тип |
Тройная спираль |
Не образует тройной спирали |
(Гли-X-Y)n повторы в структуре |
Нет повторов (Гли-X-Y) |
Имеется гидроксипролин |
Нет гидроксипролина |
Гликозилирован по гидроксилизину |
Нет гидроксилизина и соответствующего гликозилирования |
Внутримолекулярные альдольные поперечные связи |
Поперечные связи в форме десмозина |
Во время синтеза образуются дополнительные пептиды |
Дополнительных пептидов не образуется |
Расщепляется коллагеназой |
Расщепляется эластазой |
