
- •Оглавление
- •Введение
- •Общие указания и рекомендации к составлению отчета и выполнению лабораторной работы
- •1. Определение теплового эффекта образования
- •1.1. Цель работы
- •1.2. Общие указания
- •1.3. Реактивы и оборудование
- •1.4. Методика эксперимента
- •1.5. Обработка экспериментальных данных
- •1.2. Расчеты
- •1.6. Контрольное задание
- •1.7. Вопросы
- •2.3. Реактивы и оборудование
- •2.4. Методика эксперимента
- •1.5. Обработка экспериментальных данных
- •2.6. Контрольное задание
- •2.7. Вопросы
- •3. Обратимые процессы и
- •3.1. Цель работы
- •3.2. Общие указания
- •3.3. Реактивы и оборудование
- •3.4. Методика эксперимента
- •3.5. Сделайте выводы по работе
- •3.6. Контрольное задание
- •3.7. Вопросы
- •4. Буферные растворы
- •4.1. Цель работы
- •4.2. Общие указания
- •4.3. Реактивы и оборудование
- •4.4. Методика эксперимента
- •Форма таблицы для записи результатов измерений
- •Опыт 3. Буферирование раствора при разбавлении
- •4.5. Обсуждение результатов экспериментов.
- •4.6. Контрольное задание
- •5. Электрохимические процессы
- •5.1. Цель работы
- •5.2. Общие указания
- •5.3. Реактивы и оборудование
- •5.4. Методика эксперимента
- •5.4.1. Гальванические цепи
- •5.4.2. Обработка экспериментальных данных
- •5.4.3. Электролиз
- •5.4.4. Коррозия металлов
- •2. Указания по технике эксперимента
- •6.3. Реактивы и оборудование
- •6.4. Методика эксперимента
- •6.4.1. Метод стандартных добавок
- •Подготовка измерительной цепи
- •Техника титрования
- •6.4.2. Обработка экспериментальных данных
- •6.4.3. Техника работы и обработки экспериментальных данных по методу градуировочного графика
- •6.5. Обсуждение полученных результатов.
- •6.6. Контрольное задание
- •7. Мембранные процессы
- •7.1. Цель работы
- •7.2. Общие указания
- •7.3. Реактивы и оборудование
- •7.4. Методика эксперимента
- •7.4.2. Электродиализ золя гидроксида железа
- •7.5. Контрольные вопросы
- •8. Криоскопия
- •8.2. Общие указания
- •8.3. Реактивы и оборудование
- •8.3. Методика эксперимента
- •8.4. Обработка экспериментальных данных
- •8.5. Контрольное задание
- •Вопросы
- •9. Получение золей и их обнаружение
- •9.1. Цель работы Получить дисперсные системы (золи, гели) методами химической конденсации и пептизации и выполнить исследования в соответствии с указаниями к конкретным опытам.
- •9.2. Общие указания
- •9.3. Реактивы и оборудование
- •9.4. Методика эксперимента
- •9.4.1. Конденсационные методы.
- •Опыт 4. Получение дисперсных систем на основе реакции обмена
- •Целью опыта является изучить влияние концентраций исходных веществ на характер дисперсных систем, получаемых при химической конденсации.
- •9.4.2. Диспергирование пептизацией
- •9.4.3. Образование мицелл лиофильного золя
- •9.4.4. Обсуждение результатов опытов.
- •9.5. Сделайте выводы по работе в целом
- •9.6. Контрольное задание
- •9.7. Вопросы
- •10. Коагуляция и коллоидная защита золей
- •2.1. Цель работы
- •10.2. Общие указания
- •1. Подготовьте краткую теорию к отчету в соответствии с планом:
- •2. Сущность коагуляции.
- •10.3. Реактивы и оборудование
- •10.4. Методика эксперимента
- •10.5. Контрольное задание
- •10.6. Вопросы
- •11. Физико-химические свойства желатинового геля
- •11.1. Цель работы
- •11.2. Общие указания
- •11.3. Реактивы и оборудование
- •11.4. Методика эксперимента
- •Опыт 2. Синерезис желатинового геля.
- •11.5. Контрольное задание
- •11.6. Вопросы
- •12. Растворы вмс
- •12.1. Цель работы
- •12.2.Общие указания
- •12.3. Реактивы и оборудование
- •12.4. Методика эксперимента
- •1. Приготовление рабочих растворов
- •2. Измерение вязкости растворов.
- •12.5. Контрольное задание
- •12.6. Вопросы
- •13. Адсорбция из растворов
- •13.1. Цель работы
- •13.2. Общие указания к работе
- •13.3. Методика эксперимента
- •13.5. Контрольное задание
- •13.6. Вопросы
- •Использованная при подготовке сборника
- •Рекомендуемая для самоподготовки
- •Указания к выполнению графика прямой
- •Инструкция по работе с капиллярным вискозиметром впж - 4.
- •Инструкция по работе на рН - метре.
- •Подготовка к работе термометра Бекмана
7.3. Реактивы и оборудование
Электродиализатор, блок питания электродиализатора, желтая кровяная соль (K4[Fe(CN)6]) кристаллы, марганца хлорид (MnCL2)- кристаллы, магния хлорид (MgCl2)-кристаллы, меди сульфат пятиводный (CuSO45Н2О), меди сульфат, водный раствор 5 % , силикатный клей, разбавленный водой в соотношении 1:5, золь гидроксида железа1.
7.4. Методика эксперимента
7.4.1. Гетерогенные солевые системы
Опыт 1. Получение “искусственной клетки” в системе: раствор CuSO4 + кристаллы K4[Fe(CN)6].
Поместите в стеклянную пробирку несколько крупных кристалликов желтой кровяной соли. Сюда же прилейте примерно 10 см3 5% - ного раствора сульфата меди. Наблюдайте появление в пробирке образований причудливой формы. Опишите и объясните причины этого явления.
Опыт 2. Рост древовидных образований в системах на основе силикатного клея и кристаллов неорганических веществ.
В каждую из трех пробирок прилейте примерно по 10 см3 разбавленного водой примерно в 5 раз силикатного клея. Затем в разные пробирки бросьте по несколько наиболее крупных кристаллов одной из ниже приведенных солей: CuSO4·5Н2О, MnCl2 и MgCl2.
Наблюдайте появление и рост в пробирках “древовидных” образований различной толщины. Опишите эти образования и объясните причины наблюдаемого явления.
7.4.2. Электродиализ золя гидроксида железа
Подготовка электродиализатора.
На рисунке 7.1 приведена схема использованного в настоящей работе электродиализатора.
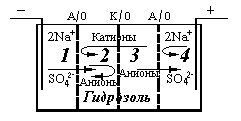
Рис. 7.1. Электродиализатор с камерами: 1- катодной; 2- концентрирования; 3- обессоливания; 4 - анодной.
Изогнутыми стрелками показан запрет на транспорт ионов через мембрану.
Изучите инструкцию по работе со стабилизированным источником питания и после этого подключите к нему электродиализатор в соответствии с полярностями, показанными на рисунке 7.1.
В электродные камеры ячейки для электродиализа залейте 0,1 М раствор сульфата натрия. В камеры обессоливания (3) и концентрирования (2) прилейте золь гидроксида железа. Можно использовать золь, оставшийся от предыдущей работы или получить свежий золь по методике, описанной в работе “Получение и обнаружение золей”. Объем золя можно взять произвольный. Проследите, чтобы расположенные на дне электродиализатора пробки были плотно подогнаны внутри отверстий для слива жидкостей.
Методика измерений
Внимание! Электродиализ выполняйте при стабилизированном напряжении в диапазоне 10 -20 В согласно рекомендациям преподавателя.
Подайте на электроды напряжение от источника питания, измерьте его величину и силу тока в цепи.
Измерьте силу тока через промежутки времени, указанные в таблице 7.1. Наблюдайте за состоянием золя в камерах электродиализатора. Когда золь разложится, процесс прекратите. После измерения конечных значений напряжения и силы тока, выключите прибор и демонтируйте установку. Слейте раствор сульфата натрия из электродных камер в ту же емкость, в которой он хранился. Содержимое из камер обессоливания и концентрирования слейте в отдельные стаканчики и опишите его. Показания прибора и характер наблюдаемых эффектов записывайте в таблицу по форме:
Таблица 7.1.
Таблица для записи результатов измерений и наблюдений.
Время (от начала опыта), мин |
Напряжение, В |
Сила тока, А |
Наблюдаемый эффект |
Начало |
|
|
|
10 |
|
|
|
20 |
|
|
|
40 |
|
|
|
Окончание |
|
|
|
Обсуждение результатов эксперимента.
Придерживайтесь следующего плана обсуждения результатов опыта.
1. Причины изменения силы тока в процессе электродиализа.
2. Строение двойного электрического слоя на мицелле гидрозоля железа и предполагаемый механизм разрушения этого золя.
3. Связь характера изменения силы тока с теоретическими представлениями о причинах разрушения золей в условиях электродиализа?
4. Выводы
