
- •Химия как раздел естествознания и ее роль в современном обществе.
- •Строение атома
- •Экспериментальные доказательства сложности строения атома
- •Электрон
- •Радиоактивность и строение ядер атома
- •Радиоактивные и стабильные изотопы Изотопы.
- •Модели строения атома. Планетарная модель атома
- •Строение атома водорода по Бору
Экспериментальные доказательства сложности строения атома
В конце XIX - начала XX в. были открыты явления, которые можно было интерпретировать только исходя из представлений о сложности строения атома.
Электрон
В самом начале XIX в. рядом ученых, в том числе русским физиком В. В. Петровым, были проведены исследования прохождения электрического тока через растворы химических соединений — электролитов, сопровождающегося электролизом этих соединений. Количественные были открыты М. Фарадеем, который показал, что для электролитического выделения одного грамм-эквивалента любого элемента, т.е. равного атомной массе, деленной на число принятых или отданных электронов, нужно пропустить через раствор одинаковое количество электричества, а именно — 96 500 кулонов (т. е. 2,9-1014 абсолютных электростатических единиц электричества).
m=k I t
Открытое Фарадеем соответствие вполне определенного количества электричества одному грамм-эквиваленту любого элемента является однозначным доказательством существования «атомов электричества», связанных с атомами вещества и их составными частями. Такой вывод был сделан, однако, долгое время в науке продолжали господствовать представления об электрических жидкостях — отрицательной и положительной.
В 1881 г. Г. Гельмгольц высказал идею об «атомном» строении электричества. Однако и после этого долго оставалось неизвестным, что именно представляют собой «атомы электричества», т. е. определенные порции электрического заряда, носителями которых являются мельчайшие частицы вещества, каков знак и величина их заряда, какова масса носителей этого заряда.
В 1891г. Стони ввел термин “электрон”, для обозначения наименьшей корпускулы электричества , хотя сам электрон к этому времени еще не был обнаружен экспериментально.
В опытах по прохождению электрического тока через газы, выполненными в 80-90-х годах XIX в., использовались откачанные до стотысячных долей атмосферного давления стеклянные трубки, внутри которых были впаяны металлические электроды. На один из электродов — катод — подавался отрицательный потенциал, на другой — анод — положительный. При этом наблюдалось свечение стекла, расположенного против катода. Это свечение вызывалось потоком лучей, идущих от катода и названных поэтому катодными лучами.
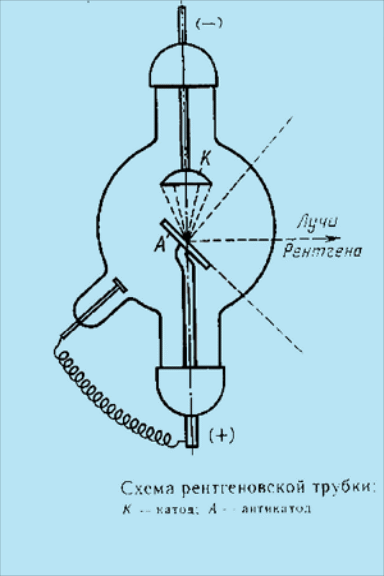
Катодные лучи распространяются прямолинейно — перпендикулярно к катоду, независимо от положения анода и, попадая на стекло, вызывают яркое свечение — флуоресценцию. В опытах Дж. Дж. Томсона и его сотрудников исследовалось поведение катодных лучей в электрическом и магнитном полях. Было обнаружено, что при пропускании катодных лучей между обкладками конденсатора поток лучей отклонялся по направлению от отрицательной обкладки к положительной .
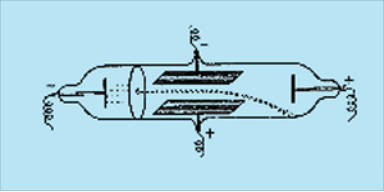
Отклонение катодных лучей в электрическом поле
Из этого факта следовал вывод, что катодные лучи обладая отрицательным зарядом, отталкиваются отрицательной обкладкой и притягиваются положительной.
Отклонение катодных лучей от первоначального направления наблюдалось и при пропускании их между полюсами магнита, т. е. в магнитом поле.
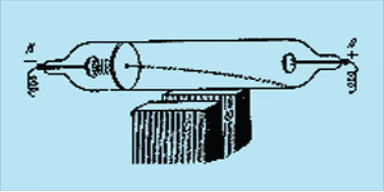
Отклонение катодных лучей в магнитном поле
До опытов Томсона было известно , согласно которому, если расставить большой, указательный и средний пальцы левой руки в трех перпендикулярных направлениях и направить указательный палец (по направлению силовых линий магнитного поля) от северного магнитного полюса к южному, а средний палец — по направлению тока, то большой палец покажет направление силы, действующей на проводник в магнитном поле. Правило левой руки было установлено до опытов, доказавших отрицательность «атомов электричества», и за направление тока в этом правиле (как и вообще вплоть до наших дней в электротехнике) условно принято направление движения положительных зарядов.
Опыт показал, что катодные лучи обладают отрицательным электрическим зарядом.
Радиус кривизны траектории движения катодных лучей зависит от массы летящих частиц т, их заряда е и скорости v.
В электрическом поле с напряженностью Е радиус кривизны определяется соотношением:
![]()
В магнитном поле с напряженностью Н радиус кривизны равняется
![]() (с
— скорость
света).
(с
— скорость
света).
Если действия двух полей компенсируют друг друга, то, очевидно,
![]()
тогда, зная Е и Н, можно определить отношение заряда частиц, образующих катодные лучи, к их массе:
![]()
Эксперименты показали, что это отношение постоянно для всех катодных частиц, независимо от материала катода и вида газа, заполнявшего разрядную трубку, и равно
![]()
Исследование катодных лучей показало, что они являются потоком частиц с массой 9.10910-31 кг и с минимально возможным отрицательным зарядом 1.60210-19 Кл. Таким образом, было доказано, что «атомы электричества» несут отрицательный заряд и являются составной частью всех атомов. Эти отрицательные «атомы электричества» были названы .
С открытием электронов стало ясно, что переносчиками заряда при прохождении тока через растворы электролитов являются атомы или группы атомов с недостатком или с избытком электронов— положительные и отрицательные ионы.
В начале XX в., на основании исследований броуновского движения, было определено число молекул в грамм-молекуле любого вещества — так называемое число Авогадро, равное
![]()
Зная это число, можно определить и величину заряда электрона. В самом деле, как показал Фарадей, одному грамм-эквиваленту любого элемента отвечает количество электричества, равное 96500 кулонов, или 2,91014 CGSE. Поскольку число атомов в грамм-атоме равняется 6,021023, ясно, что величина элементарного заряда (электрона или одновалентного иона) есть
![]()
В 1911 г. заряд электрона был определен прямым путем.
Поскольку для электронов было установлено соотношение заряда и массы. Очевидно, что теперь легко можно определить и массу электрона:
![]()
Эта масса примерно в 1840 раз меньше массы самого легкого атома — водорода.
