
- •1. Актуальность темы.
- •1. Конкретные цели:
- •2.Базовий уровень подготовки.
- •4. Задание для самостоятельного труда во время подготовки к занятию.
- •4.1 Перечень основных сроков, параметров, характеристик, которые должен
- •4.2.1 Теоретические вопросы к занятию
- •4.2.2 Практическая работа (задание), которая выполняется в письменном виде при подготовке к занятию
- •4.3 Практические работы (задания), которые выполняются на занятии
- •5.Организация содержания учебного материала.
- •Антигени
- •Мікроорганізми
- •Активація тригерних систем:
- •6. Задание для самоконтроля.
I
Антигенни
МикроорганизмиАнтигени
Мікроорганізми


Первичное Распознавание
и иммунный
ответ
Повреждение ГБМ
Нарушение функции Т-супрессоров
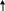
Генерация Т-лимфоцитов ефекторів
иммунные комплексы
Активация В-лимфоцитов
Циркулирующие
Локальные
Аутоантитела к ГБМ
I комплемента кінінової гемокоагуляції ренін-ангіотензин виділення
медиаторів(ПГ, ТхА2, ТхВ2, С4, IL-2
та інші) вільні радикали(О2,
ОН, ОН+ та інші)Активація тригерних систем:
 I
I
Активация тригерных систем: комплемента кининовой гемокоагуляции ренин-ангиотензин выделения
медиаторов(ПГ, ТхА2, ТхВ2, С4, IL-2
и др) свободные радикалы(О2,
ОН, ОН+ и др)

Разные клинико-морфологические формы
гломерулонефрита

Рис.1. Основные патогенетические механизмы развития ГН
КЛАССИФИКАЦИЯ И КЛИНИКА
Форма ГН |
Активность процесса |
Состояние функции почек |
Острый ГН: -с нефритическим синдромом -с нефротическим синдромом -с изолированным мочевым синдромом
-с нефротическим синдромом, гематурией и гипертензией
Хронический ГН: -нефротическая форма -гематурическая форма -смешанная форма
Подострый (злокачественный) ГН |
Период начальных проявлений Период разгара Период обратного развития
Переход в хронический ГН Период обострения
Период частичной ремиссии Период полной клинико-лабораторной ремиссии |
Без нарушения С нарушением Острая почечная недостаточность
Без нарушения С нарушением Хроническая почечная недостаточность (ХПН) С нарушением ХПН
|
Начальный период заболевания (через 7-14 дней после перенесенной инфекции) характеризуется симптомами интоксикации. На фоне нарушенного общего состояния (слабость, повышение температуры тела, головная боль, тошнота, рвота) появляются изменения цвета мочи, пастозность, отеки, боль в пояснице; в некоторых случаях – судороги, снижение остроты зрения, гипертензия. В периоде разгара ГН (2- 4 недели) симптомы становятся выраженнее. Период обратного развития длится 2 –3 месяца. Клинический диагноз хронического ГН устанавливают через 1 год после начала заболевания при сохранении активности процесса.
При нефритичному синдроме клиническая симптоматика состоит из незначительных отеков (преимущественно на лице), гипертензии и мочевого синдрома по гематуричним типу (еритроцитурія или гематурия, протеінурія до 1,5-2,0 грамма на сутки).
Под нефротическим синдромом понимают наличие: распространенных отеков (лицо, крестец, конечности, внешние половые органы, возможна анасарка); массивной протеинурии (более 2,5 грамма в сутки); гипопротеинемии (менее 55г\ л) с гипоальбуминемией (менее 25 г\ л), гипер-альфа2-глобулинемии; гиперхолестеринемии (более 5,72 ммоль\ л) и гиперлипидемии (более 7ммоль\ л).
Изолированный мочевой синдром диагностируется по наличию эритроцитурии (гематурии), протеинурии (до 1,5 грамма в сутки), цилиндрурии и возможной лейкоцитурии.
При сочетании нефротического синдрома (возможно, неполного), гипертензии и гематурии устанавливают диагноз острого ГН с нефротическим синдромом, гипертензией и гематурией.
Нефротическая форма хронического ГН по клинико- лабораторным признакам является эквивалентом нефротического синдрома острого ГН и характеризуется длительным волнообразным, непрерывно рецидивирующим или латентным течением с развитием склеротических и фибропластических изменений в почечной ткани.
Гематурическая форма хронического ГН по клинике является аналогом изолированного мочевого синдрома острого ГН и проявляется стойкой эритроцитурией (гематурией), возможной протеинурией (0,5- 1,0 грамм в сутки), длительно сохраняющейся функцией почек, недостаточной эффективностью лечения.
При смешанной форме заболевания наблюдается нефротический синдром с выраженными отеками и неселективной протеинурией, гипертензия, гематурия и быстро нарастающая почечная недостаточность.
Период обострения хронического ГН характеризуется наивысшей активностью процесса и развернутой клинико-лабораторной симптоматикой. В период частичной ремиссии исчезают клинические проявления заболевания, улучшаются лабораторные показатели и функция почек. Отсутствие клинических и лабораторных симптомов заболевания свидетельствует о периоде полной клинико-лабораторной ремиссии. Сохранение этой ремиссии в течение 5 лет означает выздоровление ребенка.
Подострые ГН имеют манифестное начало, быстропрогрессирующее злокачественное течение, нечувствительность к обычной терапии, летальный исход через 6- 18 месяцев в большинстве случаев.
В зависимости от состояния почек острый и хронический ГН могут протекать без нарушения или с нарушением их функции (снижение клубочковой фильтрации по клиренсу эндогенного креатинина). Иногда острый ГН может сопровождаться развитием острой почечной недостаточности, а хронический ГН – хронической почечной недостаточности (декомпенсованные нарушения фильтрации и канальцевых функций).
Циклическое течение ГН констатируют при наличии острого начала, развернутой клиники, обратного развития заболевания с клинико-лабораторным выздоровлением.
ОСТРЫЙ ПОСТСТРЕПТОКОККОВЫЙ ГЛОМЕРУЛОНЕФРИТ (ОПСГН)
ОПСГН – заболевание, которое имеет в своей основе иммунно-воспалительное поражение почек (преимущественно клубочков), циклическое течение и клинически проявляется нефротическим синдромом. ОПСГН встречается чаще у детей 5-12 лет.
ЭТИОПАТОГЕНЕЗ. Началу заболевания за 1-3 недели предшествует стрептококковая инфекция в виде фарингита, тонзиллита, скарлатины, пиодермии. ОПСГН вызывают преимущественно “нефритогенные” штаммы b-гемолитического стрептококка группы А, которые имеют М12, 18, 25, 49, 55, 57, 60, Т14 антигены. Допускают, что переохлаждение, респираторная вирусная инфекция у ребенка с хроническим тонзиллитом или носительство кожного нефритогенного стрептококка А может привести к активации инфекции и обусловить возникновение ОПСГН.
Ведущим патогенетическим механизмом при ОПСГН считают образование в крови или в почках иммунных комплексов ( 111 тип аллергической реакции), где антигеном является преимущественно эндострептолизин нефритогенных стрептококков А. С начала заболевания в сыворотке крови можно наблюдать повышенный уровень иммунных комплексов (ИК) и низкий уровень С3 комплемента, а также увеличение титра антител к стрептолизину-О, никотинамидадениннуклеотидазы или дезоксирибонуклеазы. ИК активизируют систему комплемента, который приводит к поражению эндотелия капилляров клубочков. Поражение эндотелия и тромбоцитов провоцируют активацию системы гемостаза и развитие локального внутрисосудистого свертывания крови, микротромбозов в капиллярах клубочков. Одновременно происходит процесс тромболизиса. Гистологически ОПСГН представляет собой эксудативно-пролиферативный эндокапиллярный ГН с пролиферацией эндотелиальных и мезангиальных клеток. Через 1,5-2 месяца гранулярные депозиты из IGG и комплемента С3, характерные для начала заболевания, могут исчезать при типичном течении болезни. Прогностически неблагоприятными при ОПСГН являются экстракапиллярные “полумесяцы” в капсуле Боумена – Шумлянского. Снижение клеточного иммунитета, дисбаланс в субпопуляциях Т-лимфоидных клеток играет существенную роль в достоверности трансформации ОПСГН в хронический нефрит.
КЛИНИКА. В типичных случаях ОПСГН начинается через 10-21 день после стрептококкового заболевания с ухудшения общего состояния, потемнения мочи, олигурии, отеков и артериальной гипертензии. Появляются головная боль (за счет гипертензии, повышения внутричерепного давления), тошнота, рвота, слабость, бледность кожи (связано с ангиоспазмом), возможно непродолжительное повышение температуры тела, боль в пояснице (обусловленная растяжением капсулы в результате отека паренхимы почек и сжатием нервно- сосудистых окончаний). Существенная артериальная гипертензия отмечается более, чем у половины детей. Она связана с активацией ренин-ангиотензин-альдостероновой системы и вазоконстрикцией. Отеки отмечаются в 80-90 % больных, возникают утром, преимущественно на лице, вокруг глаз; в дальнейшем могут распространяться на туловище и конечности. Среди причин их развития: снижение клубочковой фильтрации, гиперальдостеронизм с повышением реабсорбции натрия и увеличением секреции антидиуретического гормона и задержкой жидкости, увеличение объёма циркулирующей крови, повышение сосудистой, капиллярной и тканевой проницаемости (повышение гиалуронидазной активности крови), повышение гидростатического давления в результате гипертензии. Олигурия диагностируется у половины пациентов (связана с уменьшением массы функционирующего нефрона, снижением фильтрации в результате внутрисосудистых тромбов, отеком сосудистого эндотелия и подоцитов, пролиферацией эндотелия и мезангиума). В типичных случаях возобновление диуреза отмечается в первые 3-7 дня заболевания.
При ЛАБОРАТОРНОМ обследовании обнаруживают протеинурию (1-2 г\ сутки), которая имеет селективный характер (преимущественно, альбумины) и возникает за счет повышения проницаемости клубочкового фильтра и снижения реабсорбции белка. Гематурия – обязательный симптом ОПСГН. Увеличение проницаемости стенок капилляров клубочков приводит к эритроцитурии, тромбоз и разрыв сосудов клубочков-заканчивается макрогематурией. Лейкоцитурия (мононуклеарная, эозинофильная или смешанная) может встречаться в начале заболевания в результате поражения интерстиция. Количество гиалиновых цилиндров повышается за счет свертывания белка в почечных канальцах на фоне кислой среды. Появление эритроцитарных цилиндров – признак нефрита и доказательство гломерулярного происхождения гематурии, а зернистых – показатель тяжести поражения почек. У детей из ОПСГН часто наблюдается гипоальбуминемия, анемия за счет гиперволемии; характерны увеличение СОЭ, нейтрофилёз, при наличии инфекционного очага – лейкоцитоз. У части больных при значительной олигурии отмечается повышение содержания в крови мочевины и креатинина, ацидоз, гиперкалиемия, гипермагниемия. Эти нарушения функции почек при возобновлении диуреза и адекватной терапии быстро ликвидируются. Возможно развитие острой почечной недостаточности. При ОПСГН происходит как развитие гиперкоагуляции (повышение протромбинового индекса, угнетение фибринолитической активности крови), так и повышение общей антикоагулянтной активности крови. У 60 –95 % больных с ОПСГН после инфекции верхних дыхательных путей отмечалось увеличение титра антистрептолизина О в первые 6 месяцев болезни и в 80% - титра антиДНК-азы. Анти-М-протеиновые антитела определяются через 4-6 недель после стрептококковой инфекции в течение нескольких лет. У 80-90% больных ОПСГН на 1-ой неделе заболевания в крови находят циркулирующие ИК. С 2-ой по 6-ю неделю отмечается снижение уровня С3, С5 или С1j, С4, С2, С3 фракций комплемента. В течение 2-х месяцев происходит повышение содержания Ig G, Ig M, реже -Ig A.
Экстраренальные проявления ОПСГН длятся 2-3 недели, мочевой синдром может сохраняться до 3 месяцев.
Вариант ациклического течения острого ГН характеризуется постепенным началом, изолированным мочевым синдромом и возможными кратковременными (чаще незамеченными) экстраренальными симптомами.
ОСЛОЖНЕНИЯМИ нефрита могут быть почечная эклампсия – ангиоспастическая энцефалопатия (головная боль, артериальная гипертензия, брадикардия, тошнота, рвота; в дальнейшем – потеря сознания, клонико-тонические судороги, кома); острая почечная недостаточность; нарушение сердечно-сосудистой системы.
ДИАГНОЗ. В типичных случаях наличие предыдущей стрептококковой инфекции и латентного периода после нее, острое начало заболевания, четко выраженный клинико-лабораторный комплекс нефритического синдрома, позитивные результаты серологического обследования, выявление циркулирующих ИК и низкого уровня С3 фракции комплемента в сыворотке крови дают возможность поставить диагноз ОПСГН. Диагностические трудности возникают при ациклическом течении заболевания.
Для диагностики необходимо провести следующие обследования: анализы мочи общий и по Нечипоренко; посевы мочи трижды до назначения антибиотиков; пробу Зимницкого; ежедневное определение диуреза, выпитой жидкости, массы тела и артериального давления; клинические анализы крови с гематокритным показателем; определение содержания креатинина, мочевины, электролитов, холестерина, липидов, общего белка и белковых фракций в биохимическом анализе крови; коагулограмму; определение титра комплемента и антистрептококковых антител; пробу Реберга; осмотр глазного дна; ЭКГ; рН мочи, экскрецию аммиака с мочой; ультразвуковое исследование почек; определение показателей ацидо- и аммониогенеза, уровня b2-микроглобулина. Биопсию проводят в специализированном стационаре при отягощенном анамнезе, атипичной клинической или лабораторной картине, нефротическом синдроме в сочетании с нефритическим, гипертензией или макрогематурией, которая длится больше 3-х недель, низком уровне С3-комплемента в течение 8 недель и больше, протеинурии в течение 6 месяцев и постоянной гематурии после 12 месяцев болезни.
ЛЕЧЕНИЕ больных ОПСГН должно быть комплексным, проводиться в стационаре и включать в себя базисную и симптоматическую терапию. Соблюдение режима и диеты являются первыми пунктами базисной терапии.
На время экстраренальных проявлений болезни ребенку необходим постельный режим ( обычно 1-3 недели). С улучшением самочувствия, снижением артериального давления режим расширяется до палатного, при котором необходимо продолжать держать ноги и поясницу в тепле.
В диете ограничивают жидкость, поваренную соль и белок. Жидкость назначается по диурезу предыдущего дня с учетом потерь с перспирацией. Исключение соли рекомендуют в олигоанурическую фазу и в период схождения отеков. Когда нормализуется артериальное давление и сходят отеки в еду добавляют натрия хлорид, начиная с 0,5-1,0 г\ сутки. В дальнейшем количество соли постепенно увеличивают до 0,75 % нормы (50мг\ кг в сутки), и это ограничение должно длиться 1-2 года. Существенное уменьшение белка необходимо больным с азотемией. В этих случаях назначают сахарно-фруктовые дни (из расчета 12-14 грамм углеводов на 1 кг массы тела) с включением в диету сахара, груш, яблок, варения, меда, клюквенного и лимонного соков, при необходимости – рисового или манного пудингов, булки. Расширение диеты проводят сначала за счет белков растительного происхождения (рис, греча, картофель, капуста, морковь, масло, хлеб и др). С 5-го дня вводят молочные продукты (1-1,5 грамм белка на кг массы); на 7-10 день количество белка доводят до физиологичной нормы (2,5 г\ кг): в рацион вводят яйцо, пшеничный хлеб, рыбу, сыр, потом – мясо. В период олигурической фазы диета должна быть гипокалийной, но при нормальном диурезе и при появлении полиурии нужно употреблять продукты, обогащенные калием (изюм, чернослив, сухофрукты, бананы, арбузы, апельсины, картофель, квашеную капусту).
Антибактериальную терапию назначают всем больным ОПСГН. Используют пеницилины, макролиды в среднетерапевтических дозах в течение 8-10 дней. Наличие хронических очагов инфекции, интеркуррентных заболеваний нуждается в цикличном назначении антибиотиков (3-4 цикла) или продолжении терапии бициллином до 6 месяцев от начала болезни. Обязательна консервативная санация хронических очагов инфекции; тонзиллэктомию уместно проводить через 6-12 месяцев от начала заболевания.
Для симптоматического лечения значительных отеков используют лазикс (1-2 мг\ кг), возможно, в комбинации с гипотиазидом (0,5-1 мг\ кг) или с амилоридом (школьникам – 5мг за 2 часа до введения фуросемида).
Умеренное повышение артериального давления лечится назначением диеты и мочегонных препаратов. В терапии стойкой гипертензии используют препараты центрального действия (клофелин, резерпин), ингибиторы ангиотензинпревращающего фактора (каптоприл, капотен), блокаторы рецепторов ангиотензина 11 (нифедипин). Диуретический и гипотензивный эффект имеют эуффилин, который улучшает клубочковую фильтрацию, и гепарин в сочетании с антиагрегантами. Эффективность назначения антиагрегантов и гепарина при ОПСГН клиническими испытаниями не доказана.
К общеукрепляющей и десенсебилизующей терапии (назначение витаминов, препаратов кальция, антигистаминных) следует относиться сдержанно, а их назначение считать необоснованным.
Детям с доброкачественной гематурией, связанной с гиперкальцийурией, в диете ограничивают кальций, повышают количество жидкости, иногда назначают диуретики. Длительная эритроцитурия при остром ГН требует назначение делагила в течение 1,5 лет.
В лечении мембранозно-пролиферативного варианта хронического ГН, кроме базисной и симптоматической терапии, используют иммуносуппрессоры – глюкокортикоиды и цитостатики. Возможно длительное назначение преднизолона в альтернирующем режиме или использование 4-компонентной схемы (глюкокортикоиды, цитостатики, антикоагулянты и антиагреганты).
Быстропрогрессирующее течение экстракапиллярного с полумесяцами ГН у детей является абсолютным показанием к 4-х компонентной терапии (преднизолон и циклофосфан- в терапевтических или пульсовых дозах, курантил, гепарин) и\ или плазмаферез.
ДИСПАНСЕРНОЕ НАБЛЮДЕНИЕ за детьми, которые перенесли острый ГН длится 5 лет и состоит из периодических осмотров, измерения артериального давления, проведения анализов мочи (каждые 10 дней в течение первых 3-х месяцев, 1 раз в месяц – следующие 9 месяцев, 1 раз в квартал – в течение 2-х лет и при интеркуррентных заболеваниях) и санацию хронических очагов инфекции.
Дети с ОПСГН выздоравливают в 85-95 % случаев; в 1-2% случаев происходит трансформация в быстропрогрессирующий ГН; хронический нефрит развивается у 3-5% детей дошкольного возраста и у 12-15% детей, которые заболели в старшем школьном возрасте.
НЕФРОТИЧЕСКИЙ СИНДРОМ
НЕФРОТИЧЕСКИЙ СИНДРОМ (НС) – клинико-лабораторный симптомо-комплекс, который входит во многие заболевания почек и характеризуется протеинурией, гипопротеинемией, диспротеинемией, гиперлипидемией, отеками.
КЛАССИФИКАЦИЯ НС (Н.Д.Савенкова, А.В.Папаян, 1997).
Клинические формы НС:
Первичный НС:
1.Врожденный и инфантильный:
- врожденный “финского” типа с микрокистозом и “французского” типа с диффузными
мезангиальными изменениями;
- НС с минимальными изменениями (генуинный, идиопатический НС);
- НС с мезангио-пролиферативными изменениями или с фокально-сегментарным гломерулосклерозом (ФСГС).
2.НС при первичном гломерулонефрите:
- НС с минимальными изменениями;
- НС с мембранозными изменениями или ФСГС, с мембранозно-пролиферативными, с мезангио-пролиферативными, с экстракапиллярными,с фибропластическими изменениями, с полумесяцами.
Вторичный НС:
1.Врожденный и инфантильный НС:
- ассоциируемый с эндокринопатиями, кистозной гипоплазией легких, порэнцефалией
- тромбозом почечных сосудов, внутриутробными инфекциями.
2.НС при почечном дизэмбриогенезе, рефлюкс -нефропатии .
3.НС при наследственных и хромосомных заболеваниях.
4.НС при системных васкулитах и диффузных заболеваниях соединительной ткани.
5.НС при острых и хронических инфекционных заболеваниях, протозоозах, гельминтозах.
6.НС при первичном, вторичном, наследственном амилоидозе.
7.НС при саркоидозе, опухоли Вильмса, лейкозах, лимфосаркоме, лимфогрануломатозе.
8.НС при эндокринных заболеваниях (сахарный диабет, аутоиммунный тиреоидит), псориазе.
9.НС при гемоглобинопатиях.
10.НС при гемолитико-уремическом синдроме.
11.НС при укусе змей, пчел, ос, а также НС при введении вакцин и медикаментозное
поражение почек.
Стадии активности НС: активная, неактивная – клинико-лабораторная ремиссия (полная или частичная, на или без поддерживающей терапии).
Тяжесть НС: -средней тяжести – гипоальбуминемия до 20 г\ л;
-тяжёлая – гипоальбуминемия ниже 20 г\ л;
-крайнетяжелая – гипоальбуминемия ниже 10 г\ л.
Вариант ответа на глюкокортикоидную терапию:
гормоночувствительный; гормонозависимый; гормонорезистентный.
Течение НС: острый с окончательной ремиссией без последующих рецидивов;
хронический рецидивирующий, персистующий, прогрессирующий;
быстро прогрессирующий – подострый, злокачественный.
Функция почек:- сохранена – ПН0;
-нарушение функции почек в остром периоде;
-ОПН, ХПН.
Осложнения НС:
Нефротический гиповолемический криз (шок, абдоминальный болевой синдром, рожеподобные эритемы), почечная эклампсия, тромбозы артериальные и венозные, ОПН, ХПН, вирусная, бактериальная, микотическая инфекция;
Осложнения, обусловленные лечением глюкокортикоидами, цитостатиками, антикоагулянтами, антиагрегантами, нестероидными противовоспалительными препаратами и производными аминохинолонов.
Различают клинические формы НС: 1) чистые, которые проявляются клинико-лабораторным симптомокомплексом и смешанные – НС с гематурией и гипертензией; 2) полные – имеют все клинико-лабораторные симптомы и неполные, при которых отсутствует один (реже – два) из клинических или лабораторных симптомов.
В 65-70 % случаев дети болеют первичным НС, в 30-45 % случаев НС имеет вторичный характер. Считают, если НС возник у ребенка в возрасте 1-7 лет, то это - стероидочувствительный липоидный нефроз (генунный НС) в 90 % случаев, если в возрасте 7-16 лет – в 50 % случаев, у взрослых – в 20 % случаев.
НЕФРОТИЧЕСКИЙ СИНДРОМ С МИНИМАЛЬНЫМИ ИЗМЕНЕНИЯМИ (НСМИ)
НСМИ – липоидный нефроз – характеризуется полным клинико-лабораторным симптомокомплексом НС, обычно, отсутствием артериальной гипертензии, гематурии, нарушения функции почек и значительных изменений в клубочках.
НСМИ является патологией детей раннего и дошкольного возраста. Чаще болеют мальчики (2:1). Отягощенный семейный аллергологический анамнез и аллергические проявления у детей с липоидным нефрозом диагностируются чаще (50-70 % ) сравнительно с другими формами первичного ГН.
Факторы, которые предшествуют развитию НСМИ, не удается обнаружить в 30-40% случаев. У части детей заболевание развивается после прививок, вирусных или бактериальных детских инфекций, введения иммуноглобулина. Не исключена роль хронических латентных вирусных инфекций, стрептококков, токсоплазм, лептоспир, малярийных плазмодиев в этиопатогенезе НСМИ.
ПАТОГЕНЕЗ и ПАТОМОРФОЛОГИЯ. В основе липоидного нефроза лежит увеличение проницаемости стенки гломерулярных капилляров для протеина в результате изменения их электрического заряда; дисбаланс иммунной системы; генетическая склонность.
В биоптате находят минимальные изменения, при электронной микроскопии – слияние педикул эпителия, покрывающих капилляры. Базальная мембрана теряет сиалопротеины и подоциты закрывают увеличенные межмолекулярные поры мембран, Эти изменения похожи на дистрофичные. Вследствие этого происходит потеря анионов и негативного заряда стенки капилляров, повреждение базальной мембраны лейкоцитами и лизосомальными ферментами и увеличение проницаемости гломерулярного фильтра для белка. Вакуольная и гиалиновая дистрофия эпителия канальцев почек является вторичной и обусловлена избыточным количеством профильтрованного белка, который в дальнейшем приводит к блокаде лимфатической системы почки, ее отеку и развитию очагов склероза.
Некоторые авторы считают, что в основе патогенеза липоидного нефроза лежит дисфункция в системе Т-клеточного иммунитета, гиперпродукция интерлейкина-2.
В отличие от других вариантов ГН, при НСМИ в почках не находят отложений комплемента, иммуноглобулинов, электронно-плотных депозитов. Исключение составляет вариант ГН с очаговым гломерулосклерозом, при котором 20% больных – стероидочувствительны, у других через 3-5 лет развивается ХПН. Больные с НС при БПГН, первично хронических формах ГН, а также при вторичном НС имеют в биоптате мембранозную гломерулопатию, мембранозно-пролиферативные изменения, мезангиокапиллярный гломерулонефрит, экстракапиллярные и фибропластические поражения, которые развиваются в результате иммунокомплексного и аутоиммунного механизмов.
КЛИНИКА и ДИАГНОСТИКА. НСМИ чаще развивается постепенно с нарастающих отеков (мягких, асимметричных, подвижных): сначала - лица, поясницы, потом – анасарка, асцит, гидроторакс, гидроперикард. Отечный синдром возникает в результате гипопротеинемии (за счет протеинурии, повышения катаболизма и снижения синтеза альбуминов, перемещения белков во внесосудистое пространство) и вторичного гиперальдостеронизма. Среди первых симптомов НСМИ отмечают нарастающую бледность кожи с ее дистрофическими изменениями, анорексию, тошноту, рвоту метеоризм, диарею, уменьшение суточного диуреза (олигурия связана с гиповолемией, гиперальдостеронизмом, поражением канальцев). Артериальное давление, обычно, в пределах возрастной нормы. Иногда отмечают одышку, тахикардию, систолический шум на верхушке, увеличение печени и селезенки.
Суточная потеря белка с мочой составляет 2,5 –30 г\ л и больше. Мочевой осадок содержит гиалиновые, зернистые, эпителиальные цилиндры. Возможна непродолжительная лейкоцитурия за счет иммунопатологических процессов в почках.
Определение селективности протеинурии является важным диагностическим и прогностическим тестом. Селективная протеинурия (выделение низкомолекулярных альбуминов) присущая НСМИ, обуславливает чувствительность к глюкокортикоидной терапии и лучший прогноз. Неселективная протеинурия, когда в моче есть много высокомолекулярных белков (глобулины гамма, альфа2-макроглобулины), обычно, является следствием фибропластических процессов и для липоидного нефроза не характерна.
Общий белок плазмы уменьшен, иногда – до 40 г\ л. Диспротеинемия обусловлена резким снижением концентрации альбуминов и глобулинов гамма и повышением уровня альфа2-глобулинов. Последний показатель свидетельствует о высокой активности патологического процесса и не является обязательным признаком НС.
В общем анализе крови отмечается гипохромная анемия, увеличение СОЭ (30-60 мм\ ч), возможен умеренный лейкоцитоз и эозинофилия.
Характерным для больных с НСМИ является нарушение липидного обмена: гиперлипидемия (больше 7 г\ л), гиперхолестеринемия (больше 6,5 ммоль\ л), повышение содержания триглицеридов (больше 2 ммоль\ л), что связано с дисфункцией печени и селезенки, а также зависит от поражения интермедиарного обмена в ферментной системе канальцев, низкого уровня в крови лецитин-холестеринацетилтрансферазы (в большом количестве выделяется с мочой) и низкой активности липопротеидлипазы. Гиперлипидемия сопровождается липидурией (до 1 грамма в сутки).
Концентрационная способность почек не нарушена. Клубочковая фильтрация может быть несколько сниженной только в период увеличения отеков.
Нарушения фосфорно-кальциевого обмена обусловлены дисфункцией почек и изменениями метаболизма витамина D. Снижение уровня железа, цинка, меди, кобальта в крови определяют склонность больных к анемиям, трофическим поражениям кожи, задержке роста, иммунодефицитов.
Частичный иммунодефицит Т-клеточного типа, снижение уровня IGG и IGA, иногда повышение содержания IGE обусловливает склонность к инфекционным заболеваниям.
С помощью сонографии у детей с липоидным нефрозом обнаруживают увеличение объема почек, повышение их гидрофильности.
Диагноз НСМИ у детей 2-7 лет в типичных случаях (90-95%) может быть поставлен по характерным клинико-лабораторным данным и ответу на глюкокортикоидную терапию без биопсии почек. Целесообразно выяснять наличие хронических персистуючих инфекций, которые могут обусловить гормонорезистентность. О рецидивирующем течении НС свидетельствуют 2 рецидива за год, о часто рецидивирующем –3 и больше рецидивов за год. Ремиссию констатируют при отсутствии протеинурии или ее показателях- менее 4 мг\ м кв. в час и достижении уровня протеина сыворотки 35г\ л.
Признаки нефротического синдрома бывают у больных нефротической формой первичного ГН, при врожденном и семейном НС, а также сопровождают вторичный НС при системных поражениях соединительной ткани, почечном дизэмбриогенезе, амилоидозе,отравлениях и проч. При первичном ГН с нефротическим синдромом в 70 % случаев происходит хронизация процесса.
ЛЕЧЕНИЕ активной стадии НСМИ проводят в стационаре. Кроме базисной и симптоматической терапии, назначают патогенетические средства.
Длительность постельного режима определяется экстраренальными проявлениями. После исчезновения отеков режим должен быть активным, с включением лечебной физкультуры для предотвращения тромботических осложнений.
Ограничение жидкости при отсутствии нарушения функции почек нецелесообразно, так как ухудшает реологические свойства крови, особенно на фоне стероидной и мочегонной терапии. Суточное количество жидкости должно отвечать диурезу за предыдущие сутки и экстраренальным потерям. Введение соли с едой ограничивают (но не исключают) в период выраженного отечного синдрома и максимальных доз преднизолона. Белок (сыр, кефир, отварное мясо, рыба) назначают соответственно возрастным нормам. Дотации белка (3-4 г\ кг\ сутки) оправданы после нормализации анализов мочи. Желательно ограничение жиров животного происхождения, введение в рацион растительных жиров. Назначают свежие фрукты, овощные соки, богатые калием, витаминами, ферментами. Дополнительное оральное введение калия показано детям при максимальном диурезе. Лечение больных с отягощенным аллергологическим анамнезом следует начинать с элиминационной диеты.
На высоте активности заболевания, в период назначения максимальных доз кортикостероидов, в течение 2-3 недель показана антибактериальная терапия.
Из мочегонных препаратов используют фуросемид (1-2 мг\ кг), верошпирон (2-5 мг\ кг)
Основной вид патогенетической терапии НС– лечение глюкокортикоидами и цитостатиками – используется как фармакодинамическое. Существуют разнообразные программы стероидной терапии НСМИ. В зависимости от того, имеет ли место дебют или рецидив заболевания, стероидозависимость или резистентность, осложнения основного заболевания или терапии, изменяется врачебная тактика. Эффективность патогенетической терапии оценивается по скорости наступления клинико-лабораторной ремиссии, частотой рецидивов, возможностью избежания летального исхода. Важным является прогнозирование эффективности лечения глюкокортикоидами. Частично в этом помогает определение количества глюкокортикоидных рецепторов на лимфоцитах крови и индекса стимуляции в реакции бласттрансформации с дексазоном. Более перспективным является использование формул, основанных на комплексе клинико-лабораторных признаков, которые отображают особенности течения заболевания.
Преднизолон назначают в максимальной суточной дозе 1-3,5 (2) мг\ кг на протяжении 6-8 недель, сначала – внутривенно, а после схождения отеков – перорально. Потом каждые 6-8 недель дозу снижают на 2,5 мг, и дозу 5 мг оставляют до конца лечения. Клинические наблюдения свидетельствуют, что альтернирующая схема (через день) применения глюкокортикоидов у больных НСМИ более эффективна, чем интермитирующая (3 суток ребенок получает препарат, 4 сутки – перерыв).
Использование цитостатических (ЦС) препаратов в патогенетической терапии уместно при частых рецидивах НСМИ, развитии стероидной зависимости, резистентности и токсичности. Последовательное назначение гормонов и цитостатиков позволяет повысить эффективность терапии, уменьшить длительность максимальных доз глюкокортикоидов. Преимущество предоставляют хлорбутину (максимальная суточная доза-0,2 мг\ кг), который назначают в течение 6-12 недель через 6-8 недель после лечения максимальными дозами глюкокортикоидов(ГК), потом переходят на 1\2 дозы до конца курса терапии или комбинируют с ГК.
Режим комбинированного назначения ГК и ЦС подбирается индивидуально, учитывая клиническую картину, ответ на ГК, возраст пациента и морфологический тип ГН.
ОСЛОЖНЕНИЯ НС могут быть обусловлены основным заболеванием, терапией или сочетанием тех и других факторов. В 6% больных диагностируют нефротичний криз – “внезапное” ухудшение состояния у детей с тяжелым НС, которое заканчивается гиповолемическим шоком. Абдоминальный нефротичний синдром (тошнота, рвота, абдоминальные боли, повышение температуры, выраженные отеки, анасарка) и мигрирующие рожеподобные эритемы – проявления нефротичного криза. Гиповолемический шок развивается при снижении альбуминов сыворотки ниже 10г\ л и дефиците ОЦК больше 25%. Почечная эклампсия (ангиоспастическая энцефалопатия) развивается у 5-6% детей при НС с гипертензией. Артериальные и венозные тромбозы, которые случаются у детей с НС могут заканчиваться летально.
Осложнениями и побочными действиями глюкокортикоидной терапии, которые требуют контрольных обследований и коррекции, являются вторичный синдром Иценко-Кушинга, гипокальциемия, остеопороз, остеонекроз, стероидный диабет, поражение пищеварительного канала, стероидная кардиопатия и гипокалиемия, артериальная гипертензия, психические нарушения, катаракта, нарушение функции щитовидной железы, острая и хроническая недостаточность коры надпочечников, синдром отмены глюкокортикоидной терапии. Последствиями цитостатичной терапии НС у детей могут быть угнетение гемопоэза, геморрагический цистит, панкреатит, инфекции, холеста-тический гепатоз, стоматит, аллопеция, которые имеют обратный характер. В катамнезе больных после лечения цитостатиками отмечена гонадотоксичность, тератогенное и канцерогенное действие. К осложнениям, обусловленным заболеванием и терапией, относятся инфекции, которые возникают в результате вторичного иммунодефицитного состояния. Вирусная инфекция у детей с НС встречается чаще, чем бактериальная и микотическая.
ДИСПАНСЕРНОЕ НАБЛЮДЕНИЕ И ПРОГНОЗ. Ребенка наблюдают нефролог и участковый педиатр. Анализы мочи и измерение артериального давления проводят 1 раз в 2 недели в первые 3 месяца после выписки из стационара, 1 раз в месяц - в следующие 9 месяцев, 1 раз в квартал – в следующие 2 года, а также при интеркуррентных заболеваниях. Важно обнаруживать и рационально лечить острые
или хронические инфекции. На протяжении года от начала клинико-лабораторной ремиссии прививки противопоказаны, в дальнейшем – нежелательны. Стойкая клинико-лабораторная ремиссия в течение 5 лет является основанием для снятия с учета.
Несмотря на затяжное течение и склонность к частым рецидивам 90% больных выздоравливают. Неблагоприятный исход может быть обусловлен переходом НС в смешанный синдром и хронизацией процесса, развитием тяжелых осложнений и наслоением интеркуррентных заболеваний.
ХРОНИЧЕСКАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ (ХПН)
ХПН – неспецифический синдром, который формируется на фоне тяжелого прогрессирующего заболевания почек (ХГН в первую очередь) и сопровождается снижением гомеостатической функции почек. Скорость клубочковой фильтрации (СКФ) составляет менее 20 мл/мин в течение 3-6 месяцев.
Морфологической основой ХПН является склероз клубочков, интерстиция и атрофия канальцев.
Хроническое заболевание почек (ХЗП) – собирательный термин для заболеваний почек с последующим прогрессированием процесса, даже при отсутствии снижения уровня СКФ.
ХЗП диагностируют, когда поражение почек длится больше 3-х месяцев при наличии отклонений в составе крови и мочи, отклонений инструментальных тестов и отклонений при нефробиопсии, или когда скорость клубочковой фильтрации (СКФ) менее 60 мл\ мин в течение 3 месяцев и дольше без других признаков поражения почек.
СТАДИИ ХЗП и ХПН
Стадия ХЗП |
Стадия ХПН |
КФ, мл/мин |
Креатинин крови, ммоль/л |
|
I |
Не имеет |
>90 |
<0,104 |
|
II |
I A (Тубулярная) |
89-60 |
0,105-0,176 |
|
III |
II |
59-30 |
0.177-0,351 |
|
IV |
III |
29-15 |
0,352-0,440 |
|
V |
IV |
<15 |
>0,440 |
|
ОСНОВНЫЕ КЛИНИЧЕСКИЕ СИНДРОМЫ ХПН:
кардиоренальная анемия (Нв менее 110 г\ л сатурация трансферина менее 20 %, левожелудочковая гипертрофия; в лечении – рекормон, ранферон, феролек,ферритин, ИАПФ);
белковоэнергетический дефицит (гипоальбуминемия, гипотрансферинемия, массо- ростовой показатель, отставание в росте; в лечении – белок из расчета 0,5 -4,0 г\ кг\ сутки в зависимости от стадии и соматотропный гормон);
костно-минеральные расстройства (Саxаp менее 4,44 ммоль\ л, сниженный уровень паратгормона, остеопения, остеопороз; в лечении- диета, ренагель, активный метаболит вит.Д; форкал, гормон роста);
нарушение гомеостаза (повышение азотистых шлаков и ацидоз, гиперкалиемия, СКФ менее 10-15 мл\ мин; в лечении – диета, сорбенты, энтеропассаж, глюкоза, кальций, диализ).
ТАКТИКА ЛЕЧЕНИЯ: 1.Лечение причинного заболевания (до СКФ более 30 мл\ мин) – специфическое и неспецифическое (ренопротекция).
Посиндромное лечение ХПН (при СКФ больше 60 мл\ мин – выборочное, при СКФ менее 60 мл\ мин -обязательное.
Заместительная терапия (при СКФ меньше 15мл\ мин.) – диализ и трансплантация.
Показание к хроническому диализу (перитонеального – до 10 лет, гемодиализа – после 10 лет) /трансплантации: уровень креатинина 0,3 ммоль/л – подготовка доступа, с 0,44 ммоль/л – диализ.
