
- •Часть 3
- •Растворимость. Способы выражения состава растворов Краткие теоретические сведения
- •Примеры решения задач
- •156, 2 Г раствора — 100,0 г н2о;
- •50,0 Г раствора — m1 г н2о;
- •1 Моль (278 г) FeSo4 ·7h2о содержит 1 моль (152 г) FeSo4 ;
- •50 Г FeSo4 ·7h2о содержит m2 г FeSo4 ;
- •Разбавленные растворы неэлектролитов Краткие теоретические сведения
- •Примеры решения задач
- •Растворы электролитов Краткие теоретические сведения
- •Примеры решения задач
- •Ионное произведение воды. Буферные растворы Краткие теоретические сведения
- •Примеры решения задач
- •Произведение растворимости Краткие теоретические сведения
- •Выражение для произведения растворимости имеет вид
- •Примеры решения задач
- •Гидролиз солей Краткие теоретические сведения
- •Примеры решения задач
- •Список литературы
- •Содержание
Произведение растворимости Краткие теоретические сведения
Для любого труднорастворимого электролита (Kt)х(Аn)у между его осадком и насыщенным раствором устанавливается равновесие вида
(Kt)х(Аn)у xKtz+ + yАnz–.
осадок насыщенный раствор
Константа равновесия процесса диссоциации мало растворимого вещества в его насыщенном растворе называется произведением растворимости ПР.
Выражение для произведения растворимости имеет вид
ПР =
![]() (+·[Ktz+])
x
(–
·[Аnz–])
y,
(46)
(+·[Ktz+])
x
(–
·[Аnz–])
y,
(46)
где а+, а– – активности катиона и аниона; + , – – коэффициенты активностей катиона и аниона; [Ktz+], [Аnz–] – равновесные молярные концентрации ионов, моль/дм3.
Поскольку насыщенный раствор труднорастворимого вещества содержит небольшие количества ионов, то есть является достаточно разбавленным, то при расчете ПР активности ионов можно заменить равновесными концентрациями. Тогда уравнение (46) примет вид
ПР = [ Ktz+] x [Аnz–] y. (47)
ПР электролита при данной температуре есть величина постоянная. Численные значения произведения растворимости большинства труднорастворимых электролитов приведены в справочной литературе.
По величине ПР судят о растворимости электролита: из двух однотипных соединений большей растворимостью обладает то, произведение растворимости которого больше.
Если произведение концентраций ионов (ПРрасч) в каком-либо растворе соли больше, чем табличное значение ПРтабл, то в растворе будет присутствовать осадок данного вещества. И наоборот, если ПРрасч < ПРтабл, то осадок данного вещества растворится.
Равновесные молярные концентрации ионов [Ktz+] и [Аnz–] пропорциональны растворимости вещества L (моль/дм3)
[Ktz+] = x L ; [Аnz–] = y L . (48)
Отсюда ПР[(Kt)х(Аn)у] = (xL)x × ( y L)y ; (49)
L
=
![]() .
(50)
.
(50)
Примеры решения задач
Пример 1. Вычислите произведение растворимости фторида кальция, если его растворимость в воде равна 0,024 моль/дм3.
Р е ш е н и е
Уравнение диссоциации имеет вид СаF2↓Û Са2+ + 2F –. Тогда по уравнению (48) равновесные концентрации ионов равны
[Са2+]= L; [ F –]= 2 L .
По формуле (47)
ПР(СаF2) = [Са2+]∙[ F –]2 = L × (2 L)2 = 4 L 3 = 4 × (0,024)3 = 5,53 × 10-5.
Пример 2. Выпадет ли осадок йодида серебра при 25 °С после сливания 0,1 дм3 0,005 М раствора нитрата серебра и 0,3 дм3 0,002 М раствора иодида калия, если ПР(AgI)табл = 1,1×10-16?
Решение
При сливании указанных реактивов идет реакция
AgNO3 + KI = AgI↓ + KNO3 ,
Ag+ + I– = AgI↓ .
Молярные концентрации ионов в растворах до смешивания равны
[Ag+] = 0,005 моль/дм3 ; [I–] =0,002 моль/дм3.
Концентрации ионов в растворах после смешивания
[Ag+]
=
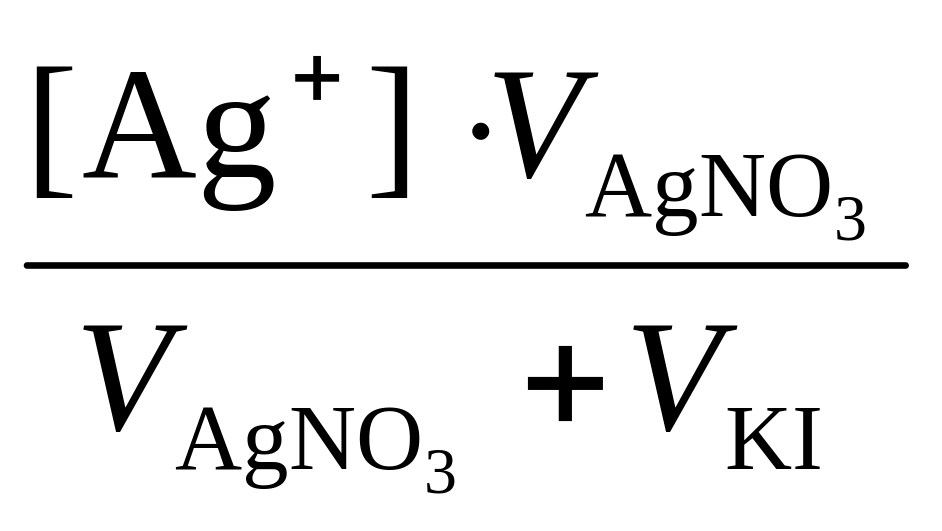 =
=![]() =
1,25∙10-3
моль/дм3;
=
1,25∙10-3
моль/дм3;
[I–]
=
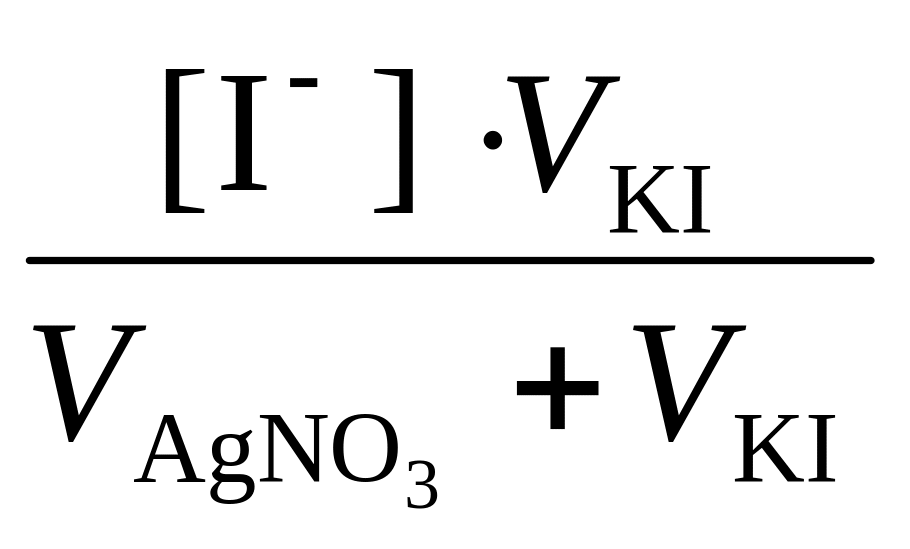 =
=![]() =
1,5∙10-3
моль/дм3 .
=
1,5∙10-3
моль/дм3 .
По формуле (47) находим произведение концентраций ионов (ПРрасч)
ПР(AgI)расч = [Ag+]×[I–]= 1,25∙10-3 ∙1,5∙10-3 = 1,88×10-6.
AgI осаждается, так как соблюдается условие выпадения осадка
ПР(AgI)расч > ПР(AgI)табл .
Пример 3. Вычислите (не учитывая гидролиза) растворимость фосфата бария в моль/л и г/л, а также молярные концентрации ионов в насыщенном растворе данной соли, если ПР [Ва3(РО4)2] = 6,3 · 10-39.
Р е ш е н и е
Фосфат бария
диссоциирует по схеме Ва3(РО4)2↓↔
3Ва2+
+ 2РО![]() ,
тогда по формуле (47)
,
тогда по формуле (47)
ПР [Ва3(РО4)2] = [Ва2+]3 · [РО ]2.
По уравнению (48) равновесные концентрации ионов равны
[Ва2+] = 3L; [РО ] = 2L .
Тогда по по формуле
(50) L
=
![]() моль/л.
моль/л.
Молярная масса фосфата бария М2(Ва3(РО4)2) = 602 г/моль, тогда растворимость, выраженная в г/л
L = 602 · 9 · 10-9 = 5,42 · 10-6 г/л.
Концентрации ионов [Ва2+] = 3L = 3 · 9 · 10-9 = 2,7 · 10-8 моль/л;
[РО ] = 2L = 9 · 10-9 · 2 = 1,8 · 10-8 моль/л.
Пример 4. Выпадет ли осадок галогенида серебра, если к 1 л 0,1 М раствора [Ag(NH3)2]NO3, содержащему 1 моль аммиака добавить:
а) 110–5 моль КВr; б) 110–5 моль КI.
Р е ш е н и е
Для решения вопроса о возможности разрушения комплексного иона за счет связывания комплексообразователя в малорастворимую соль необходимо оценить значения равновесных концентраций ионов в рассматриваемой системе. Для этого из справочника [8] выбираем значение константы нестойкости комплекса и произведения растворимости соответствующих солей
КН([Ag(NH3)2]+) = 5,9 · 10–8; ПР(AgBr) = 5,3 · 10–13; ПР(AgI) = 8,3 · 10–17.
Данная комплексная соль диссоциирует по схеме
[Ag(NH3)2]NO3 [Ag(NH3)2]+ + NO .
По определению для комплексного иона [Ag(NH3)2]+
КН([Ag(NH3)2]+)
=
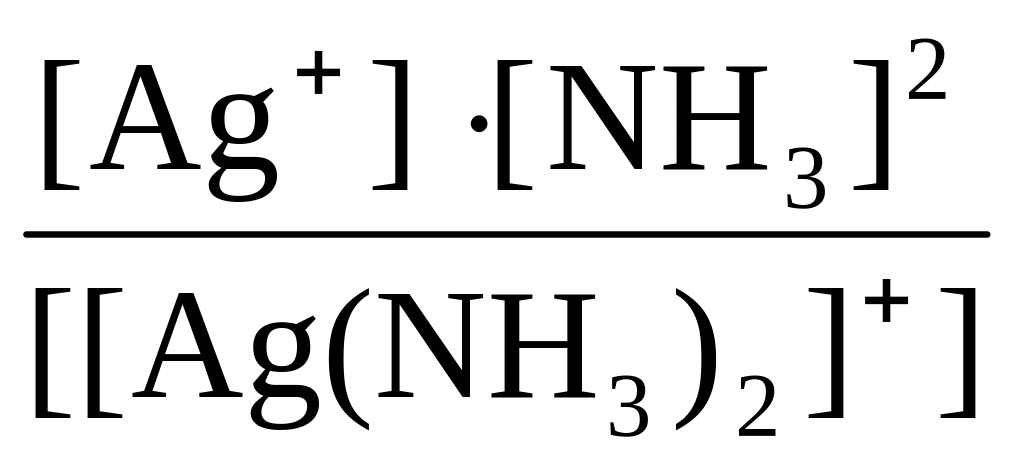 .
.
[NH3] ≈ С2(NH3) = 1 моль/л, так как концентрация молекул аммиака, образовавшихся вследствие вторичной диссоциации комплексного иона мала.
Из схемы первичной диссоциации следует, что
[[Ag(NH3)2]+] ≈ С2([Ag(NH3)2]NO3) = 0,1 моль/л.
Тогда концентрация ионов Ag+ равна
[Ag+]
=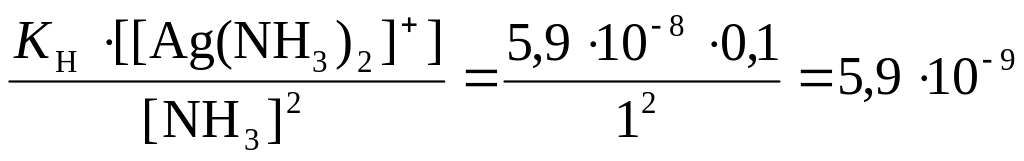 моль/л.
моль/л.
Концентрацию ионов Br –, достаточную для осаждения AgBr найдем из выражения для ПР (AgBr)
[Br
–] =
![]() моль/л.
моль/л.
Так как необходимая для осаждения бромида серебра концентрация ионов брома ([Br –] = 8,9810–5 моль/дм3) больше добавляемой в составе бромида калия ([Br –] = 110–5 моль/дм3), то осадок бромида серебра не выпадает.
Концентрацию ионов I–, достаточную для осаждения AgI найдем по аналогии
[I–]
=
![]() моль/л.
моль/л.
Так как необходимая для осаждения йодида серебра концентрация ионов йода ([I –] = 1,4110–8 моль/дм3) меньше добавляемой в составе йодида калия ([I –] = 110–5 моль/дм3), то реакция разрушения комплексного иона в данном случае будет протекать
[Ag(NH3)2]NO3 + 2КI = AgI↓ + КNO3 + 2NH3 .
