
- •Принцип и характеристика метода
- •Ход анализа
- •Обработка полученных результатов
- •Порядок выполнения работы
- •Результаты анализа воды
- •Принцип и характеристика метода
- •Порядок выполнения работы
- •Параметры процесса биохимического окисления
- •Принцип и характеристика метода
- •Обработка полученных результатов
- •Анализ загрязняющих веществ в атмосферном воздухе
- •394000, Воронеж, пр. Революции, 19
Ход анализа
Подготовить четыре градуированные склянки на 150– 200 см3. В первые две налить предварительно разбавленную исследуемую воду, в третью и четвертую – разбавляющую воду. В первой и третьей склянке сразу же определить содержание растворенного кислорода, вторую и четвертую склянки поставить в термостат при 20 оС. Через 20 сут определить в этих пробах содержание растворенного кислорода. Перед непосредственным определением растворенного кислорода отградуировать склянку. Для этого взвесить на технических весах с точностью до 0,01 г пустую склянку с пробкой, а затем доверху заполненную дистиллированной водой. Разность даст массу воды в склянке и ее объем. В отградуированную склянку вместимостью 200 – 250 см3 при помощи резиновой трубки, опущенной на дно, осторожно налить доверху исследуемую воду. Опуская пипетку до дна склянки, прилить по 1 см3 раствора хлористого марганца и раствора щелочной смеси (КОН + КI). Закрыть склянку пробкой, взболтать и поставить для отстаивания образовавшегося осадка. Бурый осадок Mn(ОН)4 растворить, приливая 2 – 3 см3 концентрированной соляной кислоты. Перемешать раствор и перелить в чистую коническую колбу. Оттитровать выделившийся йод раствором тиосульфата натрия в присутствии 1 см3 раствора крахмала до исчезновения синей окраски.
Обработка полученных результатов
БПК20 разбавляющей воды (мг О2 · дм3) – Х1
![]() (8)
(8)
![]() (9)
(9)
где а1 – объем раствора тиосульфата натрия, пошедший на титрование пробы до выдерживания в термостате, см3; а2 – объем раствора тиосульфата натрия, пошедший на титрование пробы через 20 сут, см3; V1 – объем склянки, в которой проводилось определение кислорода до выдерживания, см3; V2 – объем склянки, в которой выдерживалась проба, см3; k – поправочный коэффициент для приведения концентрации тиосульфата натрия точно к 0,005 моль/дм3; 0,08 – 1/100 доля грамм-эквивалента кислорода; 2 – объем реактивов, прибавляемых в склянку при определении содержания кислорода, см3.
БПК5 исследуемой воды (мг О2 · дм3) – Х2
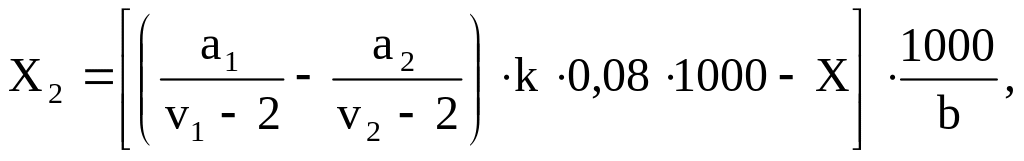 (10)
(10)
где b – объем исследуемой сточной воды (см3), взятой для анализа и разбавленной до 1 дм3.
Порядок выполнения работы
Получить у преподавателя воду для исследования и разбавляющую воду.
Определить содержание растворенного кислорода в исследуемой и разбавляющей воде.
Поставить пробы с исследуемой и разбавляющей водой в термостат для биохимического окисления.
Определить содержание растворенного кислорода в исследуемой и разбавляющей воде через 20 сут.
5. Результаты определений занести в табл. 1.
Таблица 1
Результаты анализа воды
№ склянки |
Вместимость Склянки, см3 |
Объем раствора Na2S2O3, см3 |
Объем исследуемой пробы, см3 |
БПК20, мг/дм3 |
1 2 3 4 |
|
|
|
|
Содержание отчета
1. Формулировка цели работы.
2. Используемые приборы и реактивы.
3. Порядок выполнения работы.
4. Таблица экспериментальных данных.
5. Выводы.
Лабораторная работа 2
ИССЛЕДОВАНИЕ КИНЕТИКИ
БИОХИМИЧЕСКОГО ОКИСЛЕНИЯ
Цель работы: освоить методику расчета константы скорости реакции биохимического окисления на основе экспериментальных данных.
Краткие теоретические сведения
В природе процесс биохимического окисления протекает самопроизвольно, но глубина его зависит от природы органических соединений. Аэрация воды способствует стадии окисления. Биохимическое окисление органических веществ длится несколько суток, Скорость его лимитируется концентрацией органических веществ и зависит от напряженности действия факторов, оказывающих влияние на жизнедеятельность организма. Если выразить концентрацию органических соединений через БПК, то можно охарактеризовать скорость их разложения через константу k. Это связано с тем, что биохимический распад основного количества (около 99 % мас.) органических соединений описывается уравнением реакции первого порядка, пользуясь которым, можно вычислить константу скорости биохимического разложение органического вещества k.
![]() (1)
(1)
где C – начальная концентрация органических примесей, мг/дм3;
С – текущая концентрация органических примесей, мг/дм3; k – константа скорости биохимического окисления, сут-1; t – продолжительность процесса, сут.
