
- •Топохимические реакции.
- •Уравнение Ерофеева.
- •Дисперсные системы. Основные понятия и классификации.
- •Свободная поверхностная энергия и поверхностное натяжение.
- •Методы определения поверхностного натяжения.
- •Смачивание. Работа когезии и адгезии.
- •Пав. Адсорбция на границе раздела жидкость-газ.
- •Уравнение Лангмюра, Шишковского, правило Траубе.
- •Адсорбция веществ на твёрдой поверхности. Уравнение Фрейндлиха.
- •Кинетика гетерогенных процессов. Диффузионные процессы. Законы Фика.
- •Растворение твёрдых и газообразных веществ в жидкостях.
- •Адсорбция на границе раздела твёрдое вещество-газ.
- •Адсорбция на границе раздела твёрдое вещество-жидкость. Молекулярная адсорбция электролитов.
- •Адсорбция на границе раздела твёрдое вещество-жидкость. Адсорбция электролитов.
- •Адсорбционное понижение прочности твёрдых тел.
- •Каталитические реакции. Особенности их протекания.
- •Гомогенный катализ.
- •Гетерогенный катализ.
- •Роль поверхностных явлений при флотации руд.
- •Получение и свойства коллоидных систем.
- •Теория активных столкновений.
Адсорбционное понижение прочности твёрдых тел.
Прочность обусловлена силами взаимодействия частиц, составляющих твёрдое тело. Величина прочности пропорциональна поверхностному натяжению твердого тела (чем оно больше, тем больше прочность). ПАВ, адсорбирующиеся на поверхности твёрдого тела, понижают его поверхностное натяжение, тем самым уменьшая прочность. Полярные растворители по отношению ко многим твёрдым веществам обладают адсорбционной активностью, в результате этого смачивание приводит к уменьшению их прочности на 20-30%. Сильно понижают прочность твёрдых тел растворы электролитов. Их действие максимально при очень низкой концентрации. Органические ПАВ на 40-60% понижают прочность. Адсорбционное понижение прочности используется при обработке металла резаньем и давлением. В присутствии ПАВ меньше изнашивается режущий инструмент, т.к. способствует самозатачиванию режущей кромки инструмента.
Эффект Ребиндера имеет ряд особенностей:
На каждый тип твёрдого тела действуют лишь некоторые определённые среды;
Механические свойства изменяются после взаимодействия со средой;
После удаления среды механические свойства восстанавливаются;
Понижение прочности наблюдается при небольших концентрациях адсорбционного вещества;
Возможно в определённом интервале температур;
Каталитические реакции. Особенности их протекания.
Каталитическими называются реакции, протекающие с участием катализатора.
Катализаторы – вещества, которые не входят в состав конечных продуктов реакции. Вступают в катализ с химическими участниками реакции, образуя промежуточные вещества.
Различают положительный катализ (наличие катализатора ускоряет реакцию) и отрицательный (происходит замедление реакции или ингибирование).
В некоторых случаях катализатор могут быть один из участников реакции – автокаталитические реакции:
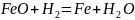
Все виды катализа можно разделить на:
гомогенный - катализатор и другие реагирующие вещества находятся в одной фазе:

гетерогенный – катализаторы и реагирующие вещества находятся в различных фазах, а химическое превращение протекает на поверхности катализа.

Особенности протекания:
К. не влияет на термодинамическое равновесие, он изменяет лишь скорость;
Действие катализатора является специфичным, т.е. К. влияет лишь на стадию;
Действие катализатора селективно;
Необходимо малое количество катализатора;
Скорость реакции пропорционально концентрации катализатора;
Действие К. зависит от его физического состояния и от присутствия посторонних вещей.
Смесь К. действует сильнее.
Гомогенный катализ.
К гомогенным каталитическим реакциям относятся реакции, протекающие в газовой фазе или в растворе.
Основные положения теории:
В результате реакции происходит образование неустойчивых промежуточных соединений, в состав которых входит катализатор и реагирующее вещество;
Расход в результате реакции промежуточных соединений;
Регенерация катализатора;


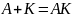

Если промежуточное соединение находится в равновесии с исходными веществами, то их называют веществами Аррениуса.
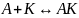
 – константы
скорости образования, разложения
соединения и образования продуктов
реакции соответственно.
– константы
скорости образования, разложения
соединения и образования продуктов
реакции соответственно.


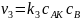
 – аналитическая
концентрация катализатора;
– аналитическая
концентрация катализатора;
 -
концентрация промежуточного соединения;
-
концентрация промежуточного соединения;
Приравняв
 ,
и выразив, подставим полученное в
уравнение 3:
,
и выразив, подставим полученное в
уравнение 3:

В обоих случаях скорость прямо пропорциональна концентрации катализатора. Порядок реакции будет колебаться от 1 до 2.
Если полученные вещества не находятся в равновесии с исходными веществами, их называют вещества Вант Гоффа, при этом
 .
.

Приравняв , и выразив, подставим полученное в уравнение 3:

Предельные случаи всегда соответствуют реакциям 1-го порядка: в первом случаи по А, а во втором – по В. Скорость реакции пропорционально концентрации катализатора.




