
- •Топохимические реакции.
- •Уравнение Ерофеева.
- •Дисперсные системы. Основные понятия и классификации.
- •Свободная поверхностная энергия и поверхностное натяжение.
- •Методы определения поверхностного натяжения.
- •Смачивание. Работа когезии и адгезии.
- •Пав. Адсорбция на границе раздела жидкость-газ.
- •Уравнение Лангмюра, Шишковского, правило Траубе.
- •Адсорбция веществ на твёрдой поверхности. Уравнение Фрейндлиха.
- •Кинетика гетерогенных процессов. Диффузионные процессы. Законы Фика.
- •Растворение твёрдых и газообразных веществ в жидкостях.
- •Адсорбция на границе раздела твёрдое вещество-газ.
- •Адсорбция на границе раздела твёрдое вещество-жидкость. Молекулярная адсорбция электролитов.
- •Адсорбция на границе раздела твёрдое вещество-жидкость. Адсорбция электролитов.
- •Адсорбционное понижение прочности твёрдых тел.
- •Каталитические реакции. Особенности их протекания.
- •Гомогенный катализ.
- •Гетерогенный катализ.
- •Роль поверхностных явлений при флотации руд.
- •Получение и свойства коллоидных систем.
- •Теория активных столкновений.
Смачивание. Работа когезии и адгезии.
Характер межмолекулярного взаимодействия между жидкостью и поверхностью твёрдого тела будет зависеть от природы жидкой фазы:
Наблюдается процесс смачивания (вода-стекло) – капля частично растекается по поверхности.
Наблюдается процесс не смачивания (стекло-ртуть) – капля будет расплющиваться на поверхности под действием силы тяжести.
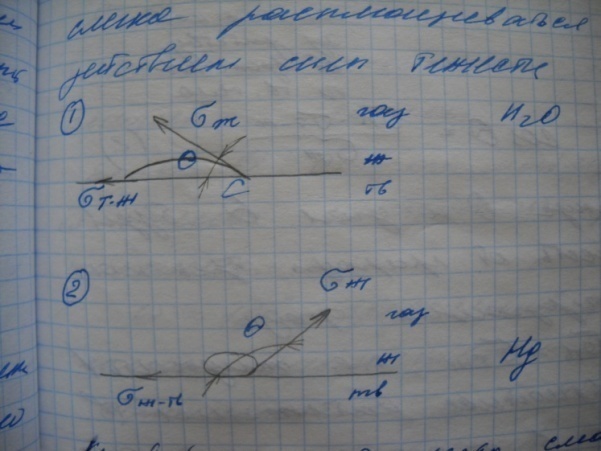
Краевой
угол
 – мера смачивания, этот угол образуется
между касательной к поверхности
жидкости, проводимой от точки С, лежащей
на периметре смачивания и смачивающей
поверхностью твёрдого тела.
– мера смачивания, этот угол образуется
между касательной к поверхности
жидкости, проводимой от точки С, лежащей
на периметре смачивания и смачивающей
поверхностью твёрдого тела.
Запишем условие равновесия капли в случаи контактного смачивания, которое описывается уравнением Юнга:

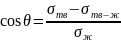
Косинус угла и краевой угол будут зависеть от природы трёх контактирующих фаз:
 ,
т.е. жидкость уменьшает поверхностное
натяжение твёрдого тела, в этом случаи
наблюдается смачивание:
,
т.е. жидкость уменьшает поверхностное
натяжение твёрдого тела, в этом случаи
наблюдается смачивание:

 ,
жидкость увеличивает поверхностное
натяжение твёрдого тела, в результате
наблюдается несмачивание:
,
жидкость увеличивает поверхностное
натяжение твёрдого тела, в результате
наблюдается несмачивание:
 .
.
Для определения условий смачивания используют такой критерий, как работа когезии и адгезии.
Работа
адгезии (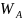 )
– характеризует силы сцепления между
двумя различными веществами. Эта работа
разрыва по межфазному слою в расчёте
на 1 см2.
Данная величина тем больше, чем сильнее
молекулярное притяжение жидкости к
поверхности твёрдого тела, т.е. чем
лучше смачивание.
)
– характеризует силы сцепления между
двумя различными веществами. Эта работа
разрыва по межфазному слою в расчёте
на 1 см2.
Данная величина тем больше, чем сильнее
молекулярное притяжение жидкости к
поверхности твёрдого тела, т.е. чем
лучше смачивание.


Работа когезии – характеризует силы сцепления между молекулами одного и того же вещества. Эта работа разрыва столба вещества с поперечным сечением в 1 см2.

Чем меньше поверхностное натяжение жидкости, тем лучше жидкость смачивает твёрдые тела.
Смачивание играет большую роль при протекании процессов, в том числе и обогащение руд методом флотации, диспергировании твёрдых тел и т.д.
Пав. Адсорбция на границе раздела жидкость-газ.
ПАВ – органические соединения, молекулы которых одновременно входят полярная функциональная группа и неполярный углеводородный радикал. Данные вещества уменьшают поверхностное натяжение: щёлочи, кислоты, амины.
Молекулы ПАВ, переходя в водный раствор, стремятся выйти на поверхность раздела фаз, полярная группа вниз, а неполярная группа вверх.
Молекулы ПАВ имеют двойное средство. Экспериментально было установлено, что ПАВ покрывает поверхность раствора слоем толщиной в 1 молекулу. При этом происходит уменьшение поверхностного натяжения.
Концентрирование вещества на поверхности раздела фаз, называется адсорбцией.
Адсорбция – самопроизвольный процесс, который сопровождается уменьшением свободной поверхностной энергии (поверхностного натяжения).
Адсорбент - вещества, на поверхности которого протекает адсорбция.
Адсорбат – вещество, которое поглощается из объёмной фазы.
Адсорбция будет зависеть от:
Природы адсорбата и адсорбента;
Состояния поверхности;
Температуры;
Концентрации фазы, из которой происходит адсорбция

инПАВ – вещества, увеличивающее поверхностное натяжение, т.к. они концентрируются в объёме жидкой фазы: растворы кислот, солей, щелочей.
Поверхностно индифферентные вещества – они распределяются равномерно. Данные вещества не изменяют поверхностное натяжение: неэлектролиты, моносахариды, полисахариды.
Зависимость адсорбции от поверхностного натяжения выражается уравнением Гиббса:

 – поверхностное
натяжение адсорбата. Она выражает
способность адсорбата понижать
поверхностное натяжение при переходе
из объёма жидкой фазы на поверхностный
слой.
– поверхностное
натяжение адсорбата. Она выражает
способность адсорбата понижать
поверхностное натяжение при переходе
из объёма жидкой фазы на поверхностный
слой.
 -
равновесная концентрация вещества в
растворе.
-
равновесная концентрация вещества в
растворе.

Важнейшей характеристикой адсорбции является изотерма адсорбции. Адсорбция бывает физическая (силы межмолекулярного взаимодействия) и химическая (химическая реакция).
