
- •Топохимические реакции.
- •Уравнение Ерофеева.
- •Дисперсные системы. Основные понятия и классификации.
- •Свободная поверхностная энергия и поверхностное натяжение.
- •Методы определения поверхностного натяжения.
- •Смачивание. Работа когезии и адгезии.
- •Пав. Адсорбция на границе раздела жидкость-газ.
- •Уравнение Лангмюра, Шишковского, правило Траубе.
- •Адсорбция веществ на твёрдой поверхности. Уравнение Фрейндлиха.
- •Кинетика гетерогенных процессов. Диффузионные процессы. Законы Фика.
- •Растворение твёрдых и газообразных веществ в жидкостях.
- •Адсорбция на границе раздела твёрдое вещество-газ.
- •Адсорбция на границе раздела твёрдое вещество-жидкость. Молекулярная адсорбция электролитов.
- •Адсорбция на границе раздела твёрдое вещество-жидкость. Адсорбция электролитов.
- •Адсорбционное понижение прочности твёрдых тел.
- •Каталитические реакции. Особенности их протекания.
- •Гомогенный катализ.
- •Гетерогенный катализ.
- •Роль поверхностных явлений при флотации руд.
- •Получение и свойства коллоидных систем.
- •Теория активных столкновений.
Уравнение Лангмюра, Шишковского, правило Траубе.
Уравнение Лангмюра выражает зависимость адсорбции от концентрации ПАВ:

– концентрация раствора ПАВ;
 -
константы;
-
константы;
 -
постоянная величина для всего
гомологического ряда. Это предельное
значение адсорбции, соответствующее
полному заполнению поверхности
молекулами ПАВ, когда толщина слоя
равна толщине в 1 молекулу.
-
постоянная величина для всего
гомологического ряда. Это предельное
значение адсорбции, соответствующее
полному заполнению поверхности
молекулами ПАВ, когда толщина слоя
равна толщине в 1 молекулу.
 -
постоянная только для данного вещества,
она увеличивается при переходе к каждому
гомологу.
-
постоянная только для данного вещества,
она увеличивается при переходе к каждому
гомологу.
Площадь:
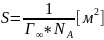
Толщина:
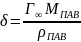
Уравнение Шишковского выражает общую зависимость поверхностного натяжения раствора от концентрации предельных кислот в водных растворах.
Предельные
кислоты:


 – константы,
связанные с константами уравнения
Ландгура;
– константы,
связанные с константами уравнения
Ландгура;

является постоянной для всего гомологического ряда;
константа увеличивается в 3-3.5 раза при переходе к каждому последующему гомологу.
Эмпирическое правило Траубе:
увеличивается при переходе к каждому последующему гомологу в 3-3.5 раза;
Константа из двух уравнений является :

которая выражает стремление молекул ПАВ концентрироваться на поверхности раздела фаз.

Адсорбция веществ на твёрдой поверхности. Уравнение Фрейндлиха.
Адсорбция на твёрдой поверхности в основном аналогична адсорбции на жидкости, но есть некоторые отличия:
При адсорбции на поверхности жидкости адсорбированное вещество извлекается из самой жидкой фазы, а адсорбция компонентов на поверхности твёрдого тела происходит из внешней среды.
На процессы адсорбции существенное влияние оказывает состояние поверхности адсорбата. Наиболее активными являются микровыступы, трещины и активные центры.
Различают физическую и химическую адсорбцию:
Физическая обусловленная действием сил междумолекулярного взаимодействия (на активированном угле). Химическая обусловлена действием химических сил (водородной, ионной или ковалентной связи).
При адсорбции на твёрдых адсорбентах определяют:
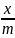 -
количество вещества адсорбирующегося
поверхностью;
-
количество вещества адсорбирующегося
поверхностью;

 – начальная
концентрация раствора;
– начальная
концентрация раствора;
- равновесная концентрация;
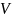 -
объём раствора адсорбата;
-
объём раствора адсорбата;
- масса адсорбента;
Т.к. поверхностное натяжение твёрдых тел определить невозможно, для описания изотермы адсорбции используют эмпирическое уравнение Фрейндлиха:

- Удельная адсорбция;
- равновесная концентрация адсорбата;
 -
эмпирические
коэффициенты;
-
эмпирические
коэффициенты;


Уравнение Фрейндлиха описывает только параболический участок изотермы адсорбции, т.е. уравнение справедливо в области средних концентраций.
 -
количество вещества, адсорбированного
единицей массы адсорбента при равновесной
концентрации равной 1 моль/л.
-
количество вещества, адсорбированного
единицей массы адсорбента при равновесной
концентрации равной 1 моль/л.
 -
степень приближения параболической
адсорбции от концентрации к прямолинейной
зависимости. Данный коэффициент
колеблеться от 0 до 1.
-
степень приближения параболической
адсорбции от концентрации к прямолинейной
зависимости. Данный коэффициент
колеблеться от 0 до 1.

Кинетика гетерогенных процессов. Диффузионные процессы. Законы Фика.
Гетерогенными процессами – процессы, протекающие на границе раздела фаз: окисление металла кислородом воздуха, процессы на поверхности катализа, физико-химические процессы (растворение твёрдых тел и газов в жидкостях).
Особенность протекания гетерогенных процессов:
Зависимость протекания гетерогенных процессов от размера и состояния поверхности раздела фаз.
Многостадийность.
В любых гетерогенном процессе существует химическое превращение, протекающее на границе раздела фаз, а также транспорт исходных веществ и продуктов реакции.
Для гетерогенного процесса суммарная скорость будет определяться наиболее медленной стадией, т.к. процессы протекают последовательно. Следовательно, гетерогенный процесс может протекать в двух областях:
Кинетической, при условии, если химическая реакция имеет самую медленную скорость.
Диффузионной, если самой медленной стадией является транспорт веществ.
При изменении условий протекания реакций процесс может перейти из кинетической области в диффузионную, или наоборот.
Диффузионные процессы описываются законом Фика:
Масса вещества
 переносимого путём диффузии в направлении
оси
переносимого путём диффузии в направлении
оси
 через перпендикулярную этому направлению
площадку за
через перпендикулярную этому направлению
площадку за
 пропорционален площади площадки,
времени и градиенту концентрации вдоль
этого направления.
пропорционален площади площадки,
времени и градиенту концентрации вдоль
этого направления.

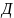 -
коэффициент
диффузии
-
коэффициент
диффузии

Устанавливает зависимость
 при условии фиксированного сечения:
при условии фиксированного сечения:

